《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)26Al和27Al_______(选填编号)。
(2)碳元素的一种核素也可以考古断代,其原子符号为_______ ;
(3)10 g10Be所含的中子数与质子数之差为_______ 个。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。硅原子的结构示意图为 _______ ,核外能量最高的电子位于_______ (填电子层符号)层。
(1)26Al和27Al_______(选填编号)。
| A.是同一种元素 | B.是同一种核素 | C.具有相同的中子数 | D.具有相同的化学性质 |
(3)10 g10Be所含的中子数与质子数之差为
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的
更新时间:2022-11-05 09:27:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】核外电子排布与化学键。在含有多个电子的原子例,电子的能量不同,根据电子能量的差异,电子应先排布在能量最低的电子层例,然后再依次由里向外排布在能量逐渐升高的电子层例,即分层排布。亨利·莫斯莱和查尔斯·巴克拉的X-射线吸收研究首次与实验中发现电子层。巴克拉把他们称为K、L、M、N(以英文字母排列)等电子层,这些字母后来被n值1、2、3等取代。
(1)结构示意图可以简明地表示微粒的核外电子排布,是一种用于表示原子或离子整体结构的图示。电子式是一类反应原子最外层电子情况,以及微粒之间化学键种类的化学语言。下列表示式正确的是___________
(2)在1916年,G.N。Lewis在讲述他的化学键理论时提出了电子式,故电子式又被称为路易斯式。根据经典的共价键理论,在形成化合物时,原子核外的单电子要尽可能地进行配对,并达到8电子稳定结构(H为2电子稳定结构)。写出 的电子式:
的电子式:___________ 。
(3)在元素周期表中,原子按核电荷数和原子核外电子排布的周期性变化进行排列。一些元素的原子易失去电子或得到电子形成离子,使最外层达到稳定结构。

如表所示是元素周期表的一部分,A、B、C均为短周期元素。已知B、C原子核外电子数之和是A原子核外电子数的4倍,则以下叙述中正确的是___________
(4)化学键(chemical bond)是纯净物分子内或晶体内相邻两个或多个原子(或离子)间强烈的相互作用力的统称。常见的化学键有离子键和共价键。离子键是由正离子和负离子之间相互的静电作用力形成的。共价键是由两个或多个原子共同使用他们的外层电子,在理想的情况下达到电子饱和状态,由此组成比较稳定的化学结构。在下列物质中:
①Ar ②SiC ③NaCl ④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦
其中,存在离子键的物质有___________ (填编号,下同),存在共价键的物质有___________ 。
(5)一般来说,主族元素的性质会随原子序数增加而呈现的变化,称为元素周期律。元素的非金属性表现为元素原子的得电子能力,元素非金属越的强弱会影响非金属单质的氧化性、气态氢化物的稳定性等等。下列物质的性质与解释均正确,且对应关系也正确的是___________
(1)结构示意图可以简明地表示微粒的核外电子排布,是一种用于表示原子或离子整体结构的图示。电子式是一类反应原子最外层电子情况,以及微粒之间化学键种类的化学语言。下列表示式正确的是
A.硫离子的结构示意图: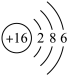 | B.钾原子的结构示意图: |
C.氯离子的电子式: | D.镁离子的电子式: |
 的电子式:
的电子式:(3)在元素周期表中,原子按核电荷数和原子核外电子排布的周期性变化进行排列。一些元素的原子易失去电子或得到电子形成离子,使最外层达到稳定结构。

如表所示是元素周期表的一部分,A、B、C均为短周期元素。已知B、C原子核外电子数之和是A原子核外电子数的4倍,则以下叙述中正确的是
| A.A、B、C都是非金属元素 | B.A、B、C最高价氧化物的水化物均为强酸 |
| C.A、B、C三种核电荷数之和是39 | D.B与A、C均能形成离子化合物 |
①Ar ②SiC ③NaCl ④
 ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦
其中,存在离子键的物质有
(5)一般来说,主族元素的性质会随原子序数增加而呈现的变化,称为元素周期律。元素的非金属性表现为元素原子的得电子能力,元素非金属越的强弱会影响非金属单质的氧化性、气态氢化物的稳定性等等。下列物质的性质与解释均正确,且对应关系也正确的是
| 选项 | 性质 | 解释 |
| A | 还原性: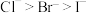 | Cl、Br、I的非金属性依次减弱 |
| B | 沸点: | N的非金属性比P强 |
| C | 分解温度: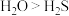 | O的非金属性比S强 |
| D | 酸性: | Cl的非金属比S强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)写出⑦的原子结构示意图:___________ 。
(2)元素④、⑩、⑪的简单气态氢化物的稳定性最强的是___________ (用化学式表示,下同),元素②、③简单氢化物沸点较高的是___________ 。
(3)元素⑤、⑥最高价氧化物对应的水化物碱性强的是___________ ,元素⑪最高价氧化物对应的水化物的化学式是___________ 。
(4)元素⑤与⑩形成化合物的电子式___________ 。
(5)元素①与⑩形成的最简单化合物中化学键类型为___________ (填“离子键”或“共价键”)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)元素④、⑩、⑪的简单气态氢化物的稳定性最强的是
(3)元素⑤、⑥最高价氧化物对应的水化物碱性强的是
(4)元素⑤与⑩形成化合物的电子式
(5)元素①与⑩形成的最简单化合物中化学键类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1) 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为_______ ;其价电子排布图为_______ 。
(2) 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为_______ , 离子的结构示意图为
离子的结构示意图为_______ 。
(3) 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ ,其原子的结构示意图为_______ 。
(4) 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ 。
(5) 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
_______ ;原子中能量最高的是_______ 电子,核外电子排布图为_______ 。
(1)
 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为(2)
 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为 离子的结构示意图为
离子的结构示意图为(3)
 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为(4)
 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为(5)
 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】原子中各粒子的作用
(1)___________ 数决定元素种类,同种元素的不同___________ ,其___________ 数相同,___________ 数不同。
(2)___________ 数和___________ 数共同决定了原子(核素)的种类。
(3)元素的化学性质决定于___________ ,特别是___________ 是决定元素化学性质的主要因素。
(1)
(2)
(3)元素的化学性质决定于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)1 mol NH3中所含质子数与____ molH2O、___ mol HF中所含质子数相等。
(2)和Ne原子具有相同电子数和质子数的多核微粒有____________ 。
(2)和Ne原子具有相同电子数和质子数的多核微粒有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】核外电子排布规律
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按___________ 顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳___________ 个电子,K、L、M、N层最多容纳的电子数依次为2、8、18、32。
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为___________ 。
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为___________ 。
(1)能量最低原理
电子总是尽可能先从内层排起,当一层充满后再填充下一层,即按
(2)电子层最多容纳的电子数
①第n层最多容纳
②K层为最外层时最多容纳的电子数为2,除K层外,其他各层为最外层时,最多容纳的电子数为
③K层为次外层时,所排电子数为2,除K层外,其他各层为次外层时,最多容纳的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在 H,
H, H,
H,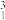 H,
H, Mg,
Mg,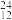 Mg,
Mg, O,
O,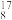 O,
O,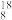 O中共有
O中共有___________ 种元素,___________ 种原子,中子数最多的是___________ ;D218O的相对分子质量是___________ ;下列各分子中,所有原子都满足最外层为8电子结构的是___________ 。
A.H2O B.BF3 C.CCl4 D.PCl5
(2)在H2O2、KCl、Na2O2、HCl、O2中只含离子键的是___________ ,只含极性键的是___________ ,既含离子键又含非极性键的是___________ ,既有极性键又有非极性键的是___________ 。
(3)已知拆开1mol H—H键、1mol N≡N、1mol N—H键分别需要吸收的能量为436kJ、946kJ、391kJ。则由N2和H2反应生成1mol NH3需要___________ (填“放出”或“吸收”)热量为___________ kJ。
(4)在体积为2 L密闭容器中加入反应物A、B,发生如下反应:A+2B=3C,经2min后,A的浓度从开始时的1.0 mol/L降到0.8 mol/L。已知反应开始时B的浓度是1.2 mol/L。则:2min末 B的浓度___________ mol/L、C的物质的量___________ mol,2min内,用A物质的浓度变化来表示该反应的反应速率,即v(A) =___________ mol/L·min。
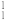 H,
H, H,
H,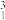 H,
H, Mg,
Mg,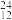 Mg,
Mg, O,
O,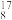 O,
O, O中共有
O中共有A.H2O B.BF3 C.CCl4 D.PCl5
(2)在H2O2、KCl、Na2O2、HCl、O2中只含离子键的是
(3)已知拆开1mol H—H键、1mol N≡N、1mol N—H键分别需要吸收的能量为436kJ、946kJ、391kJ。则由N2和H2反应生成1mol NH3需要
(4)在体积为2 L密闭容器中加入反应物A、B,发生如下反应:A+2B=3C,经2min后,A的浓度从开始时的1.0 mol/L降到0.8 mol/L。已知反应开始时B的浓度是1.2 mol/L。则:2min末 B的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下列物质中,互为同系物的有_______ ,互为同分异构体的有_______ ,互为同素异形体的有_______ ,属于同位素的有_______ ,是同一种物质的有_______ 。
①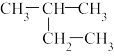 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④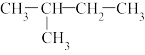 ;⑤
;⑤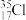 ;⑧红磷;⑦
;⑧红磷;⑦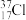 ;⑧
;⑧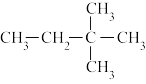
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为_______ ;
②发生1,4-加成反应的化学方程式为_______ 。
(1)下列物质中,互为同系物的有
①
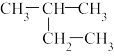 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④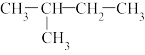 ;⑤
;⑤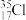 ;⑧红磷;⑦
;⑧红磷;⑦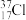 ;⑧
;⑧
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为
②发生1,4-加成反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】1.某核素 的氯化物
的氯化物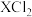 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数A______________ 。
(2)若X的核内中子数为20,求37g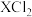 中所含质子的物质的量是
中所含质子的物质的量是______________
2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是______________ ,属于非电解质的是______________
(2)书写硫酸铁电离方程式:_______________________ 书写氯酸钾电离方程式:_______________________
 的氯化物
的氯化物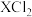 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:(1)X的质量数A
(2)若X的核内中子数为20,求37g
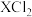 中所含质子的物质的量是
中所含质子的物质的量是2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是
(2)书写硫酸铁电离方程式:
您最近一年使用:0次



