回答下列问题:
(1) 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为_______ ;其价电子排布图为_______ 。
(2) 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为_______ , 离子的结构示意图为
离子的结构示意图为_______ 。
(3) 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ ,其原子的结构示意图为_______ 。
(4) 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为_______ ,其基态原子的电子排布式为_______ 。
(5) 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
_______ ;原子中能量最高的是_______ 电子,核外电子排布图为_______ 。
(1)
 元素基态原子的最外层有
元素基态原子的最外层有 个未成对电子,次外层有
个未成对电子,次外层有 个电子,其元素符号为
个电子,其元素符号为(2)
 元素的负一价离子和
元素的负一价离子和 元素的正一价离子的电子层结构都与氩相同,
元素的正一价离子的电子层结构都与氩相同, 的元素符号为
的元素符号为 离子的结构示意图为
离子的结构示意图为(3)
 元素的正三价离子的
元素的正三价离子的 能级为半充满,
能级为半充满, 的元素符号为
的元素符号为(4)
 元素基态原子的
元素基态原子的 层全充满,
层全充满, 层没有成对电子且只有一个未成对电子,
层没有成对电子且只有一个未成对电子, 的元素符号为
的元素符号为(5)
 元素的原子最外层电子排布式为
元素的原子最外层电子排布式为 ,则
,则
更新时间:2023-03-19 20:55:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求写出下列微粒的化学符号。
(1)3个镁离子_______ 。
(2)质量数为35的氯离子_______ 。
(3)铝离子的结构示意图_______ 。
(4)硫离子的电子式_______ 。
(5)写一个含有10个电子的阳离子:_______ (化学符号)。
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:_______
(1)3个镁离子
(2)质量数为35的氯离子
(3)铝离子的结构示意图
(4)硫离子的电子式
(5)写一个含有10个电子的阳离子:
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高压碳酸盐化学
常温常压下,碳酸根通常以分离的 基团形式存在,但在高压下可发生聚合,甚至改变配位方式形成类似于硅酸根及其多聚阴离子的结构。
基团形式存在,但在高压下可发生聚合,甚至改变配位方式形成类似于硅酸根及其多聚阴离子的结构。
(1)在20Gpa高压下,用激光加热 和SrO的混合物,得到组成为
和SrO的混合物,得到组成为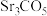 的物质,其结构类似于钙钛矿
的物质,其结构类似于钙钛矿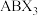 ,其中
,其中 八面体共顶点连接,写出
八面体共顶点连接,写出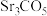 中分别对应于A
中分别对应于A______ 、B_______ 、X________ 的离子(须注明电荷)。
(2)在 的高压下,
的高压下, 中碳酸根形成环状三聚体(C),画出C的结构示意图
中碳酸根形成环状三聚体(C),画出C的结构示意图_____ 。在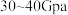 的高压下,用激光加热
的高压下,用激光加热 (M=Ca或Sr)和干冰的混合物,得到组成为
(M=Ca或Sr)和干冰的混合物,得到组成为 的物质。
的物质。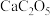 中,碳酸根以四聚形式(D)存在;
中,碳酸根以四聚形式(D)存在; 中,碳酸根以二聚形式(E)存在,画出D和E的结构。D:
中,碳酸根以二聚形式(E)存在,画出D和E的结构。D:________ ;E:_______
常温常压下,碳酸根通常以分离的
 基团形式存在,但在高压下可发生聚合,甚至改变配位方式形成类似于硅酸根及其多聚阴离子的结构。
基团形式存在,但在高压下可发生聚合,甚至改变配位方式形成类似于硅酸根及其多聚阴离子的结构。(1)在20Gpa高压下,用激光加热
 和SrO的混合物,得到组成为
和SrO的混合物,得到组成为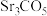 的物质,其结构类似于钙钛矿
的物质,其结构类似于钙钛矿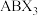 ,其中
,其中 八面体共顶点连接,写出
八面体共顶点连接,写出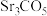 中分别对应于A
中分别对应于A(2)在
 的高压下,
的高压下, 中碳酸根形成环状三聚体(C),画出C的结构示意图
中碳酸根形成环状三聚体(C),画出C的结构示意图 的高压下,用激光加热
的高压下,用激光加热 (M=Ca或Sr)和干冰的混合物,得到组成为
(M=Ca或Sr)和干冰的混合物,得到组成为 的物质。
的物质。 中,碳酸根以四聚形式(D)存在;
中,碳酸根以四聚形式(D)存在; 中,碳酸根以二聚形式(E)存在,画出D和E的结构。D:
中,碳酸根以二聚形式(E)存在,画出D和E的结构。D:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】结合如图六种微粒的结构示意图,回答下列问题:

(1)粒子④在化学反应中易___ (填“失”或“得”)电子,形成___ (填符号)。
(2)①—⑤五种粒子中化学性质相似的是___ (填序号)。
(3)①—⑥六种粒子中具有相对稳定结构的是___ (填序号)。
(4)若⑥表示某阴离子的结构示意图,则X可能是下列中的___ (填字母序号)。
a.16 b.17 c.18 d.19
(5)若某元素的阳离子X2+核外有28个电子,相对原子质量为65,则X原子核内中子数与质子数之差为___ 。

(1)粒子④在化学反应中易
(2)①—⑤五种粒子中化学性质相似的是
(3)①—⑥六种粒子中具有相对稳定结构的是
(4)若⑥表示某阴离子的结构示意图,则X可能是下列中的
a.16 b.17 c.18 d.19
(5)若某元素的阳离子X2+核外有28个电子,相对原子质量为65,则X原子核内中子数与质子数之差为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】今年是诺贝尔奖颁发120周年,其中很多获得诺贝尔化学奖的研究成果都极大的影响着我们的生活。请回答与诺贝尔化学奖获奖成果相关的下列问题:
(1)1995年,诺贝尔化学奖授予Paul Crutzen、Mario Molina 和F.S Rowland 三位科学家,以表彰他们在平流层臭氧化学研究领域所做出的贡献。氟利昂(CCl2F2等)及氮的氧化物在O3分解中起重要作用,N、O、F的第一电离能由大到小的顺序为___________ 。
(2)2019年,诺贝尔化学奖授予John B Goodenough,M.stanley Whittlingham 和 Akira Yoshino,以表彰他们在锂离子电池的发展方面作出的卓越贡献。
①从原子结构理论角度解释,Fe3+比Fe2+稳定的原因为___________ 。
②早在1973年,Whittingham 发现一种极强富能材料TiS2,以此作为锂电池的全新阴极。Ti的基态原子核外电子排布式为___________ 。下列硫的各种微粒中,电离最外层一个电子所需能量最大的是___________ 。(填字母)。
A.[Ne]3s23p3 B.[Ne]3s23p4 C.[Ne]3s23p33d1 D.[Ne]3s23p5
(1)1995年,诺贝尔化学奖授予Paul Crutzen、Mario Molina 和F.S Rowland 三位科学家,以表彰他们在平流层臭氧化学研究领域所做出的贡献。氟利昂(CCl2F2等)及氮的氧化物在O3分解中起重要作用,N、O、F的第一电离能由大到小的顺序为
(2)2019年,诺贝尔化学奖授予John B Goodenough,M.stanley Whittlingham 和 Akira Yoshino,以表彰他们在锂离子电池的发展方面作出的卓越贡献。
①从原子结构理论角度解释,Fe3+比Fe2+稳定的原因为
②早在1973年,Whittingham 发现一种极强富能材料TiS2,以此作为锂电池的全新阴极。Ti的基态原子核外电子排布式为
A.[Ne]3s23p3 B.[Ne]3s23p4 C.[Ne]3s23p33d1 D.[Ne]3s23p5
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)Fe成为阳离子时首先失去___ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___ 。
(2)Cu2+基态核外电子排布式为___ 。
(3)Mn位于元素周期表中第四周期___ 族,基态Mn原子核外未成对电子有___ 个。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___ 、__ (填标号)。
(2)Cu2+基态核外电子排布式为
(3)Mn位于元素周期表中第四周期
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
B.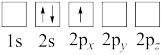
C.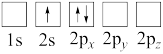
D.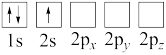
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为______ 。
(2)写出与H2O分子互为等电子体的微粒________________ (填2种)。
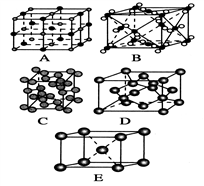
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为_________ ,与冰的晶体类型相同的是________ (请用相应的编号填写)
(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有___ 个K+和___ 个O2— ;晶体中K+ 的配位数为___ ,O2— 的配位数为______ 。
(5)60 g 金刚石中的共价键数为_________ 个,60g SiO2晶体中的共价键数为_______ 个。
(1)水分子中氧原子在基态时核外电子排布式为
(2)写出与H2O分子互为等电子体的微粒
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为

(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有
(5)60 g 金刚石中的共价键数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________ 。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是________ 。
(3)单质铜及镍都是由______ 键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1,ICu> INi的原因是_______________________ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为
(3)单质铜及镍都是由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)简化的氯离子的电子排布式:___________ ,P原子的价层电子轨道表示式:___________ ,基态Cu原子的电子排布式为:___________
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ 。
(3)PO 离子的空间构型为
离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
(1)简化的氯离子的电子排布式:
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)PO
 离子的空间构型为
离子的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)基态N原子的价电子轨道表示式为_______ ,基态N原子中电子占据最高能级的电子云轮廓图为_______ 形; 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是_______ ,分子中的N原子杂化方式为_______ 。
(2)B元素在周期表中的位置_______ ,B的第一电离能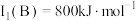 ,判断
,判断
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是_______ 。
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(1)基态N原子的价电子轨道表示式为
 分子中存在配位键,提供空轨道的原子是
分子中存在配位键,提供空轨道的原子是(2)B元素在周期表中的位置
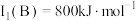 ,判断
,判断
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:电负性由大到小的顺序是
。在H、B、N三种元素中:电负性由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态硼原子的价电子轨道表达式是___________ 。
(2)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
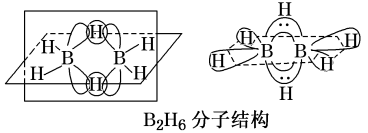
①B2H6分子结构如图,则B原子的杂化方式为___________ 。
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是___________ ,写出一种与氨硼烷互为等电子体的分子:___________ (填化学式)。
(3)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。 的键角是
的键角是___________ ,立体构型为___________ 。
(1)基态硼原子的价电子轨道表达式是
(2)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(3)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
 的键角是
的键角是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢、碳、氮、氧元素的单质及化合物在很多领域有着广泛的应用。回答下列问题:
(1)画出基态N原子的价电子轨道表示式___________ ,核外有___________ 种电子运动状态。
(2)下列微粒中:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦HCN,既有
⑦HCN,既有 键又有
键又有 键的是
键的是___________ (填序号); 中
中 键和
键和 键的数目比为
键的数目比为___________ ,其空间构型为___________ 。
(3) 的电子式
的电子式___________ ,键角
___________  (填“大于”“小于”“等于”,下同),热稳定性:
(填“大于”“小于”“等于”,下同),热稳定性:
___________  。
。
(4) (二氟氮烯)分子中的氮原子采用
(二氟氮烯)分子中的氮原子采用 杂化,则
杂化,则 的结构式为
的结构式为___________ 。
(5)重铬酸铵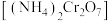 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。1mol
的结构如图。1mol 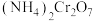 中
中 键数目为
键数目为___________  。
。
(1)画出基态N原子的价电子轨道表示式
(2)下列微粒中:
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦HCN,既有
⑦HCN,既有 键又有
键又有 键的是
键的是 中
中 键和
键和 键的数目比为
键的数目比为(3)
 的电子式
的电子式
 (填“大于”“小于”“等于”,下同),热稳定性:
(填“大于”“小于”“等于”,下同),热稳定性:
 。
。(4)
 (二氟氮烯)分子中的氮原子采用
(二氟氮烯)分子中的氮原子采用 杂化,则
杂化,则 的结构式为
的结构式为(5)重铬酸铵
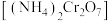 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。1mol
的结构如图。1mol 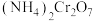 中
中 键数目为
键数目为 。
。
您最近一年使用:0次



