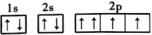(1)Fe成为阳离子时首先失去___ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___ 。
(2)Cu2+基态核外电子排布式为___ 。
(3)Mn位于元素周期表中第四周期___ 族,基态Mn原子核外未成对电子有___ 个。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___ 、__ (填标号)。
(2)Cu2+基态核外电子排布式为
(3)Mn位于元素周期表中第四周期
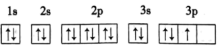
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
B.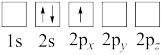
C.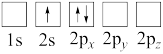
D.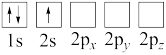
20-21高二下·湖北武汉·阶段练习 查看更多[6]
江西省南昌十九中2022-2023学年高二上学期期末考试化学试卷 第一章 原子结构与性质(A卷·知识通关练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)第一章原子结构与性质(提升卷)(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)作业01 原子结构-2021年高二化学暑假作业(人教版2019)湖北省武汉市江夏实验高中2020-2021学年高二下学期3月月考化学试题
更新时间:2021-05-08 12:52:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍_____________ ;
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3___________ ;
(3)最外层电子数不会超过8个,次外层电子数不会超过18个_____________ ;
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2________ ;
(5)磷原子的基态原子结构中,有3个未成对的单电子____________ 。
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3
(3)最外层电子数不会超过8个,次外层电子数不会超过18个
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2
(5)磷原子的基态原子结构中,有3个未成对的单电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)某元素的原子序数为33,则:
①此元素原子的电子总数是________ ;
②有________ 个能层,________ 个能级;
③它的电子排布式为_____________________________________________________________ 。
(2)写出下列基态原子或离子的电子排布式:
①S________ ;②Ca2+________ ;③Cl-________ ;④Ni2+________ ;⑤Ge________ ;⑥Mn2+________ 。
①此元素原子的电子总数是
②有
③它的电子排布式为
(2)写出下列基态原子或离子的电子排布式:
①S
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原子结构与元素周期表存在着内在联系。请你回答下列问题:
(1)前四周期的36种元素中,未成对电子数最多的元素是__________ 。(填元素符号)
(2)价电子排布式为3d104s1的元素是__________ 。(填名称)
(3)铁在周期表中的位置是_____________ ;其原子的电子排布式为_______________ 。
(4)有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:若某中性微粒,一般不和其他物质反应,这种微粒符号是____________ 。若某微粒还原性很弱,但失去1个电子后氧化性很强,这种微粒符号是________ 。若某微粒氧化性很弱,但得到2个电子后还原性很强,这种微粒符号是________ 。
(1)前四周期的36种元素中,未成对电子数最多的元素是
(2)价电子排布式为3d104s1的元素是
(3)铁在周期表中的位置是
(4)有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:若某中性微粒,一般不和其他物质反应,这种微粒符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O=== [Zn(H2O)4]2++4HOCH2CN

(1)Zn2+基态核外电子排布式为________ 。
(2)1 mol HCHO分子中含有σ键的数目为_______ mol。
(3)HOCH2CN分子中碳原子轨道的杂化轨道类型是________ 。
(4)与H2O分子互为等电子体的阴离子为_____________ 。
(5)C、N、O第一电离能由小到大的顺序__________ 。
(6)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_____________ 。
4HCHO+[Zn(CN)4]2-+4H++4H2O=== [Zn(H2O)4]2++4HOCH2CN

(1)Zn2+基态核外电子排布式为
(2)1 mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化轨道类型是
(4)与H2O分子互为等电子体的阴离子为
(5)C、N、O第一电离能由小到大的顺序
(6)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请根据所学知识回答下列问题:
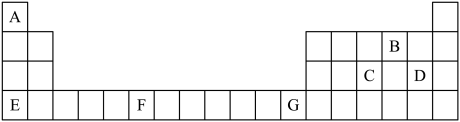
(1)B、C、D三种元素的电负性由大到小的顺序是_______ (用元素符号表示)。B、C、D的简单离子半径由大到小的顺序是_______ (填离子符号),A2B2为_______ (填“极性”或“非极性”)分子,形成的晶体类型为_______ 。
(2)上述元素的原子中,未成对电子数最多的是_______ (填名称),写出该元素基态原子的核外电子排布式:_______ 。
(3)上述7种元素中金属性最强的为_______ (填名称)。该元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为_______ ,其中所含的化学键类型为_______ 。

(1)B、C、D三种元素的电负性由大到小的顺序是
(2)上述元素的原子中,未成对电子数最多的是
(3)上述7种元素中金属性最强的为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)C、N、O、Al、Si、Cu是常见的六种元素。
①Si位于元素周期表第________ 周期第________ 族。
②C的基态原子核外电子排布式为________ ;Cu的基态原子最外层有________ 个电子。
(2)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是________ (填写元素符号)。
②基态锗(Ge)原子的电子排布式是________ 。Ge的最高价氯化物的分子式是________ 。
③Ge元素可能的性质或应用有________ 。
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
①Si位于元素周期表第
②C的基态原子核外电子排布式为
(2)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | …… |
| In/(kJ·mol-1) | 578 | 1 817 | 2 745 | 11 578 | …… |
则该元素是
②基态锗(Ge)原子的电子排布式是
③Ge元素可能的性质或应用有
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】请完成下列各题:
(1)前4周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有________ 种。
(2)第ⅢA、ⅤA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。在GaN晶体中,每个Ga原子与________ 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为____________ 。在四个晶体类型中,GaN属于________ 晶体。
(3)在极性分子NCl3(遇水强烈水解)中,N原子的化合价为-3价,Cl原子的化合价为+1价,请推测NCl3水解的主要产物是________________ (填化学式)。
(1)前4周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有
(2)第ⅢA、ⅤA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。在GaN晶体中,每个Ga原子与
(3)在极性分子NCl3(遇水强烈水解)中,N原子的化合价为-3价,Cl原子的化合价为+1价,请推测NCl3水解的主要产物是
您最近一年使用:0次
【推荐3】地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素。它们在化学中占有极其重要的地位。
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为___________
②金属钠原子的堆积方式是体心立方,其配位数为___________
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈___________ 色的物质是水合铜离子,请写出它的结构简式,并标明其中配位键___________
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式___________
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有___________ molσ键。
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:___________ (要求:仅写1个总的离子方程式)
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为
②金属钠原子的堆积方式是体心立方,其配位数为
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:
您最近一年使用:0次

 :
:
 :
:
 :
:
 :
: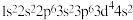
 :
:
 :
: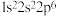
 :
: