《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。
(1)27Al是地壳中最丰富的金属元素,其原子含有中子数为_______ ,与26Al互为_______ 。
(2)用化学符号表示:铝离子的结构示意图_______ ,硅原子的电子式_______ 。
(3)Al与Al3+两种微粒结构上相同的是_______(填选项字母)。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si,计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。核外能量最高的电子位于_______ (填电子层符号)层。
(5)A、B、C、D四种微粒都含10个电子,若A++B- C+D↑,则A+和B-分别是
C+D↑,则A+和B-分别是_______ 、______ 。除C、D外,再写出2个含10个电子的分子_______ 、______ 。
(6)10g10Be所含的中子数与质子数之差为_______ 个。
(1)27Al是地壳中最丰富的金属元素,其原子含有中子数为
(2)用化学符号表示:铝离子的结构示意图
(3)Al与Al3+两种微粒结构上相同的是_______(填选项字母)。
| A.质子数 | B.中子数 | C.电子层数 | D.最外层电子数 |
(5)A、B、C、D四种微粒都含10个电子,若A++B-
 C+D↑,则A+和B-分别是
C+D↑,则A+和B-分别是(6)10g10Be所含的中子数与质子数之差为
更新时间:2023-01-13 15:54:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】甲烷的分子式:_______ ,电子式:_______ ,结构式:_______ ,可知碳原子最外层有_______ 个电子,能形成_______ 个_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请回答:
(1)NH4Cl的电子式:___________ 。
(2)HClO的结构式:___________ 。
(3)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是___________ 。
(4)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为___________ 。
(5)金属铝和氢氧化钠溶液反应的化学方程式为___________ 。
(1)NH4Cl的电子式:
(2)HClO的结构式:
(3)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是
(4)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为
(5)金属铝和氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)已知:A、B属于1-18号元素,且核电荷数A<B,A元素的原子核外M层电子数是L层电子数的一半;B元素的原子次外层电子数比最外层电子数多1个。试写出A原子结构示意图为:___________ ,B形成简单离子的电子式为___________ 。
(2)标准状况下,8.96LCH4和CO的混合气体,其质量为7.6g,则混合气体中CH4的体积为_______ L,CO的质量为_________ g。
(3)___________ molCO2中含有的氧原子数与1.806×1024个H2O分子中含有的氧原子数相同。
(4)0.4molSiH4分子中所含原子数与___________ gHCl分子中所含原子数相等。
(1)已知:A、B属于1-18号元素,且核电荷数A<B,A元素的原子核外M层电子数是L层电子数的一半;B元素的原子次外层电子数比最外层电子数多1个。试写出A原子结构示意图为:
(2)标准状况下,8.96LCH4和CO的混合气体,其质量为7.6g,则混合气体中CH4的体积为
(3)
(4)0.4molSiH4分子中所含原子数与
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某元素的基态原子最外层电子排布式为nsnnpn+2,则n=_______ ;基态原子中能量最高的是_______ 电子,核外电子的轨道表示式为_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求完成题目。
(1)写出含有6个质子,8个中子的原子的化学符号是_______ 。
(2)用“<”或“>”填空:酸性:H2SO4_______ HClO4 ;H2CO3_______ H2SiO3
(3)电子总数为18的正一价的单核阳离子的结构示意图________ ,
(4)与氩原子电子层结构相同的-2价阴离子的结构示意图_____________ 。
(1)写出含有6个质子,8个中子的原子的化学符号是
(2)用“<”或“>”填空:酸性:H2SO4
(3)电子总数为18的正一价的单核阳离子的结构示意图
(4)与氩原子电子层结构相同的-2价阴离子的结构示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-与Ar原子电子层结构相同;X是短周期主族元素中原子半径最小的;Z是短周期主族元素中原子半径最大的;化合物XN常温下为气体。据此回答:
(1)N的最高价氧化物对应水化物的化学式是_______ 。
(2)Z与M形成的化合物水溶液显碱性,其原因是_______ (用离子方程式表示)。
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是_______ ,反应的化学方程式是_______ 。
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式_______ 。
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是_______ 。
(6)如图所示:
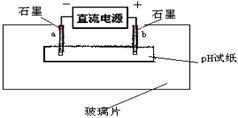
取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是_______ 。
(1)N的最高价氧化物对应水化物的化学式是
(2)Z与M形成的化合物水溶液显碱性,其原因是
(3)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应可观察到的现象是
(4)由X、Y、Z、M四种元素组成一种强酸的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式
(5)Y、Z、N形成的化合物的水溶液中离子浓度的大小顺序是
(6)如图所示:

取一张用ZN溶液浸湿的pH试纸平铺在玻璃片上,取两根石墨棒做电极,接通直流电源。一段时间后,a电极处的pH试纸上可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】理解化学用语的内涵和外延,掌握背后的规律性内容,是步入化学学科的必经之路。请用相应的化学用语回答下列问题:
(1)1911年,卢瑟福在α粒子的散射实验中,用α粒子轰击氮原子核,发现了质子的存在,提出了原子的核式结构,该核反应为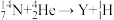 ,则Y的核素符号为
,则Y的核素符号为___________ 。
(2)Sr是第五周期第IIA族元素,用电子式表示SrF2的形成过程___________ 。
(3)汽车安全气囊中的主要物质为NaN3,此物质中共价键的类型为___________ 。
(4)元素周期表的第三周期元素中,最高价氧化物对应的水化物呈两性的是___________ (填元素符号,下同);最高价氧化物对应的水化物的酸性最强的是___________ 。
(1)1911年,卢瑟福在α粒子的散射实验中,用α粒子轰击氮原子核,发现了质子的存在,提出了原子的核式结构,该核反应为
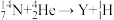 ,则Y的核素符号为
,则Y的核素符号为(2)Sr是第五周期第IIA族元素,用电子式表示SrF2的形成过程
(3)汽车安全气囊中的主要物质为NaN3,此物质中共价键的类型为
(4)元素周期表的第三周期元素中,最高价氧化物对应的水化物呈两性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
Ⅰ.图是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:
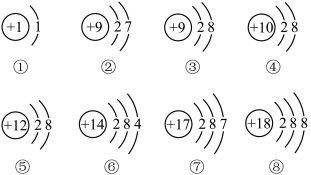
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是_______ ;在化学反应中容易得到电子的是_______ ;属于阳离子的是_______ ;表示F-的是_______ ;属于同一种元素的是_______ ;属于非金属元素的是_______ ;电子层数相同,最外层电子数也相同的粒子有_______ 。
Ⅱ.某微粒的结构示意图可表示为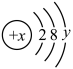 。
。
(2)当x=10+y时,该粒子为_______ (填“原子”“阳离子”或“阴离子”),当x<10+y时,该粒子为_______ 。
(3)当y=2时,x=_______ 。该元素能形成的离子符号为_______ 。
(4)若该结构示意图表示的粒子是R-,则x=_______ ,y=_______ 。
Ⅰ.图是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:

(1)用序号填空:上述粒子中,属于稀有气体元素的原子是
Ⅱ.某微粒的结构示意图可表示为
 。
。(2)当x=10+y时,该粒子为
(3)当y=2时,x=
(4)若该结构示意图表示的粒子是R-,则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学计量和化学用语在化学中占有重要地位,请回答下列问题。
(1)含0.4 mol·L-1 Al3+的Al2(SO4)3溶液,取10 mL该溶液,加水稀释为100 mL溶液,稀释后的溶液中c(SO )=
)=___________ mol·L-1。
(2)标准状况下,6.72LNH3分子中所含原子数与___________ mol H2O分子中所含原子数相等。
(3)9.8 g硫酸溶解在___________ g水中,使H+与H2O个数比为1∶50(忽略水的电离)。
(4)中子数为14的铝原子,其微粒符号可表示为___________ 。
(5)质量数为35,中子数为18的原子,其原子结构示意图可表示为___________ 。
(6)已知KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。反应中氧化剂与还原剂的物质的量之比为___________ 。
(1)含0.4 mol·L-1 Al3+的Al2(SO4)3溶液,取10 mL该溶液,加水稀释为100 mL溶液,稀释后的溶液中c(SO
 )=
)=(2)标准状况下,6.72LNH3分子中所含原子数与
(3)9.8 g硫酸溶解在
(4)中子数为14的铝原子,其微粒符号可表示为
(5)质量数为35,中子数为18的原子,其原子结构示意图可表示为
(6)已知KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C- D+E↑;②B++C-===2D。
D+E↑;②B++C-===2D。
请回答:
(1)C-离子的电子式是________________ 。
(2)A+离子中的键角为______________ 。
(3)分别写出A+和D反应、B+和E反应的离子方程式____________ 、____________ 。
(4)除D、E外,请再写出两种含10个电子的分子的分子式____________ 。
(5)除A+、B+外,请再写出两种含10个电子的阳离子________ 。
①A++C-
 D+E↑;②B++C-===2D。
D+E↑;②B++C-===2D。请回答:
(1)C-离子的电子式是
(2)A+离子中的键角为
(3)分别写出A+和D反应、B+和E反应的离子方程式
(4)除D、E外,请再写出两种含10个电子的分子的分子式
(5)除A+、B+外,请再写出两种含10个电子的阳离子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)1 mol NH3中所含质子数与____ molH2O、___ mol HF中所含质子数相等。
(2)和Ne原子具有相同电子数和质子数的多核微粒有____________ 。
(2)和Ne原子具有相同电子数和质子数的多核微粒有
您最近一年使用:0次



