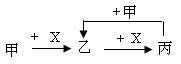
硫酸是重要的化工原料。稀硫酸具有酸的通性;浓硫酸具有很强的氧化性,能氧化大多数金属单质和部分非金属单质。金属冶炼时产生的含SO2废气经回收处理、催化氧化、吸收后可制得硫酸。2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。在指定条件下,下列选项所示的物质间转化能实现的是
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。在指定条件下,下列选项所示的物质间转化能实现的是
 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。在指定条件下,下列选项所示的物质间转化能实现的是
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。在指定条件下,下列选项所示的物质间转化能实现的是A.FeS2(s) SO3(g) SO3(g) | B.稀H2SO4(aq)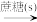 SO2(g) SO2(g) |
C.浓H2SO4(aq)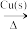 SO2(g) SO2(g) | D.SO2(g)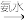 (NH4)2SO4(aq) (NH4)2SO4(aq) |
更新时间:2021-09-22 21:55:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
| A | 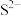 、 、 、 、 、 、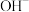 | 不能共存,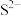 与 与 发生氧化还原反应生成S 发生氧化还原反应生成S |
| B |  、 、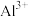 、 、 、 、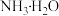 | 能够大量共存 |
| C |  、 、 、 、 、 、 | 不能共存, 能催化 能催化 分解 分解 |
| D |  、 、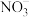 、 、 、 、 | 能够大量共存 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在给定条件下,下列物质间所示可以实现的是
A. | B.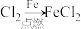 |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用图所示装置进行实验,下列对实验现象的解释不合理的是
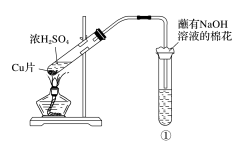

选项 | ①中试剂 | ①中现象 | 解释 |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | 含酚酞的NaOH溶液 | 红色消失 | SO2具有酸性氧化物的性质 |
C | Ba(NO3)2溶液 | 生成白色沉淀 |
|
D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“绿水青山就是金山银山”,为落实“五水共治”,某工厂拟综合处理含NH 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:

下列说法正确的是
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
下列说法正确的是
| A.固体1中含有CaSO3,再经还原可用于生产石膏 |
| B.X可以是空气,其作用是将CO转化为CO2 |
C.NaNO2与含有NH 的废水反应,有1molN2生成转移6mol电子 的废水反应,有1molN2生成转移6mol电子 |
| D.捕获产物的主要成分可用于工业炼铁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各组物质由于浓度不同而能发生不同氧化还原反应的是
①Cu与HNO3溶液;②NaOH与AlCl3溶液;③Zn与H2SO4溶液;④Na与O2反应
①Cu与HNO3溶液;②NaOH与AlCl3溶液;③Zn与H2SO4溶液;④Na与O2反应
| A.①③ | B.①② | C.③④ | D.①④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.1mol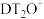 所含电子数为 所含电子数为 |
B.用溶有1mol 的饱和溶液制备 的饱和溶液制备 胶体,制成的胶体中含有的胶粒数为 胶体,制成的胶体中含有的胶粒数为 |
C.常温常压下,16g 和 和 的混合气体中含有O原子数目为 的混合气体中含有O原子数目为 |
D.50mL18.4mol/L浓硫酸与足量铜微热反应,生成 分子的数目为 分子的数目为 |
您最近一年使用:0次


 与Ba2+生成BaSO3白色沉淀
与Ba2+生成BaSO3白色沉淀