南开大学陈军院士团队通过对钾-二氧化碳电池正负极同时改进,实现了稳定高效且可遵循环的钾-二氧化碳电池。该电池原理如图所示,放电时Y极会有碳单质生成。下列说法错误的是
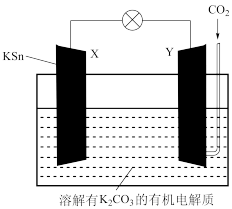

A.该装置不可将有机电解质换成 水溶液 水溶液 |
B.放电时,X极的电极反应式为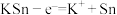 |
C.放电时,该装置转移4mol电子,Y极吸收44g |
D.放电一段时间后,有机电解质中的 浓度增大 浓度增大 |
更新时间:2021-10-19 19:41:25
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】一种新型中温全瓷铁-空气电池结构如图所示。下列有关该电池放电时的说法错误的是


| A.通入空气的电极为正极 |
| B.O2—由a极移向b极 |
C.正极的电极反应式为: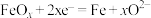 |
D.铁表面发生了反应: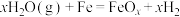 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
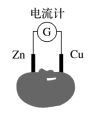
【推荐2】a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b 相连时,电流由a经导线流向b,c、d相连时,电子由d到c;a、c相连时,a极上产生大量气泡,b、d相连时,H+移向d极,则四种金属的活动性顺序由强到弱的顺序为
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>d>c>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2 LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法不正确的是
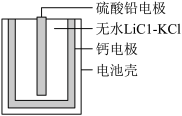

| A.负极反应式:Ca+2Cl﹣﹣2e﹣═CaCl2 |
| B.放电过程中,Li+向负极移动 |
| C.每转移0.2mol电子,理论上生成20.7gPb |
| D.常温时,在正负极间接上电流表或检流计,指针不偏转 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用反应6NO2+8NH3=7N2+12H2O,设计原电池(如图所示)。该反应既能有效降低氮氧化物的排放量,减轻环境污染,又能充分利用化学能。下列说法正确的是


| A.外电路中电子由电极B经负载后流向电极A |
| B.电池工作一段时间后,左右两侧电极室溶液的pH发生变化 |
| C.同温同压下,左右两侧电极室产生的气体体积比为3∶4 |
| D.电极A的电极反应式为2NH3-6e-=N2↑+6H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】锌—空气燃料电池有比能量高、容量大、使用寿命长等优点,可用作电动车动力电源,电池的电解质溶液为 KOH 溶液,放电时发生反应:2Zn + O2+4OH-+2H2O= 2[Zn(OH)4]2-。下列说法正确的是:
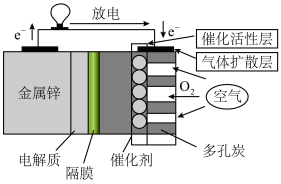

| A.放电时,负极反应为 Zn-2e- = Zn2+ |
| B.该隔膜为阳离子交换膜,允许K+通过 |
| C.充电时,当 0.1 molO2 生成时,流经电解质溶液的电子个数约为 1.204×1022 |
| D.采用多孔炭可提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中正确的是:
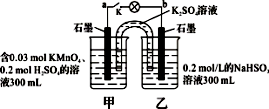

| A.当电路中有0.06 mol电子转移时,乙烧杯中溶液c(H+) 约为0.1 mol · L-1 |
| B.乙池中的还原产物为SO42- |
| C.电池工作时,甲烧杯中溶液的pH逐渐增大 |
| D.电池工作时,盐桥中的K+移向乙烧杯,外电路的电流方向是从b到a |
您最近一年使用:0次

 2Ni(OH)2,则下列说法正确的是(
2Ni(OH)2,则下列说法正确的是( 4Al2Cl7-+3Cn(Cn表示石墨)。下列说法正确的是(
4Al2Cl7-+3Cn(Cn表示石墨)。下列说法正确的是(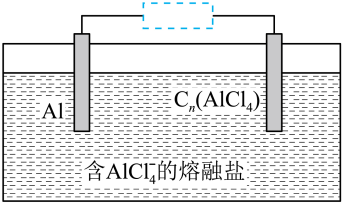
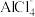 移向正极
移向正极

