部分物质的燃烧热如下表,下列关于CH4和水蒸气反应得到H2和CO的热化学方程式正确的是
注:1 mol H2O(g)转变成1 mol H2O(l)时放热44.0 kJ。
| 物质 | 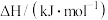 |
| H2 | -285.8 |
| CO | -283.0 |
| CH4 | -890.0 |
A. |
B. |
C.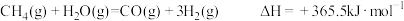 |
D. |
更新时间:2021-10-14 22:01:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是
A.同温同压下,反应 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
B.已知 , , ,则 ,则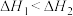 |
C.表示甲烷燃烧热的热化学方程式为: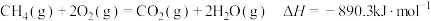 |
D. 和 和 反应中和热 反应中和热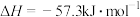 ,则: ,则: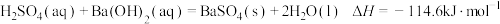 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式书写正确的是
| A.已知甲烷的燃烧热为890.3 kJ‧mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ‧mol-1 |
| B.已知强酸和强碱的稀溶液反应的中和热为57.3 kJ‧mol-1,则CH3COOH+OH—=CH3COO—+H2O ΔH=-57.3 kJ‧mol-1 |
C.一定条件下,将0.5mol N2和1.5mol H2置于密闭容器中,充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-38.6 kJ‧mol-1 2NH3(g) ΔH=-38.6 kJ‧mol-1 |
| D.已知1g N2H4(l)和足量H2O2(l)反应生成氮气和水蒸气,放出热量20.05kJ,该热化学方程式可表示为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ΔH=-641.6 kJ‧mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.由C(石墨) = C(金刚石) △H=+1.9 kJ·mol-1可知,金刚石比石墨稳定 |
| B.在一定条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| C.已知2C(s) + O2(g) = 2CO(g) △H=-221 kJ·mol-1,可知C的标准燃烧热为110.5 kJ·mol-1 |
| D.在一密闭容器中,9.6 g的硫粉与11.2 g的铁粉混合加热,充分反应,生成硫化亚铁17.6 g,放出19.12 kJ的热量,则Fe(s) + S(s) = FeS(s) △H= - 95.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程发生下列反应:
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-58.6kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ·mol-1
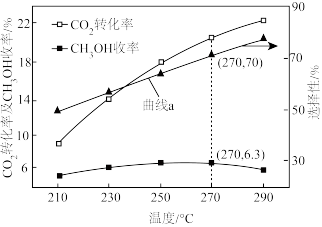
0.5MPa下,将n(H2):n(CO2)=3的混合气体以一定流速通过装有催化剂的反应器,测得CO2的转化率、CH3OH或CO的选择性[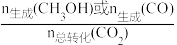 ×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-58.6kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ·mol-1
0.5MPa下,将n(H2):n(CO2)=3的混合气体以一定流速通过装有催化剂的反应器,测得CO2的转化率、CH3OH或CO的选择性[
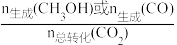 ×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
| A.CO(g)+2H2(g)=CH3OH(g) △H=99.8kJ·mol-1 |
| B.曲线a表示CH3OH的选择性随温度的变化 |
| C.图中所示270℃时,对应CO2的转化率为21% |
| D.在210℃~250℃之间,CH3OH的收率增大是由于CH3OH的选择性增大导致 |
您最近一年使用:0次
【推荐2】CO与N2O气体均会造成环境污染,研究表明二者可在Pt2O+表面转化为无害气体N2和CO2,其反应过程中的能量变化如图所示。下列说法错误的是
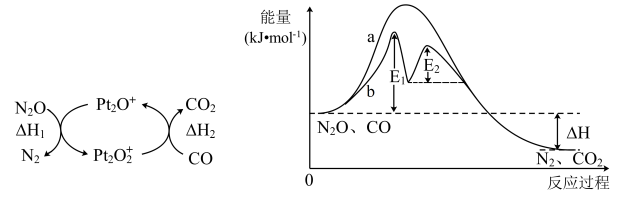

| A.使用催化剂可改变反应历程,降低反应活化能 |
| B.有催化剂条件下,E1时的反应速率比E2慢 |
| C.N2O(g)+CO(g)=N2(g)+CO2(g) △H=△H1+△H2 |
D.Pt2O+是反应的中间体,Pt2O 是反应的催化剂 是反应的催化剂 |
您最近一年使用:0次



