对于数以千万计的化学物质和为数众多的化学反应,分类法几乎是无可代替的。
I.现有以下物质:① ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ (酒精)⑥
(酒精)⑥ ⑦稀硫酸
⑦稀硫酸
(1)以上物质中属于混合物的是__________ (填序号,下同)。
(2)属于电解质的是__________ ,属于非电解质的是__________
II.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是__________ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)__________ 。
(5)向 溶液中加入少量的
溶液中加入少量的 ,对应的离子方程式为
,对应的离子方程式为___________ 。
I.现有以下物质:①
 ②Cu③
②Cu③ ④
④ 胶体⑤
胶体⑤ (酒精)⑥
(酒精)⑥ ⑦稀硫酸
⑦稀硫酸(1)以上物质中属于混合物的是
(2)属于电解质的是
II.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)(5)向
 溶液中加入少量的
溶液中加入少量的 ,对应的离子方程式为
,对应的离子方程式为
更新时间:2021-10-19 20:23:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氢氧化钙,俗称熟石灰或消石灰,是一种白色粉末状固体。氢氧化钙是重要的建筑材料。农药中的波尔多液正是利用石灰乳(溶于水的氢氧化钙)和硫酸铜水溶液按照一定的比例配制而成的。冬天,树木过冬防虫,树木根部以上涂80 cm的石灰浆。
工业上常用下列方法制备氢氧化钙。具体过程为:将石灰石煅烧成氧化钙后,经精选与水按1∶(3~3.5)的比例混合,生成氢氧化钙料液经净化分离除渣,再经离心脱水,干燥,即为氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
(2)写出生成波尔多液的化学反应方程式,并注明反应类型:__________ 。
(3)写出工业制备氢氧化钙的化学方程式,并注明物质类别的转化关系。示例如下:
A(氧化物)+B(氧化物)→C(盐)___________ 。
(4)请写出与题目不相同的制备氢氧化钙的方法,并说明工业生产方法的优点:___________ 。
工业上常用下列方法制备氢氧化钙。具体过程为:将石灰石煅烧成氧化钙后,经精选与水按1∶(3~3.5)的比例混合,生成氢氧化钙料液经净化分离除渣,再经离心脱水,干燥,即为氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
| 类别 | 混合物 | 碱 | 氧化物 |
| 名称 | |||
| 化学式 | 无 |
(3)写出工业制备氢氧化钙的化学方程式,并注明物质类别的转化关系。示例如下:
A(氧化物)+B(氧化物)→C(盐)
(4)请写出与题目不相同的制备氢氧化钙的方法,并说明工业生产方法的优点:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列一组反应:
①CO2+C 2CO
2CO
②Cu2(OH)2CO3 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2 2CO2
2CO2
⑤3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
⑥CuO+CO Cu+CO2
Cu+CO2
⑦4NH3+3O2 2N2+6H2O
2N2+6H2O
⑧2H2O 2H2↑+O2↑
2H2↑+O2↑
⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
⑩CO2+H2O=H2CO3
(1)其中属于化合反应的有________ (填序号,下同),属于置换反应的有________ 。
(2)在化学反应前后元素的化合价没有变化的是________ 。
(3)上述反应中,既是分解反应,又是氧化还原反应的是________ 。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是________ 。
(5)根据你的理解,氧化还原反应的实质是 (填字母)。
Ⅱ.饮用水中的NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
请回答下列问题:
(6)上述反应中,________ 元素的化合价升高,则该元素的原子________ (填“得到”或“失去”)电子;而________ 元素的化合价降低,该元素发生________ 反应。
(7)用双线桥法表示反应中电子转移的方向和数目:_____________ 。
①CO2+C
 2CO
2CO②Cu2(OH)2CO3
 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2
 2CO2
2CO2⑤3Fe+4H2O(g)
 Fe3O4+4H2
Fe3O4+4H2⑥CuO+CO
 Cu+CO2
Cu+CO2⑦4NH3+3O2
 2N2+6H2O
2N2+6H2O⑧2H2O
 2H2↑+O2↑
2H2↑+O2↑⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
⑩CO2+H2O=H2CO3
(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有变化的是
(3)上述反应中,既是分解反应,又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是 (填字母)。
| A.分子中的原子重新组合 |
| B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 |
| D.化合价的改变 |
Ⅱ.饮用水中的NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。请回答下列问题:
(6)上述反应中,
(7)用双线桥法表示反应中电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某学习小组以氢氧化钡、水、硫酸为实验对象探究离子反应发生的条件。
(1)氢氧化钡与硫酸在溶液中能发生___________ (填字母)。
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加水后,灯泡变亮的原因是氢氧化钡发生了___________ 。
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因___________ 。
(4)实验2:用硫酸钠溶液替代稀硫酸,重复实验进行对照。加入硫酸钠溶液过程中灯泡不熄灭,原因是___________
| 实验1:向烧杯中依次加入下列试剂,记录灯泡变化 | |
 | ①氢氧化钡粉末:灯泡不亮 ②加入蒸馏水:灯泡变亮 ③逐滴滴加硫酸,灯泡变化如下:亮  暗(溶液1) 暗(溶液1) 熄灭(溶液2) 熄灭(溶液2) 亮(溶液3) 亮(溶液3) |
(1)氢氧化钡与硫酸在溶液中能发生
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加水后,灯泡变亮的原因是氢氧化钡发生了
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因
(4)实验2:用硫酸钠溶液替代稀硫酸,重复实验进行对照。加入硫酸钠溶液过程中灯泡不熄灭,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体:⑥铝;⑦CO2;⑧CH3COOH;⑨蔗糖晶体
请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出④的电离方程式_______
(3)写出①和⑥反应的化学方程式_______
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式_______ 。
(5)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,即制得Fe(OH)3胶体。写出该反应的化学方程式_______ 。
(6)下列叙述错误的是_______(填标号)。
请回答下列问题:
(1)以上物质中属于混合物的是
(2)写出④的电离方程式
(3)写出①和⑥反应的化学方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式
(5)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,即制得Fe(OH)3胶体。写出该反应的化学方程式
(6)下列叙述错误的是_______(填标号)。
| A.雾属于胶体,能产生丁达尔效应 |
| B.用盐卤点豆腐与胶体性质有关 |
| C.无法从颜色上区别FeCl3溶液和Fe(OH)3胶体 |
| D.工业静电除尘装置是根据胶体的性质设计的 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
Ⅰ.纳米磁珠(纳米 )颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
)颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
【查阅资料】
 为黑色固体,硬度较大,有磁性,不溶于
为黑色固体,硬度较大,有磁性,不溶于 、碱和
、碱和 ,纳米
,纳米 在潮湿的
在潮湿的 中容易被
中容易被 氧化,高温下被
氧化,高温下被 氧化成
氧化成 ,溶于
,溶于 的溶液中,生成
的溶液中,生成 和
和 。向含有一定配比的
。向含有一定配比的 和
和 的混合盐溶液中,加入过量的碱性物质,如
的混合盐溶液中,加入过量的碱性物质,如 、
、 ,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米
,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米 颗粒。
颗粒。
(1)①~⑩,能导电的是_______ (填编号,后同),属于非电解质的是___________ 。
(2)将⑥气体通入⑩,写出发生反应的离子方程式:___________ 。
Ⅱ.空气与我们的生存息息相关。 是主要的温室气体,
是主要的温室气体, 是主要的大气污染物之一。
是主要的大气污染物之一。
(3)写出 与NaOH反应的离子方程式
与NaOH反应的离子方程式___________ 。
(4) 、
、 均属于酸性氧化物,类比
均属于酸性氧化物,类比 下列物质中可以与
下列物质中可以与 发生反应的是_______。
发生反应的是_______。
(5)双碱法脱硫过程如下图所示。
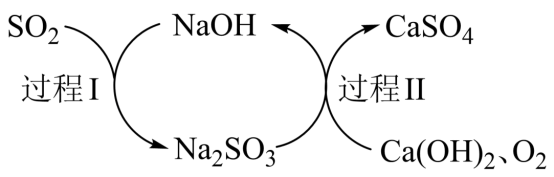
①下列反应中,不能用同一离子方程式表示的是_______ (填序号)。
A. 溶液和稀
溶液和稀 B.NaOH和稀
B.NaOH和稀
C. 溶液与稀
溶液与稀 D.NaOH和稀盐酸
D.NaOH和稀盐酸
②类比 与碱反应,过程Ⅰ的离子方程式是
与碱反应,过程Ⅰ的离子方程式是_______ 。
③双碱法脱硫过程中,循环利用的物质是_______ (填化学式)。
Ⅰ.纳米磁珠(纳米
 )颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。
)颗粒中含有人体代谢生长必需的微量元素铁,不含其他有毒的金属元素,可以用于对比增强磁共振成像、免疫检测、组织修复、药物运输和细胞分离等方面。【查阅资料】
 为黑色固体,硬度较大,有磁性,不溶于
为黑色固体,硬度较大,有磁性,不溶于 、碱和
、碱和 ,纳米
,纳米 在潮湿的
在潮湿的 中容易被
中容易被 氧化,高温下被
氧化,高温下被 氧化成
氧化成 ,溶于
,溶于 的溶液中,生成
的溶液中,生成 和
和 。向含有一定配比的
。向含有一定配比的 和
和 的混合盐溶液中,加入过量的碱性物质,如
的混合盐溶液中,加入过量的碱性物质,如 、
、 ,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米
,使其达到某个pH范围,在适当的温度和高速搅拌下发生反应合成纳米 颗粒。
颗粒。(1)①~⑩,能导电的是
(2)将⑥气体通入⑩,写出发生反应的离子方程式:
Ⅱ.空气与我们的生存息息相关。
 是主要的温室气体,
是主要的温室气体, 是主要的大气污染物之一。
是主要的大气污染物之一。(3)写出
 与NaOH反应的离子方程式
与NaOH反应的离子方程式(4)
 、
、 均属于酸性氧化物,类比
均属于酸性氧化物,类比 下列物质中可以与
下列物质中可以与 发生反应的是_______。
发生反应的是_______。A. | B.NaCl | C.HCl | D. |

①下列反应中,不能用同一离子方程式表示的是
A.
 溶液和稀
溶液和稀 B.NaOH和稀
B.NaOH和稀
C.
 溶液与稀
溶液与稀 D.NaOH和稀盐酸
D.NaOH和稀盐酸②类比
 与碱反应,过程Ⅰ的离子方程式是
与碱反应,过程Ⅰ的离子方程式是③双碱法脱硫过程中,循环利用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)现有下列物质:①碘酒 ②AgCl ③液氯 ④液态氯化氢 ⑤ ⑥澄清石灰水 ⑦铜 ⑧氨水 ⑨蔗糖 ⑩
⑥澄清石灰水 ⑦铜 ⑧氨水 ⑨蔗糖 ⑩ 。请将序号分别填入下面的横线处:
。请将序号分别填入下面的横线处:
上述状态下可导电的是_______ ,属于电解质的是_______ ,属于非电解质的是_______ 。
(2)在9.5g某二价金属的氯化物中含有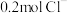 ,该金属元素的相对原子质量为
,该金属元素的相对原子质量为_______ 。
(3)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是_______ (设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(4)在标准状况下,2.24L由 组成的混合气体中含有的氮元素的质量约为
组成的混合气体中含有的氮元素的质量约为_______ 。
(5)在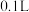 由
由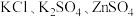 形成的植物营养液中,
形成的植物营养液中,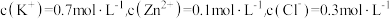 ,向混合溶液中滴加足量的
,向混合溶液中滴加足量的 溶液后产生沉淀的物质的量为
溶液后产生沉淀的物质的量为_______ 。
(1)现有下列物质:①碘酒 ②AgCl ③液氯 ④液态氯化氢 ⑤
 ⑥澄清石灰水 ⑦铜 ⑧氨水 ⑨蔗糖 ⑩
⑥澄清石灰水 ⑦铜 ⑧氨水 ⑨蔗糖 ⑩ 。请将序号分别填入下面的横线处:
。请将序号分别填入下面的横线处:上述状态下可导电的是
(2)在9.5g某二价金属的氯化物中含有
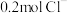 ,该金属元素的相对原子质量为
,该金属元素的相对原子质量为(3)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(4)在标准状况下,2.24L由
 组成的混合气体中含有的氮元素的质量约为
组成的混合气体中含有的氮元素的质量约为(5)在
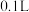 由
由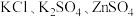 形成的植物营养液中,
形成的植物营养液中,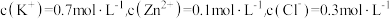 ,向混合溶液中滴加足量的
,向混合溶液中滴加足量的 溶液后产生沉淀的物质的量为
溶液后产生沉淀的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_______ (填序号)。
a.单质 b.氧化物 c.电解质 d.盐 e.化合物
Ⅱ.有一瓶无色溶液只含 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:
①原溶液中加足量 溶液产生白色沉淀;
溶液产生白色沉淀;
②原溶液中加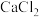 溶液不产生沉淀;
溶液不产生沉淀;
③原溶液中加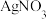 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
(2)原溶液中一定含有的离子是_______ ,一定不含有的离子是_______ ,可能含有的离子是_______ 。
(3)实验③说明原溶液中含有_______ 。有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_______ ,理由是_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在有
a.单质 b.氧化物 c.电解质 d.盐 e.化合物
Ⅱ.有一瓶无色溶液只含
 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:①原溶液中加足量
 溶液产生白色沉淀;
溶液产生白色沉淀;②原溶液中加
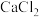 溶液不产生沉淀;
溶液不产生沉淀;③原溶液中加
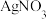 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。(2)原溶液中一定含有的离子是
(3)实验③说明原溶液中含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】
(1)+6价铬的化合物毒性较大,常用NaHSO3将废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为__________________________________________________________ 。
(2)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____________________________________ 。
(3)“酸浸”时V2O5转化为 ,反应的离子方程式为
,反应的离子方程式为________________________________________ 。
(4)在H2SO4的酸性环境中ClO2与碘化钾反应的离子方程式___________________________ 。
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________________________ 。
(1)+6价铬的化合物毒性较大,常用NaHSO3将废液中的
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为(2)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(3)“酸浸”时V2O5转化为
 ,反应的离子方程式为
,反应的离子方程式为(4)在H2SO4的酸性环境中ClO2与碘化钾反应的离子方程式
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:_______ 。
②有难溶性碱生成的离子反应方程式:_______ 。
(3)某兴趣小组的同学向一定体积的 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。

Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 、
、 、
、 、
、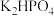 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。
(4) 属于
属于_______ 酸; 为
为_______ 盐(填序号)
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
| A.单质 | B.化合物 | C.水 | D.电解质 |
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:
②有难溶性碱生成的离子反应方程式:
(3)某兴趣小组的同学向一定体积的
 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
| A.XY段混合溶液的导电能力逐渐减弱,说明生成的白色沉淀BaSO,不是电解质 |
| B.a时刻,两溶液恰好完全反应 |
C.YZ段的导电能力不断增大,主要是由于 溶液电离出的离子导电 溶液电离出的离子导电 |
D.向一定体积的 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 |
Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
 、
、 、
、 、
、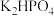 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。(4)
 属于
属于 为
为①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出
 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按要求写出对应的方程式
(1)NaHSO4在熔融状态下的电离方程式为:___________
(2)制备Fe(OH)3胶体的化学方程式___________
(3)碳酸氢钙与过量氢氧化钠溶液反应的离子方程式___________
(4)除去Na2CO3固体中的NaHCO3的化学方程式:___________
(5)除去NaHCO3溶液中的Na2CO3的离子方程式:___________
(1)NaHSO4在熔融状态下的电离方程式为:
(2)制备Fe(OH)3胶体的化学方程式
(3)碳酸氢钙与过量氢氧化钠溶液反应的离子方程式
(4)除去Na2CO3固体中的NaHCO3的化学方程式:
(5)除去NaHCO3溶液中的Na2CO3的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
您最近一年使用:0次




