回答下列问题
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度___________ mol/L。
(2)标准状况下,33.6L的NH3所具有的物质的量为___________ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L,在Cl2+2NaOH=NaCl+NaClO+H2O的反应中,写出反应的离子方程式___________ 。氧化产物是___________ ,还原产物是___________ ;氧化剂与还原剂的物质的量的比是___________ 。
(3)用双线桥表示出电子转移的方向和数目___________ 。
Cl2+2NaOH=NaCl+NaClO+H2O
(1)1mol/L的CaCl2溶液0.5L,Cl-离子的物质的量浓度
(2)标准状况下,33.6L的NH3所具有的物质的量为
(3)用双线桥表示出电子转移的方向和数目
Cl2+2NaOH=NaCl+NaClO+H2O
更新时间:2023-01-19 13:17:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)日常使用的金属材料,大多数属于合金。合金有许多优良的物理、化学或机械性能。生活中比较常见的合金有___________ (填写一类即可,下同)。近年来,为满足某些尖端技术发展的需要,人们有设计和合成了许多新型合金,例如:___________ 。
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式: )的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
)的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:

①葡萄糖的摩尔质量为___________ 。
②该注射液中葡萄糖的物质的量浓度为___________ (保留两位小数)
(3)某饮用矿泉水中,测得含有 、
、 、
、 、
、 和
和 五种主要离子(不考虑溶液中少量的
五种主要离子(不考虑溶液中少量的 和
和 或其他离子),其中
或其他离子),其中 :
: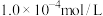 ,
, :
: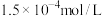 ,
, :
: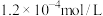 ,
, :
: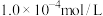 ,则溶液中
,则溶液中 的物质的量浓度是
的物质的量浓度是______  。
。
(4)水是万物之源,为探究高铁酸钾(化学式为: )在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
)在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:___________ 。
(1)日常使用的金属材料,大多数属于合金。合金有许多优良的物理、化学或机械性能。生活中比较常见的合金有
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式:
 )的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
)的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
①葡萄糖的摩尔质量为
②该注射液中葡萄糖的物质的量浓度为
(3)某饮用矿泉水中,测得含有
 、
、 、
、 、
、 和
和 五种主要离子(不考虑溶液中少量的
五种主要离子(不考虑溶液中少量的 和
和 或其他离子),其中
或其他离子),其中 :
: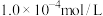 ,
, :
: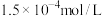 ,
, :
: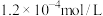 ,
, :
: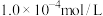 ,则溶液中
,则溶液中 的物质的量浓度是
的物质的量浓度是 。
。(4)水是万物之源,为探究高铁酸钾(化学式为:
 )在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
)在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)在标准状况下,1.7 g氨气所占的体积为___________ L,它与标准状况下___________ L硫化氢含有相同数目的氢原子。
(2)某气态氧化物的化学式为 ,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为___________ g/mol,相对原子质量为___________ 。
(3)1 L 0.5 mol/L的 溶液中,
溶液中,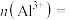
___________ ,
___________ ,
___________ 。
(1)在标准状况下,1.7 g氨气所占的体积为
(2)某气态氧化物的化学式为
 ,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为(3)1 L 0.5 mol/L的
 溶液中,
溶液中,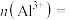


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)在标准状况下,测得 某气体的体积为
某气体的体积为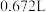 ,该气体的摩尔质量为
,该气体的摩尔质量为_______ 。
(2)将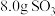 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为_______ 。
(3) 溶液和
溶液和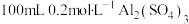 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4)设 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是_______ (用含 的式子表示)
的式子表示)
(5)标准状况下,将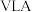 气体(摩尔质量为
气体(摩尔质量为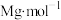 )全部溶于
)全部溶于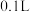 水(水的密度为
水(水的密度为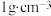 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为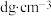 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(6)某盐混合溶液中含有离子: ,测得
,测得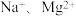 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: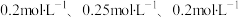 ,则
,则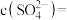
_______ 。
(1)在标准状况下,测得
 某气体的体积为
某气体的体积为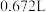 ,该气体的摩尔质量为
,该气体的摩尔质量为(2)将
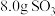 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为(3)
 溶液和
溶液和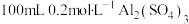 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(4)设
 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是 的式子表示)
的式子表示)(5)标准状况下,将
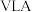 气体(摩尔质量为
气体(摩尔质量为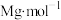 )全部溶于
)全部溶于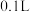 水(水的密度为
水(水的密度为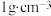 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为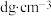 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(6)某盐混合溶液中含有离子:
 ,测得
,测得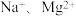 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: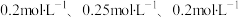 ,则
,则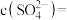
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请按要求书写下列离子方程式:
(1)利用FeCl3溶液制备胶体的离子方程式为_______ ;
(2)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:_______ ;
(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:_______ ;
(4)Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为_______ ;
(5)向NaClO溶液中通入少量的CO2离子方程式为_______ ;
(6)FeBr2溶液中通入等物质的量的Cl2气体,离子方程式为:_______ 。
(1)利用FeCl3溶液制备胶体的离子方程式为
(2)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:
(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:
(4)Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为
(5)向NaClO溶液中通入少量的CO2离子方程式为
(6)FeBr2溶液中通入等物质的量的Cl2气体,离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

(1)两种物质都是电解质的是_______ (填分类标准代号)。
(2)分类标准代号A表示_______
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:_______ 。

(1)两种物质都是电解质的是
(2)分类标准代号A表示
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:
您最近一年使用:0次
【推荐3】氢氧化钠是白色固体,易潮解,具有强腐蚀性,所以又叫火碱、烧碱、苛性钠。是常用的碱性干燥剂,是重要的化工原料。
工业制法:氯碱工业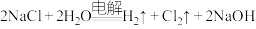
苛化法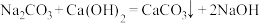
在实验室,钠、氧化钠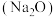 、过氧化钠
、过氧化钠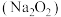 分别与水反应都生成
分别与水反应都生成
回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是_______ (填“升高”、“降低”、“不变”)。
(2) 可拆写,苛化法反应前后
可拆写,苛化法反应前后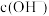
___________ (填“变大”、“变小”、“不变”)。
(3)写出 与水反应的化学方程式
与水反应的化学方程式___________ 。
(4)补项:过氧化钠与水反应为: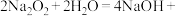
___________ ↑。
(5) 固体不能干燥酸性气体。能用
固体不能干燥酸性气体。能用 固体干燥的气体是
固体干燥的气体是___________ (填序号)。
a. b.
b. c.
c. (碱性气体) d.
(碱性气体) d.
(6)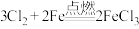 ,氯化铁能催化双氧水分解
,氯化铁能催化双氧水分解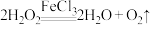 其反应机理为:①
其反应机理为:① ;②
;② 。在反应①中,
。在反应①中, 是还原剂,在反应②中,
是还原剂,在反应②中, 是
是___________ 剂(填“氧化”或“还原”)。
工业制法:氯碱工业
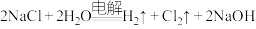
苛化法
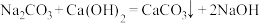
在实验室,钠、氧化钠
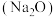 、过氧化钠
、过氧化钠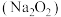 分别与水反应都生成
分别与水反应都生成
回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是
(2)
 可拆写,苛化法反应前后
可拆写,苛化法反应前后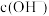
(3)写出
 与水反应的化学方程式
与水反应的化学方程式(4)补项:过氧化钠与水反应为:
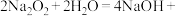
(5)
 固体不能干燥酸性气体。能用
固体不能干燥酸性气体。能用 固体干燥的气体是
固体干燥的气体是a.
 b.
b. c.
c. (碱性气体) d.
(碱性气体) d.
(6)
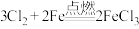 ,氯化铁能催化双氧水分解
,氯化铁能催化双氧水分解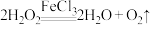 其反应机理为:①
其反应机理为:① ;②
;② 。在反应①中,
。在反应①中, 是还原剂,在反应②中,
是还原剂,在反应②中, 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+2FeCl3=CuCl2+2FeCl2。
(1)请在上式中标出电子转移的方向和数目:________ 。
(2)上述反应中被氧化的元素是___________ 。
(3)写出FeCl3的电离方程式:___________ 。
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是______(填序号)。
(5)若要由反应后的废液回收金属铜和得到较纯净的FeCl2溶液,你选择加入的物质是_______ 。
(1)请在上式中标出电子转移的方向和数目:
(2)上述反应中被氧化的元素是
(3)写出FeCl3的电离方程式:
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是______(填序号)。
| A.氯气 | B.铁 | C.双氧水 | D.稀硫酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
____ ____
____ ____
____ ___
___ ____
____ _____KOH,配平反应方程式,并
_____KOH,配平反应方程式,并标出电子转移的方向和数目 _______ 。
____
 ____
____ ____
____ ___
___ ____
____ _____KOH,配平反应方程式,并
_____KOH,配平反应方程式,并
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______ (填字母)。
(2)下列反应中,HCl作还原剂的是_______ ,HCl作氧化剂的是_______ ,HCl为还原产物的是_______ 。
①KOH+HCl=KCl+H2O
②K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
③Cl2+H2O=HCl+HClO
④2NaCl+H2SO4(浓) Na2SO4+2HCl↑
Na2SO4+2HCl↑
⑤Fe+2HCl=FeCl2+H2↑
(3)用双线桥法表明反应②中电子转移的方向和数目_______ 。
(4)若把钠放在石棉网上加热可观察到_______ ,反应的化学方程式为_______ ,其中还原剂为_______ 。若把1.15g钠放在足量的氯气中燃烧,生成氯化钠的质量是_______ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
 |  |  |  |
| A.简单机械织布 | B.我国古代烧制陶器 | C.煤的形成 | D.卫星上的太阳能电池工作 |
(2)下列反应中,HCl作还原剂的是
①KOH+HCl=KCl+H2O
②K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
③Cl2+H2O=HCl+HClO
④2NaCl+H2SO4(浓)
 Na2SO4+2HCl↑
Na2SO4+2HCl↑⑤Fe+2HCl=FeCl2+H2↑
(3)用双线桥法表明反应②中电子转移的方向和数目
(4)若把钠放在石棉网上加热可观察到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】“84消毒液”是一种以NaClO为有效成分的高效消毒剂,在新冠肺炎防治中被广泛用于宾馆、旅游、医院、家庭等的卫生消毒。
Ⅰ.如表为“84”消毒液说明书,请回答下列问题。
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式___ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___ ,从氧化还原角度分析Cl2表现了___ 性。
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是___ (用离子方程式表达)。(已知:酸性:H2CO3>HClO>HCO ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是___ 。
Ⅱ.某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
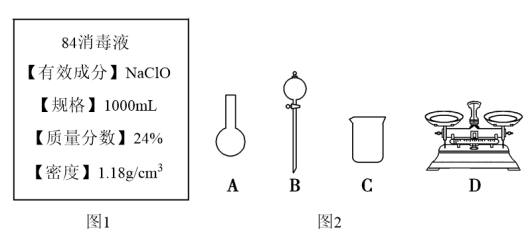
(3)此“84消毒液”的物质的量浓度约为___ mol·L-1。(计算结果保留一位小数)
(4)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL该消毒液。
①如图2所示的仪器中配制溶液需要使用的是___ 。(填仪器序号),还缺少的玻璃仪器是___ 。
②请计算该同学配制此溶液需用托盘天平称量NaClO固体的质量为___ g。
(5)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是___ (填字号)。
Ⅰ.如表为“84”消毒液说明书,请回答下列问题。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1:200水溶液餐饮具,瓜果等1:100水溶液 |
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
 ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是Ⅱ.某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(3)此“84消毒液”的物质的量浓度约为
(4)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL该消毒液。
①如图2所示的仪器中配制溶液需要使用的是
②请计算该同学配制此溶液需用托盘天平称量NaClO固体的质量为
(5)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是
| A.定容时俯视制度线 | B.转移前,容量瓶内有蒸馏水 |
| C.未冷至室温就转移定容 | D.定容时水多用胶头滴管吸出 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断下列实验操作是否正确。
1.保存硫酸亚铁溶液需加入铁钉和少量硫酸。(_______)
2.金属钠保存在装有煤油的玻璃塞广口瓶中。(_______)
3.溴化银固体保存在棕色玻璃塞广口瓶中。(_______)
4.保存浓硝酸需用带橡胶塞的棕色细口瓶。(_______)
5.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中。(_______)
6.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中。(_______)
7.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
8.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
9.取用少量白磷时,应在水中切割白磷,剩余的白磷立即放回原试剂瓶中。(_______)
10.做完铜与浓硫酸反应实验后的试管,立即用大量水冲洗。(_______)
11.取用一小块钠后,剩余的钠放到垃圾桶里。(_______)
12.燃着的酒精灯被打翻,引起失火,应立即用水浇灭。(_______)
13.少量浓硫酸沾在皮肤上,应立即用氢氧化钠溶液冲洗。(_______)
14.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜。(_______)
15.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理。(_______)
16.有大量的氯气泄漏时,应用肥皂水浸湿的软布捂住鼻孔,并迅速离开现场。(_______)
17.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液。(_______)
18.用 方法点燃酒精灯。(_______)
方法点燃酒精灯。(_______)
19.用 配制硫酸溶液。(_______)
配制硫酸溶液。(_______)
20.用 制备氢气并检验H2的可燃性。(_______)
制备氢气并检验H2的可燃性。(_______)
1.保存硫酸亚铁溶液需加入铁钉和少量硫酸。(_______)
2.金属钠保存在装有煤油的玻璃塞广口瓶中。(_______)
3.溴化银固体保存在棕色玻璃塞广口瓶中。(_______)
4.保存浓硝酸需用带橡胶塞的棕色细口瓶。(_______)
5.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中。(_______)
6.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中。(_______)
7.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
8.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中。(_______)
9.取用少量白磷时,应在水中切割白磷,剩余的白磷立即放回原试剂瓶中。(_______)
10.做完铜与浓硫酸反应实验后的试管,立即用大量水冲洗。(_______)
11.取用一小块钠后,剩余的钠放到垃圾桶里。(_______)
12.燃着的酒精灯被打翻,引起失火,应立即用水浇灭。(_______)
13.少量浓硫酸沾在皮肤上,应立即用氢氧化钠溶液冲洗。(_______)
14.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜。(_______)
15.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理。(_______)
16.有大量的氯气泄漏时,应用肥皂水浸湿的软布捂住鼻孔,并迅速离开现场。(_______)
17.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液。(_______)
18.用
 方法点燃酒精灯。(_______)
方法点燃酒精灯。(_______)19.用
 配制硫酸溶液。(_______)
配制硫酸溶液。(_______)20.用
 制备氢气并检验H2的可燃性。(_______)
制备氢气并检验H2的可燃性。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。
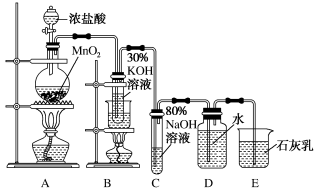
制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:___ 。

制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:
您最近一年使用:0次



