实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。
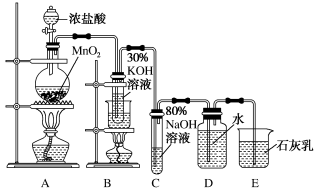
制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:___ 。

制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:
2021高三·全国·专题练习 查看更多[1]
(已下线)专题04 陌生反应方程式-【微专题·大素养】备战2022年高考化学讲透提分要点
更新时间:2021-11-16 08:04:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某化学实验兴趣小组,进行铁及其化合物有关的实验。
实验一:铁及其化合物性质实验
该小组学生将表面生锈的铁片放在稀硫酸中,刚开始观察到无气泡产生,溶液变为黄色,一会儿后才观察到有气泡产生。
(1)刚开始无气泡产生,溶液变为黄色的原因为___ (用离子方程式解释)。
(2)产生气泡的离子方程式为___ ,反应前后铁元素化合价___ (选填“升高”或“降低”),发生___ (选填“氧化”或“还原”)反应。
实验二:Fe(OH)3胶体制备
向煮沸的蒸馏水中滴加几滴饱和氯化铁溶液,继续加热煮沸至溶液呈红褐色时,停止加热,即可制得Fe(OH)3胶体。
(3)证明Fe(OH)3胶体制备成功的方法是___ 。
(4)写出制备Fe(OH)3胶体的化学反应方程式___ 。
(5)向制得的Fe(OH)3胶体中逐滴加入稀硫酸,可观察到先产生红褐色沉淀,然后红褐色沉淀消失,溶液变为黄色。产生红褐色沉淀的原因是___ ,红褐色沉淀消失的原因是___ (用离子方程式表示)。
实验一:铁及其化合物性质实验
该小组学生将表面生锈的铁片放在稀硫酸中,刚开始观察到无气泡产生,溶液变为黄色,一会儿后才观察到有气泡产生。
(1)刚开始无气泡产生,溶液变为黄色的原因为
(2)产生气泡的离子方程式为
实验二:Fe(OH)3胶体制备
向煮沸的蒸馏水中滴加几滴饱和氯化铁溶液,继续加热煮沸至溶液呈红褐色时,停止加热,即可制得Fe(OH)3胶体。
(3)证明Fe(OH)3胶体制备成功的方法是
(4)写出制备Fe(OH)3胶体的化学反应方程式
(5)向制得的Fe(OH)3胶体中逐滴加入稀硫酸,可观察到先产生红褐色沉淀,然后红褐色沉淀消失,溶液变为黄色。产生红褐色沉淀的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的类别和元素价态是学习和研究元素化合物性质和转化的重要认识视角,利用价、类之间的关系,可以寻求物质转化的途径。下图是中学常见的含N元素物质的部分转化关系图,请回答下列问题:

(1)图中X的摩尔质量是___________ ,根据N元素的化合价分析,X在氧化还原反应中表现出的性质是___________ 。
(2)工业上处理氮氧化物时,可用浓硝酸将NO氧化为NO2,有关反应的化学方程式为___________ ;再利用NO2CO3溶液吸收NO2,并通入空气使之全部转化为NaNO3,有关反应的离子方程式为___________ 。
(3)SCR选择性催化还原技术可有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如下图所示:
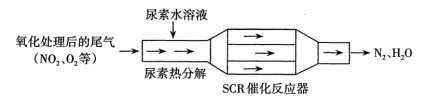
①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式___________ 。
②尿素溶液的浓度会影响NO2的转化,测定溶液中尿素浓度的方法如下:取ag尿素溶液,将所含氮元素完全转化为NH3,所得NH3用过量的V1mL、c1mol H2SO4溶液完全吸收,剩余H2SO4用V2mL、c2mol·L-1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数___________ 。(列出计算表达式即可)

(1)图中X的摩尔质量是
(2)工业上处理氮氧化物时,可用浓硝酸将NO氧化为NO2,有关反应的化学方程式为
(3)SCR选择性催化还原技术可有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如下图所示:

①已知尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出SCR催化反应器中NH3还原NO2的化学方程式
②尿素溶液的浓度会影响NO2的转化,测定溶液中尿素浓度的方法如下:取ag尿素溶液,将所含氮元素完全转化为NH3,所得NH3用过量的V1mL、c1mol H2SO4溶液完全吸收,剩余H2SO4用V2mL、c2mol·L-1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F六种元素(前20号元素)的核电荷数依次增大。C是地壳中含量最高的元素;D的最高价氧化物的水化物分别能与E、F的最高价氧化物的水化物反应;E原子的最外层电子数是其最内层电子数的3倍;F元素是化学肥料中一种重要元素,其原子的次外层电子数与倒数第三层的电子数相等;A与F具有相同的最外层电子数;B元素的某种单质常作为干电池中的电极材料。试回答下列问题:
(1)由A、B两元素按原子个数之比为1︰1组成的某分子,其相对分子质量小于30,请写出实验室制备该物质的化学反应方程式_____________________________________________ 。
(2)D、E、F三种元素的原子半径由大到小顺序是___________________ (用元素符号表示)。
(3)由C、D、E、F四种元素组成的某盐,可用作净水剂,也可用于制作膨化食品。该盐的化为_____ ,将该盐溶液与Ba(OH)2溶液按溶质物质的量之比1:2混合反应,此反应的离子方程式为_________________ 。
(1)由A、B两元素按原子个数之比为1︰1组成的某分子,其相对分子质量小于30,请写出实验室制备该物质的化学反应方程式
(2)D、E、F三种元素的原子半径由大到小顺序是
(3)由C、D、E、F四种元素组成的某盐,可用作净水剂,也可用于制作膨化食品。该盐的化为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: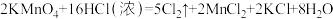 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
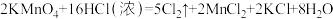 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气有广泛的用途,回答下列问题:
(1)氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移的方向和数目:TiO2+2C+2Cl2 TiCl4+2CO。
TiCl4+2CO。___
(2)反应8NH3+3Cl2=N2+6NH4Cl可用于氯气管道的检漏,在该反应中,N2为__ 产物(填“氧化”或“还原”)
(3)氯气可与NaOH溶液反应制备“84”消毒液,在2020年初抗击新冠病毒感染的肺炎(Covid-19)疫情中,“84”消毒液发挥了重要的作用。但若将“84”消毒液与洗厕剂洁厕灵混合使用,则会产生氯气,其反应的离子方程式是:__ 。
(4)氯气可与水反应,产生有漂白、杀菌作用的物质,反应的离子方程式为__ ;氯气可以用于制备漂白粉,漂白粉的有效成分是__ (填化学式)。
(5)实验室检验某溶液中是否含有Cl-的操作方法是:__ 。
(1)氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移的方向和数目:TiO2+2C+2Cl2
 TiCl4+2CO。
TiCl4+2CO。(2)反应8NH3+3Cl2=N2+6NH4Cl可用于氯气管道的检漏,在该反应中,N2为
(3)氯气可与NaOH溶液反应制备“84”消毒液,在2020年初抗击新冠病毒感染的肺炎(Covid-19)疫情中,“84”消毒液发挥了重要的作用。但若将“84”消毒液与洗厕剂洁厕灵混合使用,则会产生氯气,其反应的离子方程式是:
(4)氯气可与水反应,产生有漂白、杀菌作用的物质,反应的离子方程式为
(5)实验室检验某溶液中是否含有Cl-的操作方法是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式__ 。
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式__ 。
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式__ 。
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为__ ,制备漂白粉的离子方程式为__ 。
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为__ 。将反应后的产物溶于水配成饱和溶液,向溶液中加入一小块金属钠,反应的离子方程式为__ ,除了钠与水反应的现象其余可以观察到的现象是__ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学反应方程式
(2)小苏打是食品加工业应用最广泛的疏松剂,请写出碳酸氢钠与氢氧化钠的离子方程式
(3)舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一,请写出相应的离子方程式
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,漂白粉主要成分的化学式为
②将灼热的铜丝伸入盛有氯气的集气瓶中,反应现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】ClO2气体是一种高效、广谱、安全的杀菌消毒剂,可用NaClO3和草酸(H2C2O4)反应制得。已知:无水草酸100℃可以升华。在制备ClO2时实验需在60~100℃进行的原因是_____ ,控制所需温度的方法是______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】石棉尾矿主要含有 Mg3(Si2O5)(OH)4 和少量的 Fe2O3、Al2O3。以石棉尾矿为镁源制备碳酸镁晶须(MgCO3•nH2O)的工艺如下:
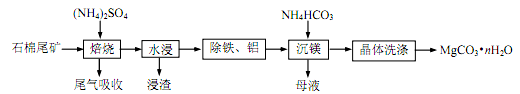
已知“焙烧”过程中的主反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。
(1)写出焙烧产物 NH3 的电子式___________ 。
(2)为提高水浸速率,可采取的措施为________________ (任写一条)。“浸渣”的主要成分为_________________ 。
(3)“除铁、铝”时,需将 pH 调至 8.0 左右,适宜作调节剂的是____ (填字母代号)。
a.NaOH b.Mg(OH)2 c.NH3•H2O
(4)“沉镁”过程中反应的离子方程式为______________ 。“沉镁”时若温度超过 60℃,将产生较多的碱式碳酸镁杂质,原因是_______ 。
(5)流程中可以循环利用的物质是______ (填化学式)。

(6)某小组同学称取 13.8 g MgCO3•nH2O 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则 n=________ 。

已知“焙烧”过程中的主反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4
 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。(1)写出焙烧产物 NH3 的电子式
(2)为提高水浸速率,可采取的措施为
(3)“除铁、铝”时,需将 pH 调至 8.0 左右,适宜作调节剂的是
a.NaOH b.Mg(OH)2 c.NH3•H2O
(4)“沉镁”过程中反应的离子方程式为
(5)流程中可以循环利用的物质是

(6)某小组同学称取 13.8 g MgCO3•nH2O 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则 n=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。
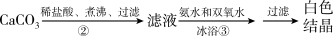
(1)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈______ 性(填“酸”“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作用是______ 。
(2)步骤③中反应的化学方程式为_____ ,该反应需要在冰浴下进行,原因是______ 。
(3)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_____ 。
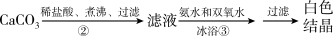
(1)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈
(2)步骤③中反应的化学方程式为
(3)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是
您最近一年使用:0次



