化学与人类生活密切相关。请按要求,回答下列问题:
(1)日常使用的金属材料,大多数属于合金。合金有许多优良的物理、化学或机械性能。生活中比较常见的合金有___________ (填写一类即可,下同)。近年来,为满足某些尖端技术发展的需要,人们有设计和合成了许多新型合金,例如:___________ 。
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式: )的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
)的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:

①葡萄糖的摩尔质量为___________ 。
②该注射液中葡萄糖的物质的量浓度为___________ (保留两位小数)
(3)某饮用矿泉水中,测得含有 、
、 、
、 、
、 和
和 五种主要离子(不考虑溶液中少量的
五种主要离子(不考虑溶液中少量的 和
和 或其他离子),其中
或其他离子),其中 :
: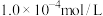 ,
, :
: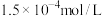 ,
, :
: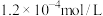 ,
, :
: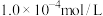 ,则溶液中
,则溶液中 的物质的量浓度是
的物质的量浓度是______  。
。
(4)水是万物之源,为探究高铁酸钾(化学式为: )在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
)在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:___________ 。
(1)日常使用的金属材料,大多数属于合金。合金有许多优良的物理、化学或机械性能。生活中比较常见的合金有
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式:
 )的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
)的水溶液,某同学获知其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
①葡萄糖的摩尔质量为
②该注射液中葡萄糖的物质的量浓度为
(3)某饮用矿泉水中,测得含有
 、
、 、
、 、
、 和
和 五种主要离子(不考虑溶液中少量的
五种主要离子(不考虑溶液中少量的 和
和 或其他离子),其中
或其他离子),其中 :
: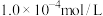 ,
, :
: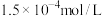 ,
, :
: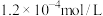 ,
, :
: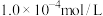 ,则溶液中
,则溶液中 的物质的量浓度是
的物质的量浓度是 。
。(4)水是万物之源,为探究高铁酸钾(化学式为:
 )在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
)在水质处理中发挥的作用,现查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
更新时间:2023-12-21 22:38:43
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】物质的量是联系宏观物质和微观粒子的桥梁。
(1)34g 与标准状况下
与标准状况下_______ L 含有相同数目的H原子。
含有相同数目的H原子。
(2)0.5L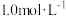
 溶液与0.2L
溶液与0.2L
 溶液中
溶液中 的物质的量浓度之比为
的物质的量浓度之比为_______ 。
(3)100mL 溶液中含有
溶液中含有 2.7g,则
2.7g,则 的物质的量浓度是
的物质的量浓度是_______ mol/L。
(4)同温同压下,体积比为 的
的 和CO,它们的物质的量之比为
和CO,它们的物质的量之比为_______ ,质量之比为_______ (填最简整数比)。
(5)设 为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为
为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为_______  。
。
(6)三种盐的混合溶液中含有0.2mol 、0.25mol
、0.25mol 、0.4mol
、0.4mol 和一定物质的量的
和一定物质的量的 ,则该混合溶液中含有
,则该混合溶液中含有 的个数为
的个数为_______ 。
(1)34g
 与标准状况下
与标准状况下 含有相同数目的H原子。
含有相同数目的H原子。(2)0.5L
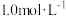
 溶液与0.2L
溶液与0.2L
 溶液中
溶液中 的物质的量浓度之比为
的物质的量浓度之比为(3)100mL
 溶液中含有
溶液中含有 2.7g,则
2.7g,则 的物质的量浓度是
的物质的量浓度是(4)同温同压下,体积比为
 的
的 和CO,它们的物质的量之比为
和CO,它们的物质的量之比为(5)设
 为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为
为阿伏加德罗常数的值,已知ag某气体中含分子数为b,则该气体的摩尔质量为 。
。(6)三种盐的混合溶液中含有0.2mol
 、0.25mol
、0.25mol 、0.4mol
、0.4mol 和一定物质的量的
和一定物质的量的 ,则该混合溶液中含有
,则该混合溶液中含有 的个数为
的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为_______ 。
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为_______ 。
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的_______ 倍。
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在_______ 刻度,容器内气体压强与反应前气体压强之比为_______ 。
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中
 的物质的量浓度是
的物质的量浓度是(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硫有多种含氧酸,亚硫酸(H2SO3),硫酸(H2SO4),焦硫酸(H2SO4·SO3)其中硫酸最为重要,在工业上有广泛的应用。试回答下列问题:
(1)14 mol/L的H2SO4溶液中溶质的质量分数为80%,则7 mol/L的H2SO4溶液中溶质的质量分数将_______ (填“大于”等于”或“小于”)40%。
(2)若将18.4 mol/L的浓硫酸稀释为500 mL 0.2 mol/L的溶液,需用量筒取该浓硫酸____ mL。
(3)焦硫酸(H2SO4·SO3))溶于水,其中的SO3都转化为H2SO4。若将89 g焦硫酸溶于水配成800 mLH2SO4溶液,则该H2SO4溶液的物质的量浓度为_______ mol/L。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:
3FeS2+8O2=Fe3O4+6SO2
4FeS2+11O2=2Fe2O3+8SO2
若2.4 mol FeS2完全反应消耗氧气145.6 L(标准状况),则反应产物中Fe3O4与Fe2O3的物质的量之比为_______ 。
(1)14 mol/L的H2SO4溶液中溶质的质量分数为80%,则7 mol/L的H2SO4溶液中溶质的质量分数将
(2)若将18.4 mol/L的浓硫酸稀释为500 mL 0.2 mol/L的溶液,需用量筒取该浓硫酸
(3)焦硫酸(H2SO4·SO3))溶于水,其中的SO3都转化为H2SO4。若将89 g焦硫酸溶于水配成800 mLH2SO4溶液,则该H2SO4溶液的物质的量浓度为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:
3FeS2+8O2=Fe3O4+6SO2
4FeS2+11O2=2Fe2O3+8SO2
若2.4 mol FeS2完全反应消耗氧气145.6 L(标准状况),则反应产物中Fe3O4与Fe2O3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】填写下列空白:
(1)用14.2g无水硫酸钠配制成500 mL溶液,其物质的量浓度为___ mol/L。
(2) 若从上述溶液中取出10 mL,则这10 mL 溶液的物质的量浓度为_____ mol/L,含溶质的质量为____ g。
(3)若将上述10 ml 溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为____ mol/L;若将稀释后溶液中的SO42-全部沉淀下来,至少需要加入0.1 mol/L的BaCL2溶液_____ mL。
(4)现有36%的醋酸(CH3COOH),密度为1.04g/mL,
欲配制0.1 mol/L的醋酸250 mL,需要取用36%的醋酸_____ mL。
需要使用的实验仪器有烧杯、___ 、___ 、___ 、____ ,
若配制时仅有其中一步操作(如图所示)有错误,其他操作全部正确,则所配醋酸的浓度_____ (填“正确”、“偏大”或“偏小”)。

(1)用14.2g无水硫酸钠配制成500 mL溶液,其物质的量浓度为
(2) 若从上述溶液中取出10 mL,则这10 mL 溶液的物质的量浓度为
(3)若将上述10 ml 溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为
(4)现有36%的醋酸(CH3COOH),密度为1.04g/mL,
欲配制0.1 mol/L的醋酸250 mL,需要取用36%的醋酸
需要使用的实验仪器有烧杯、
若配制时仅有其中一步操作(如图所示)有错误,其他操作全部正确,则所配醋酸的浓度

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识,按要求填写下列空格。
(1)约含 个氧原子的
个氧原子的 的物质的量为
的物质的量为___________  ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是___________ L;
(2) 硫酸铝溶液中,
硫酸铝溶液中,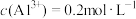 ,则
,则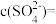
___________  ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为___________  。
。
(3) 某金属硝酸盐
某金属硝酸盐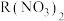 中含有
中含有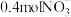 ,则
,则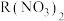 的摩尔质量为
的摩尔质量为___________ , 的相对原子质量为
的相对原子质量为___________ 。
(4)现有标准状况下 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为___________ ,C和O原子个数比为___________ 。
(1)约含
 个氧原子的
个氧原子的 的物质的量为
的物质的量为 ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是(2)
 硫酸铝溶液中,
硫酸铝溶液中,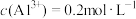 ,则
,则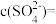
 ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为 。
。(3)
 某金属硝酸盐
某金属硝酸盐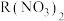 中含有
中含有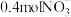 ,则
,则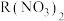 的摩尔质量为
的摩尔质量为 的相对原子质量为
的相对原子质量为(4)现有标准状况下
 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如右图所示。利用标签所提供的信息,回答下列问题:

(1)该注射液中葡萄糖的质量分数为___________
(2)葡萄糖分子的摩尔质量________________
(3)该注射液中溶质与溶剂的分子个数比为_______
(4)该注射液中溶质的物质的量浓度为________ (小数点后保留2位)
(5)已知室温下,饱和葡萄糖水溶液中溶质的质量分数为51.3%, 请计算室温下葡萄糖的溶解度____________ (保留小数点后1位)。
(6)若在实验室利用葡萄糖固体配制该注射液( 500mL5%葡萄糖)在没有容量瓶的情况下,能否配制上述溶液?______ ,若不能说明理由,若能说明配制步骤__________________________

(1)该注射液中葡萄糖的质量分数为
(2)葡萄糖分子的摩尔质量
(3)该注射液中溶质与溶剂的分子个数比为
(4)该注射液中溶质的物质的量浓度为
(5)已知室温下,饱和葡萄糖水溶液中溶质的质量分数为51.3%, 请计算室温下葡萄糖的溶解度
(6)若在实验室利用葡萄糖固体配制该注射液( 500mL5%葡萄糖)在没有容量瓶的情况下,能否配制上述溶液?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气及氯的含氧酸盐在与定条件下均可表现出强氧化性。
(1)向氯气与Na2S2O3溶液反应后的溶液中加入BaCl2溶液,可得到不溶于水和盐酸的白色沉淀,写出前者反应的离子方程式_____________________ ;Cl2与KOH溶液反应时可生成三种盐:KCl、KClO、KClO3,且溶液中c(Cl-):c(ClO-)的值与温度高低有关。当n(KOH)=0.28mol时,Cl2与KOH恰好反应完,且c(Cl-):c(ClO-)=11,则n(ClO-)=_______ ,改变温度时,产物中KClO3的最大理论产量是___________ mol。
(2)400℃时KClO3会分解生成一种无氧酸盐和另一种含氧酸盐,写出相应的化学方程式:____________ ;将KClO3、MnO2、KOH混合后加热,可得到氧化产物K2MnO4反应的化学方程式为___________ 。
(1)向氯气与Na2S2O3溶液反应后的溶液中加入BaCl2溶液,可得到不溶于水和盐酸的白色沉淀,写出前者反应的离子方程式
(2)400℃时KClO3会分解生成一种无氧酸盐和另一种含氧酸盐,写出相应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 电池级碳酸锂是制造LiCoO2等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含Li+、Fe3+、Mg2+、SO 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
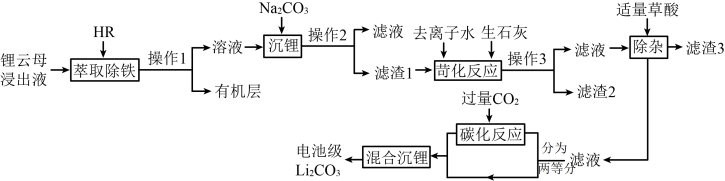
(1)“混合沉锂”的离子方程式为___________ 。
(2)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式___________ 。
 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
(1)“混合沉锂”的离子方程式为
(2)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是人类较早使用的金属之一,运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________
A.纯铁硬度比生铁高
B.不锈钢是铁合金,只含金属元素
C.铁在一定条件下,可与水蒸气反应
(2)向沸水中逐滴滴加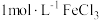 溶液,至液体呈透明的红褐色,该反应的离子方程式为:
溶液,至液体呈透明的红褐色,该反应的离子方程式为:___________ ,形成该分散系的微粒直径范围是___________ 。
(3)电子工业需用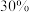 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
(4)高铁酸钠 是一种新型净水剂。
是一种新型净水剂。
①高铁酸钠主要通过如下反应制取: ,则X的化学式为
,则X的化学式为___________ 。
②高铁酸钠在水中可以发生如下反应: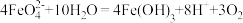 。由此看来,高铁酸钠能够杀菌消毒是因为它具有
。由此看来,高铁酸钠能够杀菌消毒是因为它具有___________ 性。
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是
A.纯铁硬度比生铁高
B.不锈钢是铁合金,只含金属元素
C.铁在一定条件下,可与水蒸气反应
(2)向沸水中逐滴滴加
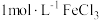 溶液,至液体呈透明的红褐色,该反应的离子方程式为:
溶液,至液体呈透明的红褐色,该反应的离子方程式为:(3)电子工业需用
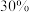 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(4)高铁酸钠
 是一种新型净水剂。
是一种新型净水剂。①高铁酸钠主要通过如下反应制取:
 ,则X的化学式为
,则X的化学式为②高铁酸钠在水中可以发生如下反应:
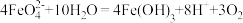 。由此看来,高铁酸钠能够杀菌消毒是因为它具有
。由此看来,高铁酸钠能够杀菌消毒是因为它具有
您最近一年使用:0次
【推荐2】(1)积极保护生态环境可实现人与自然的和谐共处。
①下列做法会加剧温室效应的是____ (填字母)。
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是_____ (填字母)。
a.使用可降解塑料 b.露天焚烧废弃塑料 c.直接填埋废弃塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是_____ (填字母)。

(2)合理应用化学知识可提高人们的生活质量。
某品牌牙膏的成分有甘油、山梨酸钾、氟化钠等。
①在上述牙膏成分中,属于防腐剂的是_____ 。
②甘油的结构简式为______ ;油脂水解时生成甘油和______ 。
③氟化钠(NaF)可与牙齿中的羟基磷酸钙[Ca5(PO4)3OH]反应,生成更难溶的氟磷酸钙[Ca5(PO4)3F],从而达到防治龋齿的目的,写出该反应的化学方程式__________ 。
(3)创新发展材料技术可推动人类社会进步。
①石墨烯(见图)可用作太阳能电池的电极,这里主要利用了石墨烯的_______ 性。

②基础工程建设中常使用水泥、玻璃、钢材等。生产水泥和玻璃都用到得原料是___ ;在钢材中添加铬、镍等元素的目的是____ 。
③新型战斗机常用纳米SiC粉体作为吸收材料,高温下焦炭和石英反应可制得SiC,石英的化学式为______ ;高温分解Si(CH3)2Cl2也可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式_____ 。
①下列做法会加剧温室效应的是
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是
a.使用可降解塑料 b.露天焚烧废弃塑料 c.直接填埋废弃塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是

(2)合理应用化学知识可提高人们的生活质量。
某品牌牙膏的成分有甘油、山梨酸钾、氟化钠等。
①在上述牙膏成分中,属于防腐剂的是
②甘油的结构简式为
③氟化钠(NaF)可与牙齿中的羟基磷酸钙[Ca5(PO4)3OH]反应,生成更难溶的氟磷酸钙[Ca5(PO4)3F],从而达到防治龋齿的目的,写出该反应的化学方程式
(3)创新发展材料技术可推动人类社会进步。
①石墨烯(见图)可用作太阳能电池的电极,这里主要利用了石墨烯的

②基础工程建设中常使用水泥、玻璃、钢材等。生产水泥和玻璃都用到得原料是
③新型战斗机常用纳米SiC粉体作为吸收材料,高温下焦炭和石英反应可制得SiC,石英的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】合金是由两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
(1)下列物质不属于合金的是_____ (填字母)。
A.明矾 B.硬铝 C.生铁 D.青铜
(2)Na、Cu、Al、Fe四种金属的熔、沸点如下:
其中不能形成合金的是______ (填字母)。
①Cu与Na ②Fe与Cu ③Fe与Na ④Al与Na
A.①② B.①③ C.①④ D.②④
(1)下列物质不属于合金的是
A.明矾 B.硬铝 C.生铁 D.青铜
(2)Na、Cu、Al、Fe四种金属的熔、沸点如下:
| 金属 | Na | Cu | Al | Fe |
| 熔点/℃ | 97.8 | 1083 | 660 | 1535 |
| 沸点/℃ | 883 | 2567 | 2467 | 2750 |
①Cu与Na ②Fe与Cu ③Fe与Na ④Al与Na
A.①② B.①③ C.①④ D.②④
您最近一年使用:0次

 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,反应的总离子方程式为:
溶液至中性,反应的总离子方程式为: 都属于酸式盐,但将二者同时加入水中可产生气泡,写出该反应的离子方程式为:
都属于酸式盐,但将二者同时加入水中可产生气泡,写出该反应的离子方程式为: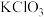 可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式
可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式

