铁是人类较早使用的金属之一,运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________
A.纯铁硬度比生铁高
B.不锈钢是铁合金,只含金属元素
C.铁在一定条件下,可与水蒸气反应
(2)向沸水中逐滴滴加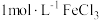 溶液,至液体呈透明的红褐色,该反应的离子方程式为:
溶液,至液体呈透明的红褐色,该反应的离子方程式为:___________ ,形成该分散系的微粒直径范围是___________ 。
(3)电子工业需用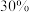 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
(4)高铁酸钠 是一种新型净水剂。
是一种新型净水剂。
①高铁酸钠主要通过如下反应制取: ,则X的化学式为
,则X的化学式为___________ 。
②高铁酸钠在水中可以发生如下反应: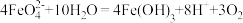 。由此看来,高铁酸钠能够杀菌消毒是因为它具有
。由此看来,高铁酸钠能够杀菌消毒是因为它具有___________ 性。
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是
A.纯铁硬度比生铁高
B.不锈钢是铁合金,只含金属元素
C.铁在一定条件下,可与水蒸气反应
(2)向沸水中逐滴滴加
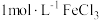 溶液,至液体呈透明的红褐色,该反应的离子方程式为:
溶液,至液体呈透明的红褐色,该反应的离子方程式为:(3)电子工业需用
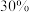 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(4)高铁酸钠
 是一种新型净水剂。
是一种新型净水剂。①高铁酸钠主要通过如下反应制取:
 ,则X的化学式为
,则X的化学式为②高铁酸钠在水中可以发生如下反应:
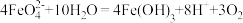 。由此看来,高铁酸钠能够杀菌消毒是因为它具有
。由此看来,高铁酸钠能够杀菌消毒是因为它具有
更新时间:2024-02-03 15:24:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁元素存在多种价态,且不同价态的铁元素在一定条件下可以相互转化。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式___________ 。
(2) 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。
① 中铁元素的化合价为
中铁元素的化合价为___________ ,当有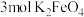 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为___________  。
。
②发生相应反应的离子方程式为___________ 。
(3)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
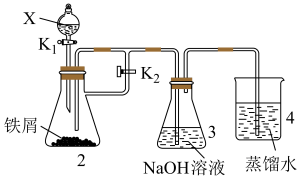
①写出 易被空气中的氧气氧化的方程式
易被空气中的氧气氧化的方程式_______ 。
②X是___________ (填试剂名称),装置4的作用是___________ 。
③实验开始时,开关 应
应___________ (填“打开”成“关闭”);这样操作的目的是___________ 。
(1)向2 mL 1 mol/L的Fe(NO3)2溶液中加入2 mol/L的H2SO4溶液至Fe2+恰好转化为Fe3+为止,写出反应的离子方程式
(2)
 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 。
。①
 中铁元素的化合价为
中铁元素的化合价为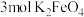 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为 。
。②发生相应反应的离子方程式为
(3)某同学设计如图装置制备一定量的
 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
①写出
 易被空气中的氧气氧化的方程式
易被空气中的氧气氧化的方程式②X是
③实验开始时,开关
 应
应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有中学化学中常见的九种物质:
①氯酸钾固体 ②铜丝 ③Fe(OH)3胶体 ④纯醋酸 ⑤二氧化碳气体 ⑥碳酸氢钾固体 ⑦稀盐酸 ⑧蔗糖晶体 ⑨熔融氢氧化钡,请用上述序号填空:
(1)上述状态下可导电的是__________________ ,属于非电解质的是_______________________ 。
(2)写出⑥在水溶液中的电离方程式:________________________________________ 。
(3)制备③Fe(OH)3胶体的化学方程式:________________________________________ 。
(4)已知①和⑦的浓溶液可以反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,当有10个电子发生转移后,被氧化的氯原子与被还原的氯原子的个数之比是__________________ 。
(5)少量⑥的溶液与大量⑨的溶液混合的离子方程式_______________________ 。
①氯酸钾固体 ②铜丝 ③Fe(OH)3胶体 ④纯醋酸 ⑤二氧化碳气体 ⑥碳酸氢钾固体 ⑦稀盐酸 ⑧蔗糖晶体 ⑨熔融氢氧化钡,请用上述序号填空:
(1)上述状态下可导电的是
(2)写出⑥在水溶液中的电离方程式:
(3)制备③Fe(OH)3胶体的化学方程式:
(4)已知①和⑦的浓溶液可以反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,当有10个电子发生转移后,被氧化的氯原子与被还原的氯原子的个数之比是
(5)少量⑥的溶液与大量⑨的溶液混合的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】废水中氨氮(主要以NH4+和NH3形式存在)的去除常见的有生物脱氮法和电解法。
(1)生物脱氮法是将水中的氨氮通过硝化和反硝化作用最终转化为氮气而除去,其过程如下:
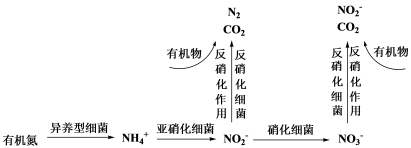
①硝化反应的适宜温度是15~20℃,温度过高,硝化速率会迅速下降,其可能原因是_____ 。
②请写出以有机物甲醇CH3OH对NO3-进行反硝化过程的离子反应方程式_____ 。
(2)电解法产生的强氧化性物质HClO也可将氨氮转化为氮气而除去,实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl的酸性混合溶液来模拟。
①阳极的电极反应式_____ ,处理1mol的(NH4)2SO4,需要消耗HClO的物质的量是_____ mol。
②已知25℃氯水溶液中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如下图所示。
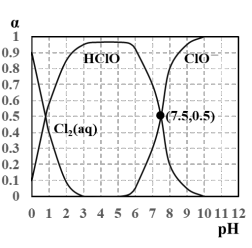
由图可知该温度下HClO的电离常数值为_____ 。
③电解过程中溶液初始Cl-浓度和pH对氨氮去除速率影响关系如图甲和图乙所示。


图甲中发现随着Cl-浓度逐渐增大,氨氮的去除速率不断加快的原因可能是_____ 。
图乙中pH为6时处理效果最佳,当pH过低时,处理效果不佳的原因可能是_____ 。
(1)生物脱氮法是将水中的氨氮通过硝化和反硝化作用最终转化为氮气而除去,其过程如下:
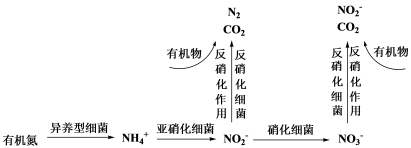
①硝化反应的适宜温度是15~20℃,温度过高,硝化速率会迅速下降,其可能原因是
②请写出以有机物甲醇CH3OH对NO3-进行反硝化过程的离子反应方程式
(2)电解法产生的强氧化性物质HClO也可将氨氮转化为氮气而除去,实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl的酸性混合溶液来模拟。
①阳极的电极反应式
②已知25℃氯水溶液中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如下图所示。

由图可知该温度下HClO的电离常数值为
③电解过程中溶液初始Cl-浓度和pH对氨氮去除速率影响关系如图甲和图乙所示。


图甲中发现随着Cl-浓度逐渐增大,氨氮的去除速率不断加快的原因可能是
图乙中pH为6时处理效果最佳,当pH过低时,处理效果不佳的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一个体重50kg的健康人含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____ 。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_____ 性。下列也能实现这种转化的物质是_____ (填字母序号)。
A.Cl2 B.O2
C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有______ 性。
(4)在Fe+4HNO3===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_____ 性和____ 性,每有1 molFe参加反应,被还原的HNO3为____ mol,转移电子数____ mol。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2
C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海带是高含碘的物质,可以用来提取碘,生产过程可以使用多种氧化剂,如NaNO2、NaClO、Cl2、MnO2等
(1)分别写出使用上述氧化剂提取碘的离子方程式:
_____________________________________________________________
_____________________________________________________________
_____________________________________________________________
_____________________________________________________________
(2)如果使用Cl2作氧化剂,你认为最可能发生的副反应是什么?写出离子反应方程式。
____________________________________________________ 、___________________________________________________
(3)如果发生⑵中副反应,你认为应采取什么办法重新得到碘? 写出离子反应方程式。
___________________________________________________ 、_______________________________________________________
(1)分别写出使用上述氧化剂提取碘的离子方程式:
(2)如果使用Cl2作氧化剂,你认为最可能发生的副反应是什么?写出离子反应方程式。
(3)如果发生⑵中副反应,你认为应采取什么办法重新得到碘? 写出离子反应方程式。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)氯及其化合物在生活中应用广泛。
①将铁片插入盛有少量新制氯水的试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为_____ 。
②向新制氯水中加入碳酸钙固体,可以收集2种气体(水蒸气除外),写出这2种气体的化学式:_____ 。
(2)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为_____ 。
②亚硫酸钠将水中多余次氯酸除去的反应的化学方程式为________________________ 。
(3)某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验:

已知:①无机盐M仅由钠离子和一种含氧酸根离子构成,其化学式中的原子个数比为1∶2∶4。
②如图中所示,将1.66 g该无机盐M溶于水,滴加适量稀硫酸后,再加入 1.12 g 还原铁粉,恰好完全反应得混合溶液N。
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验。
④在路线Ⅱ中,首先向溶液N中滴加适量NaOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得到纯净的Fe2O3粉末1.20 g;再将滤液在一定条件下蒸干,只得到2.84 g纯净的不含结晶水的正盐W。
请按要求回答下列问题:
①由路线Ⅰ的现象可知,溶液N中含有的阳离子是_____ 。
②由实验流程图可推得,含氧酸盐W的化学式是_____ 。
③无机盐M的溶液与1.12 g还原铁粉恰好完全反应生成溶液N的离子方程式为________________ 。
①将铁片插入盛有少量新制氯水的试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为
②向新制氯水中加入碳酸钙固体,可以收集2种气体(水蒸气除外),写出这2种气体的化学式:
(2)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为
②亚硫酸钠将水中多余次氯酸除去的反应的化学方程式为
(3)某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验:

已知:①无机盐M仅由钠离子和一种含氧酸根离子构成,其化学式中的原子个数比为1∶2∶4。
②如图中所示,将1.66 g该无机盐M溶于水,滴加适量稀硫酸后,再加入 1.12 g 还原铁粉,恰好完全反应得混合溶液N。
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验。
④在路线Ⅱ中,首先向溶液N中滴加适量NaOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得到纯净的Fe2O3粉末1.20 g;再将滤液在一定条件下蒸干,只得到2.84 g纯净的不含结晶水的正盐W。
请按要求回答下列问题:
①由路线Ⅰ的现象可知,溶液N中含有的阳离子是
②由实验流程图可推得,含氧酸盐W的化学式是
③无机盐M的溶液与1.12 g还原铁粉恰好完全反应生成溶液N的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁是应用最广泛的金属,铁的卤化物、氧化物、氢氧化物以及高价铁的含氧酸盐均为重要化合物。如图是铁及其化合物的“价一类”二维图。回答下列问题:

(1)在高温下,甲与水蒸气反应的化学方程式为___________ 。
(2)若戊为硫酸盐,缺铁性贫血往往口服戊,当用戊制成药片时,外表包有一层特殊的糖衣,其作用是防止___________ 。
(3)铁元素的高价铁盐 可以做杀毒剂和净水剂,原因是
可以做杀毒剂和净水剂,原因是___________ 。
(4)若己为氯化物,工业上还可以用己溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是___________ (填字母)。
a.若无固体剩余,则溶液中可能含有 、
、 、
、 、
、 四种离子
四种离子
b.若溶液中有 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余
c.若有固体剩余,则溶液中一定有反应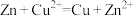 发生
发生
d.当溶液中有 存在时,则一定没有Cu析出
存在时,则一定没有Cu析出

(1)在高温下,甲与水蒸气反应的化学方程式为
(2)若戊为硫酸盐,缺铁性贫血往往口服戊,当用戊制成药片时,外表包有一层特殊的糖衣,其作用是防止
(3)铁元素的高价铁盐
 可以做杀毒剂和净水剂,原因是
可以做杀毒剂和净水剂,原因是(4)若己为氯化物,工业上还可以用己溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是
a.若无固体剩余,则溶液中可能含有
 、
、 、
、 、
、 四种离子
四种离子b.若溶液中有
 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余c.若有固体剩余,则溶液中一定有反应
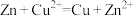 发生
发生d.当溶液中有
 存在时,则一定没有Cu析出
存在时,则一定没有Cu析出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾。制备方法有:①湿法:次氯酸盐氧化法②干法:高温过氧化物氧化法。
(1)湿法制备的主要反应为:Fe(OH)3+NaClO+ →Na2FeO4+NaCl+H2O
在上述空格中填写适当物质,并配平化学反应方程式___ 。
(2)上述反应中1mol氧化剂___ (填“得到”或“失去”)__ mol电子。
(3)干法制备中牵涉到的物质有:FeSO4、Na2FeO4、Na2SO4、Na2O2
发生氧化反应的过程是:___ →___ 。
(4)制备相同质量Na2FeO4时转移的电子数,湿法制备___ 干法制备(填“>”或“<”或“=”)
(5)干法制备中,一定要在密闭容器中进行,原因是__ 。
(1)湿法制备的主要反应为:Fe(OH)3+NaClO+ →Na2FeO4+NaCl+H2O
在上述空格中填写适当物质,并配平化学反应方程式
(2)上述反应中1mol氧化剂
(3)干法制备中牵涉到的物质有:FeSO4、Na2FeO4、Na2SO4、Na2O2
发生氧化反应的过程是:
(4)制备相同质量Na2FeO4时转移的电子数,湿法制备
(5)干法制备中,一定要在密闭容器中进行,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质,可利用明矾石制备氢氧化铝。
(1)已知明矾石脱水后要硫化,化学方程式为2Al2(SO4)3+3S 2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是
2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是___________ ;若生成1 mol Al2O3,则转移的电子数为________ 。
(2)证明废渣中含有Fe2O3 的化学方法:_____________________ 。
II.镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为:Mg17Al12 + 17H2=17MgH2 + 12Al ,得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。
(3)熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是_____________________
(4)在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为_______ mol。(已知:MgH2 + 2HCl = MgCl2 + 2H2↑)
(1)已知明矾石脱水后要硫化,化学方程式为2Al2(SO4)3+3S
 2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是
2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是(2)证明废渣中含有Fe2O3 的化学方法:
II.镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为:Mg17Al12 + 17H2=17MgH2 + 12Al ,得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。
(3)熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是
(4)在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】考古出土的吴王夫差剑为春秋末期制造的青铜剑,历经2500余年,剑的表面虽有一层蓝色薄锈,但仍寒光逼人,剑刃锋利。回答下列问题。
(1)青铜是一种合金材料,该合金的主要成分是___________ (填元素符号)。合金材料有许多优良性能,比如①多数合金的熔点___________ 组成它的任何一种组分金属。②合金的导电性和导热性一般 ___________ 任何一种组分金属。(填“高于”或“低于”)。不锈钢中除了铁元素外,主要的合金元素是 ___________ (占12%-32%),采用该元素作合金是因为: ___________ 。
(2)从上述信息可以看出,青铜具有的性质有___________(填字母)
(3)青铜剑表面的蓝色薄锈,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],这层蓝色薄锈形成的原理是 ___________ 。(用方程式表示)
(4)若要除去表面蓝色薄锈,一是用稀硫酸洗涤,该反应的离子方程式________________ ;此法弊端是 ___________ 。二是可以在炼铁高炉中锻造,其原理 ___________ 。
(1)青铜是一种合金材料,该合金的主要成分是
(2)从上述信息可以看出,青铜具有的性质有___________(填字母)
| A.强度高 | B.耐腐蚀 | C.可塑性好 | D.易加工 |
(4)若要除去表面蓝色薄锈,一是用稀硫酸洗涤,该反应的离子方程式
您最近一年使用:0次



