回答下列问题
(1)①写出金刚砂的化学式:_______ ;②写出S2Cl2的电子式:_______ ;
(2)NH2OH 显弱碱性的原因和NH3类似,写出 NH2OH 在水溶液中的电离方程式_______ 。
(3)用一个化学方程式证明碳酸的酸性强于硅酸:_______ 。
(1)①写出金刚砂的化学式:
(2)NH2OH 显弱碱性的原因和NH3类似,写出 NH2OH 在水溶液中的电离方程式
(3)用一个化学方程式证明碳酸的酸性强于硅酸:
更新时间:2021-10-26 16:52:36
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氨的化学性质
(1)氨与水的反应
氨的水溶液俗称____ ,显____ 性,反应的方程式为____ 。
(2)氨与酸的反应
两根分别蘸取浓氨水和浓盐酸的玻璃棒,靠近时,产生____ ,反应方程式为____ 。
(3)氨具有还原性
①氨的催化氧化,反应化学方程式:____ ,NH3在反应中作____ 。
②氨可在加热条件下和氧化铜反应生成铜和氮气,反应的化学方程式为____ 。
(1)氨与水的反应
氨的水溶液俗称
(2)氨与酸的反应
两根分别蘸取浓氨水和浓盐酸的玻璃棒,靠近时,产生
(3)氨具有还原性
①氨的催化氧化,反应化学方程式:
②氨可在加热条件下和氧化铜反应生成铜和氮气,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列方程式
(1)钠与水反应(离子方程式)__________________________ ;
(2)用氯化铁溶液腐蚀印刷电路板(离子方程式)__________________________ ;
(3)铝与氢氧化钠溶液反应(离子方程式)__________________________ ;
(4)氢氧化铁胶体制备(化学方程式)__________________________ ;
(5)侯氏制碱法原理(化学方程式)__________________________ 。
(1)钠与水反应(离子方程式)
(2)用氯化铁溶液腐蚀印刷电路板(离子方程式)
(3)铝与氢氧化钠溶液反应(离子方程式)
(4)氢氧化铁胶体制备(化学方程式)
(5)侯氏制碱法原理(化学方程式)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】非金属元素在生产生活中扮演着重要角色。请根据题意填空;
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变_______ (填“红”或“蓝”);
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被_______ (填“氧化”或“还原”),起到保质作用;
(3)玻璃中的成分SiO2能与NaOH溶液反应: ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带_______ (填“玻璃塞”或“橡胶塞”)的试剂瓶。
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被
(3)玻璃中的成分SiO2能与NaOH溶液反应:
 ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3和X。
①根据题意,可判断出X是_____________ (写化学式)
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:______ 。
(2)铝元素是地壳中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式____________________________________ 。
(3)Na2O2可用作呼吸面具的供氧剂,发生反应的化学方程式为____________________ 。
(4)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式_________________________________ 。
(5)小苏打可作胃药,请写出其中和胃酸时的离子方程式______________________ 。
(6)在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,被氧化的元素是____________ ,当有5mol水反应时,由H2O还原的BrF3为______________ mol。
(1)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3和X。
①根据题意,可判断出X是
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:
(2)铝元素是地壳中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式
(3)Na2O2可用作呼吸面具的供氧剂,发生反应的化学方程式为
(4)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式
(5)小苏打可作胃药,请写出其中和胃酸时的离子方程式
(6)在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)在 CO、CO2、SO2、NO、NO2、SiO2中,属于酸性氧化物的是__________ ,能导致酸雨的是___________ 。
(2)硅酸钠是为数不多的溶于水的硅酸盐,向硅酸钠溶液中通入足量CO2有白色沉淀产生,写出该反应的离子反应方程式:____________________ 。
(3)有如下反应(未配平):BrF3+H2O→Br2+O2+HBrO3+HF,已知生成物中Br2与O2的物质的量之比为1∶1。则:
①配平后H2O与HF物质的量之比为___________ ;
②还原剂为______________ ;
③如有5mol H2O参加反应,则参加氧化还原反应的H2O物质的量为_______________ mol。
(1)在 CO、CO2、SO2、NO、NO2、SiO2中,属于酸性氧化物的是
(2)硅酸钠是为数不多的溶于水的硅酸盐,向硅酸钠溶液中通入足量CO2有白色沉淀产生,写出该反应的离子反应方程式:
(3)有如下反应(未配平):BrF3+H2O→Br2+O2+HBrO3+HF,已知生成物中Br2与O2的物质的量之比为1∶1。则:
①配平后H2O与HF物质的量之比为
②还原剂为
③如有5mol H2O参加反应,则参加氧化还原反应的H2O物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题.
(1)久置的硅酸钠溶液会出现浑浊现象其原因为________ (用化学方程式表示)
(2)红热的木炭与浓硫酸反应的化学方程式________
(3)SO2催化氧化成SO3的化学方程式:________
(4)写出铜与稀硝酸反应的离子方程式________
(5)实验室制取氨气的化学方程式为________ ,常用________ 来干燥氨气.
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是________ ,还原产物是_______ .
②氧化剂与氧化产物的物质的量比是________ 。
(1)久置的硅酸钠溶液会出现浑浊现象其原因为
(2)红热的木炭与浓硫酸反应的化学方程式
(3)SO2催化氧化成SO3的化学方程式:
(4)写出铜与稀硝酸反应的离子方程式
(5)实验室制取氨气的化学方程式为
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是
②氧化剂与氧化产物的物质的量比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
______ SiO2+_______ C+______ N2
_______ Si3N4+_____ CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是___________ 。
(3)分析反应可推测碳、氮气的氧化性:C________ N2(填“>”“<”“=”)。
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途

根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是
(3)分析反应可推测碳、氮气的氧化性:C
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年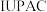 确认了四种新元素,其中一种为
确认了四种新元素,其中一种为 ,中文名为“镆”。元素
,中文名为“镆”。元素 可由反应:
可由反应: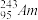 +
+ =
= +3
+3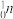 得到。该元素的质子数为
得到。该元素的质子数为______ ,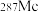 与
与 互为
互为_________ 。
(2) 位于元素周期表中第
位于元素周期表中第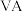 族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式
族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式________________ .该分子内存在的共价键类型有_______ 。
(3)该族中的另一元素P能呈现多种化合价,其中 价氧化物的分子式为
价氧化物的分子式为______ , 价简单含氧酸的分子式为
价简单含氧酸的分子式为______ 。
(1)2016年
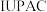 确认了四种新元素,其中一种为
确认了四种新元素,其中一种为 ,中文名为“镆”。元素
,中文名为“镆”。元素 可由反应:
可由反应: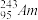 +
+ =
= +3
+3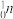 得到。该元素的质子数为
得到。该元素的质子数为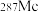 与
与 互为
互为(2)
 位于元素周期表中第
位于元素周期表中第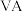 族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式
族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式(3)该族中的另一元素P能呈现多种化合价,其中
 价氧化物的分子式为
价氧化物的分子式为 价简单含氧酸的分子式为
价简单含氧酸的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)比较 S 和 Cl 元素非金属性相对强弱:S__ Cl(填“<”、“>”或“=”),用离子方程式说明Cl-和 S2-失电子能力的相对强弱_____ 。
(2)CSO 是共价化合物,各原子均满足 8 电子稳定结构,写出 CSO 的电子式_____ 。
(3)常压下,石英的硬度比晶体硅的硬度大,其主要原因是_____ 。
(2)CSO 是共价化合物,各原子均满足 8 电子稳定结构,写出 CSO 的电子式
(3)常压下,石英的硬度比晶体硅的硬度大,其主要原因是
您最近一年使用:0次



