实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL:
(1)配制时,必须使用到的玻璃仪器有_______ 、_______ 、_______ 、_______ 。
(2)使用容量瓶前必须进行的一步操作是_______ 。
(3)要完成本实验该同学应称出NaOH_______ g。
(4)在配制过程中,其他操作都是正确的,下列情况会引起所配溶液浓度偏高的是_______ 。
①固体药品混有少量氧化钠
②称量时间过长
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
(1)配制时,必须使用到的玻璃仪器有
(2)使用容量瓶前必须进行的一步操作是
(3)要完成本实验该同学应称出NaOH
(4)在配制过程中,其他操作都是正确的,下列情况会引起所配溶液浓度偏高的是
①固体药品混有少量氧化钠
②称量时间过长
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
更新时间:2021-10-20 08:34:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】(I)化学是一门以实验为基础的学科,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验装置图回答问题:
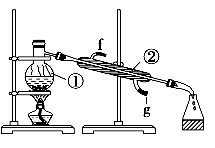
(1)写出上图中所示仪器的名称:①___ ;②___ 。
(2)若利用该装置分离乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有___ ,将仪器补充完整后进行的实验操作的名称为___ ;实验时仪器②中冷却水的进口为________ (填“f”或“g”)。
(3)应用上述分离操作,首先得到的物质是________ 。
(4)蒸馏烧瓶内碎瓷片的作用是________________ 。
(Ⅱ)硫酸试剂瓶标签上的内容:

(1)该硫酸的物质的量浓度是________ mol·L-1。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要240 mL 4.6 mol·L-1的稀硫酸,则配制稀硫酸时需要取________ mL的该硫酸;配制时需选用的仪器主要有量筒、烧杯、玻璃棒、___ 、___ (在横线上填写所缺仪器的名称)。
(3)配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是___ (填序号)。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线

(1)写出上图中所示仪器的名称:①
(2)若利用该装置分离乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有
(3)应用上述分离操作,首先得到的物质是
(4)蒸馏烧瓶内碎瓷片的作用是
(Ⅱ)硫酸试剂瓶标签上的内容:

(1)该硫酸的物质的量浓度是
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要240 mL 4.6 mol·L-1的稀硫酸,则配制稀硫酸时需要取
(3)配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
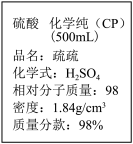
现欲用该浓硫酸配制成1mol/L的稀硫酸,现实验室仅需要这种稀硫酸220mL。试回答下列问题:
(1)用量筒量取该浓硫酸____________ mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是____ 。
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是__________ 。
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,仰视容量瓶刻度线
(4)某同学用固体Na2CO3配制500 mlL 0.1mol•L-1溶液的过程如图所示:

你认为该同学的错误步骤有__________ 处。

现欲用该浓硫酸配制成1mol/L的稀硫酸,现实验室仅需要这种稀硫酸220mL。试回答下列问题:
(1)用量筒量取该浓硫酸
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,仰视容量瓶刻度线
(4)某同学用固体Na2CO3配制500 mlL 0.1mol•L-1溶液的过程如图所示:

你认为该同学的错误步骤有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室需要0.2 mol/LNaOH溶液480 mL和0.5 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)用如图所示的仪器中配制溶液肯定不需要的是___________ (填字母),配制上述溶液还需用到的玻璃仪器是___________ (填仪器名称)。
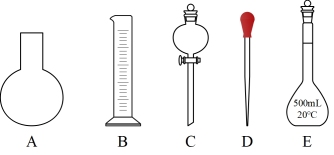
(2)下列有关容量瓶使用方法的操作中,错误的是___________(填字母)。
(3)在配制NaOH溶液时:
①根据计算,用托盘天平称取NaOH的质量为___________ g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___________ (填“>”“<”或“=”,下同)0.2 mol/L;
③若NaOH固体溶解后立即移入容量瓶→洗涤烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度___________ 0.2mol/L。
(4)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为___________ (计算结果保留一位小数)mL;
②如果实验室有15 mL、20 mL、50 mL规格的量筒,应选用___________ mL量筒最好。
(1)用如图所示的仪器中配制溶液肯定不需要的是

(2)下列有关容量瓶使用方法的操作中,错误的是___________(填字母)。
| A.使用容量瓶之前应检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后,再用待配溶液润洗 |
| C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平 |
| D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容 |
| E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复上下颠倒、摇匀 |
①根据计算,用托盘天平称取NaOH的质量为
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度
③若NaOH固体溶解后立即移入容量瓶→洗涤烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度
(4)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
②如果实验室有15 mL、20 mL、50 mL规格的量筒,应选用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】已知:硫代硫酸钠(化学式为Na2S2O3)易溶于水,具有强还原性,其相对分子质量是158。某实验室配制500mL0.100mol·L-1Na2S2O3溶液,并测定样品中CuSO4·5H2O的纯度:
(1)使用无水硫代硫酸钠进行配制,需要固体的质量是___________ 。配制过程中需要的玻璃仪器有玻璃棒、烧杯、胶头滴管和___________ 。
(2)配制时使用的蒸馏水需先烧开再冷却,其目的是___________ 。
(3)定容时俯视刻度线,则配制得到的Na2S2O3溶液的浓度将___________ (填“偏大”、“偏小”或“不变”)。定容时,如果不小心加水超过了刻度线,则处理的方法是___________ 。
(4)测定样品CuSO4·5H2O的纯度:准确称取0.5000gCuSO4·5H2O样品,加入适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀硫酸酸化,以淀粉溶液为指示剂,用0.100mol·L-1Na2S2O3溶液反应至终点,消耗Na2S2O3溶液19.20mL。过程中发生下列反应:2CuSO4+4KI=2CuI↓+I2+2K2SO4;2Na2S2O3+I2=Na2S4O6+2NaI;计算CuSO4·5H2O样品的纯度(纯度=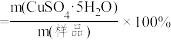 ,写出计算过程)
,写出计算过程)___________ 。
(1)使用无水硫代硫酸钠进行配制,需要固体的质量是
(2)配制时使用的蒸馏水需先烧开再冷却,其目的是
(3)定容时俯视刻度线,则配制得到的Na2S2O3溶液的浓度将
(4)测定样品CuSO4·5H2O的纯度:准确称取0.5000gCuSO4·5H2O样品,加入适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀硫酸酸化,以淀粉溶液为指示剂,用0.100mol·L-1Na2S2O3溶液反应至终点,消耗Na2S2O3溶液19.20mL。过程中发生下列反应:2CuSO4+4KI=2CuI↓+I2+2K2SO4;2Na2S2O3+I2=Na2S4O6+2NaI;计算CuSO4·5H2O样品的纯度(纯度=
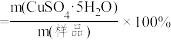 ,写出计算过程)
,写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作如下(该药片中其他成分不与盐酸或者氢氧化钠反应):
①配制0.10 mol/L的稀盐酸和0.10 mol/L的NaOH溶液:
②向一粒研碎后的药片(0.10g)中加入20.00mL蒸馏水:
③加入25.00mL 0.10mol/L的稀盐酸;
④用0.10mol/L的NaOH溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积。
请回答下列问题:
(1)该测定实验共进行了4次,其中步骤①中配制0.10mo/L的稀盐酸需要用到的仪器有_______ 。(填写字母)
A.托盘天平 B.胶头滴管 C.烧杯 D.量筒 E.玻璃棒 F.50mL容量瓶 G.250mL容量瓶
(2)步骤③和步骤④中发生反应的离子方程式分别为_______ 、_______ 。
(3)配制0.10 mol/L的NaOH溶液,下列说法正确的是_______。
(4)某同学4次测定所消耗的NaOH溶液的体积如下:
计算这种药片中碳酸钙的质量分数_______ 。
①配制0.10 mol/L的稀盐酸和0.10 mol/L的NaOH溶液:
②向一粒研碎后的药片(0.10g)中加入20.00mL蒸馏水:
③加入25.00mL 0.10mol/L的稀盐酸;
④用0.10mol/L的NaOH溶液中和过量的稀盐酸,记录所消耗NaOH溶液的体积。
请回答下列问题:
(1)该测定实验共进行了4次,其中步骤①中配制0.10mo/L的稀盐酸需要用到的仪器有
A.托盘天平 B.胶头滴管 C.烧杯 D.量筒 E.玻璃棒 F.50mL容量瓶 G.250mL容量瓶
(2)步骤③和步骤④中发生反应的离子方程式分别为
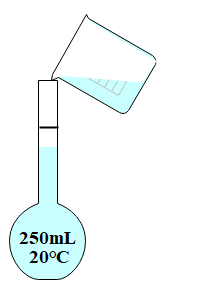
(3)配制0.10 mol/L的NaOH溶液,下列说法正确的是_______。

| A.NaOH固体可放在烧杯中称量 |
| B.定容时的操作如图所示 |
| C.NaoH固体溶解后立即转移到容量瓶中,所得溶液浓度偏低 |
| D.末用蒸馏水洗涤烧杯和玻璃棒,所得溶液的浓度偏低 |
| 测定次数 | 1 | 2 | 3 | 4 |
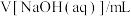 | 12.00 | 11.90 | 12.10 | 14.00 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】现用质量分数为98%、密度为1.84g·cm-3的浓H2SO4来配制450mL、0.2mol·L-1的稀H2SO4。
(1)除烧杯、玻璃棒、量筒外,配制上述溶液还需要的玻璃仪器是___________ 。
(2)经计算,需用量筒量取浓H2SO4的体积为___________ 。
(3)稀释浓硫酸的方法是________ 。
(4)在配制过程中,其他操作都准确,下列操作中,能引起浓度偏高的有___________ (填代号)。
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中;
②洗涤溶解用的烧杯与玻璃棒,并将洗涤液转移到容量瓶中;
③转移前,容量瓶中含有少量蒸馏水;
④定容时,俯视标线;
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线。
(1)除烧杯、玻璃棒、量筒外,配制上述溶液还需要的玻璃仪器是
(2)经计算,需用量筒量取浓H2SO4的体积为
(3)稀释浓硫酸的方法是
(4)在配制过程中,其他操作都准确,下列操作中,能引起浓度偏高的有
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中;
②洗涤溶解用的烧杯与玻璃棒,并将洗涤液转移到容量瓶中;
③转移前,容量瓶中含有少量蒸馏水;
④定容时,俯视标线;
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线。
您最近一年使用:0次



