回答下列问题
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=___________ kJ·mol-1。
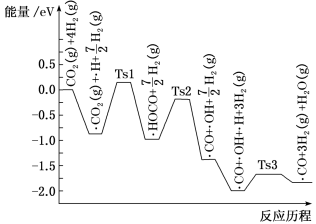
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会___________ (填“放出热量”或“吸收热量”);反应历程中最小能垒步骤的化学方程式为___________ 。
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l) CH4(g)+CO(g)的ΔH=
CH4(g)+CO(g)的ΔH=___________ 。
(4)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是___________ 。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)
 NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1反应Ⅱ:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1总反应:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1则反应Ⅰ的ΔH1=
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)
 CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)
 CH4(g)+CO(g)的ΔH=
CH4(g)+CO(g)的ΔH=(4)已知断开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式是
更新时间:2021-10-23 14:39:10
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】在如图所示的量热计中,将100mL 0.50mol·L-1CH3COOH溶液与100mL0.55mol·L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃。已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J·℃-1,生成溶液的比热容为4.184J·g-1·℃-1,溶液的密度均近似为1g·mL-1。
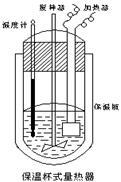
(1)试求CH3COOH的中和热△H =________ kJ/mol。
(2)CH3COOH的中和热的文献值为56.1KJ· mol-1,则请你分析在(1)中测得的实验值偏差可能的原因_________________ 。(答两条原因)
(3)实验中NaOH过量的目的是__________________ 。

(1)试求CH3COOH的中和热△H =
(2)CH3COOH的中和热的文献值为56.1KJ· mol-1,则请你分析在(1)中测得的实验值偏差可能的原因
(3)实验中NaOH过量的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应同时存在着物质和能量的变化,依据化学反应与能量变化回答下列问题:
(1)已知汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。反应的化学方程式为2NO(g)+2CO(g) N2(g)+2CO2(g)。已知部分化学键的键能如下:
N2(g)+2CO2(g)。已知部分化学键的键能如下:
请计算上述反应的ΔH=_____ kJ/mol。
(2)1gH2气体完全燃烧生成液态水放出143kJ热量,其热化学方程式为:_____ 。
(3)已知①2O2(g)+N2(g)=N2O4(l)ΔH1;
②N2(g)+2H2(g)=N2H4(l)ΔH2;
③O2(g)+2H2(g)=2H2O(g)ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=_____ 。
(4)已知稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出的热量比57.3kJ_____ (填“大”“小”)。
(5)将1molCH4与Cl2发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl2的物质的量为_____ 。
(1)已知汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。反应的化学方程式为2NO(g)+2CO(g)
 N2(g)+2CO2(g)。已知部分化学键的键能如下:
N2(g)+2CO2(g)。已知部分化学键的键能如下:| 分子式/结构式 | NO/N≡O | CO/C=O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C=O | C=O | N≡N |
| 键能/(kJ/mol) | 632 | 1072 | 750 | 946 |
请计算上述反应的ΔH=
(2)1gH2气体完全燃烧生成液态水放出143kJ热量,其热化学方程式为:
(3)已知①2O2(g)+N2(g)=N2O4(l)ΔH1;
②N2(g)+2H2(g)=N2H4(l)ΔH2;
③O2(g)+2H2(g)=2H2O(g)ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=
(4)已知稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出的热量比57.3kJ
(5)将1molCH4与Cl2发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下:

根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为________________________ 。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) ΔH= -90.8kJ·mol-1
CH3OH(g) ΔH= -90.8kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH= -41.3kJ·mol-1
CO2(g)+H2(g) ΔH= -41.3kJ·mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH=
CH3OCH3(g)+CO2(g);ΔH=______ 。

根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)
 CH3OH(g) ΔH= -90.8kJ·mol-1
CH3OH(g) ΔH= -90.8kJ·mol-1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH= -23.5kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH= -41.3kJ·mol-1
CO2(g)+H2(g) ΔH= -41.3kJ·mol-1完成热化学反应方程式:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g);ΔH=
CH3OCH3(g)+CO2(g);ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知某反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。

该反应是____ (填“吸热”或“放热”)反应,该反应的ΔH=_____ kJ· mol-1(用含E1、E2的代数式表示)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l) =H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式___________________________ 。
(3)已知:H2(g)+Cl2(g)==2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为______ kJ。
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是_________________ 。
 C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。
该反应是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l) =H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)已知:H2(g)+Cl2(g)==2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。
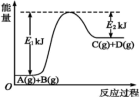
①该反应是_______ (填“吸热”或“放热”)反应,反应的ΔH=_______ kJ· mol-1(用含E1、E2的代数式表示)。
②该反应过程中,断裂旧化学键吸收的总能量_______ (填“>”“ <”或“=”)形成新化学键释放的总能量。
(2)已知:①C4H10(g)+ O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
② H2(g)+ O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
则:C4H10(g)= C4H8(g)+H2(g) ΔH3=_______ kJ·mol-1。
(3)已知拆开1 mol H-Cl键、1 mol H-H键、1 mol Cl-Cl键分别需要的能量是431 kJ、436 kJ、243 kJ,则2 mol HCl气体分解生成1molCl2与1 molH2的热化学方程式为_______ 。
(4)已知:101 kPa时,C(s)+O2(g)═CO(g) ΔH=﹣110.5kJ/mol,则碳的燃烧热数值_______ 110.5 kJ/mol(填>,<,=)。
(1)某反应A(g)+B(g)= C(g)+D(g)过程中的能量变化如图所示,回答问题。

①该反应是
②该反应过程中,断裂旧化学键吸收的总能量
(2)已知:①C4H10(g)+
 O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH1=-119 kJ·mol-1 ② H2(g)+
 O2(g) = H2O(g) ΔH2=-242 kJ·mol-1
O2(g) = H2O(g) ΔH2=-242 kJ·mol-1则:C4H10(g)= C4H8(g)+H2(g) ΔH3=
(3)已知拆开1 mol H-Cl键、1 mol H-H键、1 mol Cl-Cl键分别需要的能量是431 kJ、436 kJ、243 kJ,则2 mol HCl气体分解生成1molCl2与1 molH2的热化学方程式为
(4)已知:101 kPa时,C(s)+O2(g)═CO(g) ΔH=﹣110.5kJ/mol,则碳的燃烧热数值
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
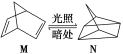 ΔH=88.6 kJ/mol
ΔH=88.6 kJ/mol
则M、N相比,较稳定的是___________ 。
(2)已知CH3OH(l)的燃烧热为-726.5 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2O(g) ΔH=-a kJ·mol-1,则a___________ 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应生成1molCO2时的热化学方程式:___________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为___________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=88.6 kJ/mol
ΔH=88.6 kJ/mol则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热为-726.5 kJ·mol-1,CH3OH(l)+1/2O2(g)=CO2(g)+2H2O(g) ΔH=-a kJ·mol-1,则a
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应生成1molCO2时的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知下列热化学方程式:
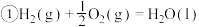
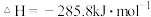


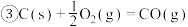
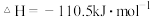
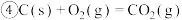
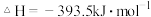
回答下列问题:
(1)上述反应中属于放热反应的是________ 。
(2)H2的燃烧热
________________ ;C的燃烧热
________________ 。
(3)燃烧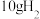 生成液态水,放出的热量为
生成液态水,放出的热量为________ 。
(4)写出CO燃烧的热化学方程式:________________________________ 。
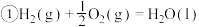
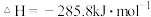


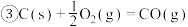
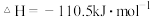
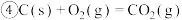
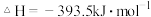
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热


(3)燃烧
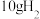 生成液态水,放出的热量为
生成液态水,放出的热量为(4)写出CO燃烧的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) △H=-285.8kJ/mol
O2(g)=H2O(l) △H=-285.8kJ/mol
②CO(g)=C(s)+ O2(g) △H=+110.5kJ/mol
O2(g) △H=+110.5kJ/mol
③H2(g)+ O2(g)=H2O(g) △H=-241.8kJ/mol
O2(g)=H2O(g) △H=-241.8kJ/mol
④CO2(g)=C(s)+O2(g) △H=+393.5kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填序号)。
(2)H2的燃烧热为_______ 。
(3)已知如下热化学方程式:
①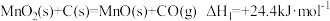
②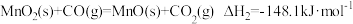
③
则△H3=_______ 。
①H2(g)+
 O2(g)=H2O(l) △H=-285.8kJ/mol
O2(g)=H2O(l) △H=-285.8kJ/mol②CO(g)=C(s)+
 O2(g) △H=+110.5kJ/mol
O2(g) △H=+110.5kJ/mol③H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ/mol
O2(g)=H2O(g) △H=-241.8kJ/mol④CO2(g)=C(s)+O2(g) △H=+393.5kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)已知如下热化学方程式:
①
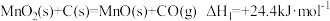
②
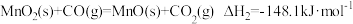
③

则△H3=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于___________ (填“热吸”或“放热”)反应。
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:___________ 。
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②
则白磷转化为红磷的热化学方程式为___________ 。
(4)已知破坏1molH-H键、1molI-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2molHI需要放出___________ kJ的热量。
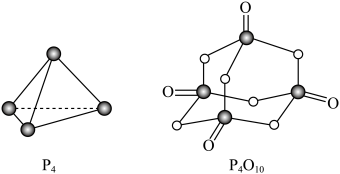
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P-P键akJ·mol-1、P-O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为___________ 。
(6)常温下,pH=1的H2SO4溶液,由水电离出来的c(H+)=___________ mol/L
(7)H3BO3溶液中存在以下平衡:H3BO3(aq)+H2O(l)⇌[B(OH)4]-(aq)+H+(aq)。已知0.70mol/LH3BO3溶液在298K达到平衡时,c(H+)=2.0×10-5mol/L,水的电离忽略不计,求此温度下该反应的平衡常数K(保留2位有效数字):___________ 。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②则白磷转化为红磷的热化学方程式为
(4)已知破坏1molH-H键、1molI-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2molHI需要放出
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P-P键akJ·mol-1、P-O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为

(6)常温下,pH=1的H2SO4溶液,由水电离出来的c(H+)=
(7)H3BO3溶液中存在以下平衡:H3BO3(aq)+H2O(l)⇌[B(OH)4]-(aq)+H+(aq)。已知0.70mol/LH3BO3溶液在298K达到平衡时,c(H+)=2.0×10-5mol/L,水的电离忽略不计,求此温度下该反应的平衡常数K(保留2位有效数字):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
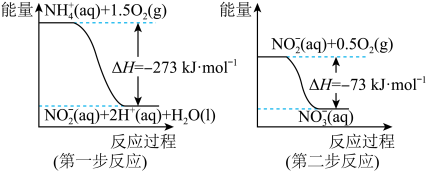
(1)第一步反应是________ (填“放热”或“吸热”)反应,判断依据是_______________________ 。
(2)已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1①
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226kJ·mol-1②
O2(g) ΔH=-226kJ·mol-1②
则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为__________ 。
(3)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=______________ 。
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
(1)第一步反应是
(2)已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1①
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-226kJ·mol-1②
O2(g) ΔH=-226kJ·mol-1②则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为
(3)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
则表中a=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为_______ ;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式_______ ;
(3)已知H2O(l)=H2O(g) ΔH3=+44 kJ·mol-1,则表示肼燃烧热的热化学方程式为_______ 。
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为_______ 。
(1)氮元素原子的L层电子数为
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式
(3)已知H2O(l)=H2O(g) ΔH3=+44 kJ·mol-1,则表示肼燃烧热的热化学方程式为
(4)肼-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
您最近一年使用:0次



