完成下列问题。
(1)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
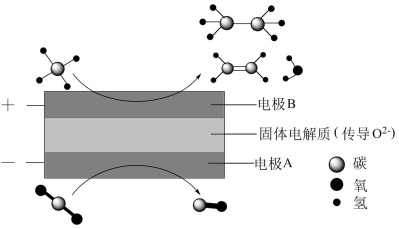
阴极上的反应式为___________ 。
(2)我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
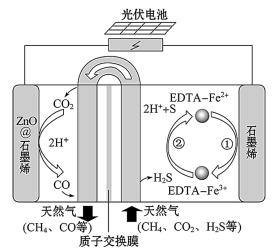
该装置工作时,阴极的电极反应:_____ ;协同转化总反应:______ ;若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为______ (填“碱性”“中性”或“酸性”)。
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极增重______ g。
(1)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:

阴极上的反应式为
(2)我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+

该装置工作时,阴极的电极反应:
(3)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池正极增重
更新时间:2021-10-27 09:17:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法 。
(1)某兴趣小组以SO2为原料,采用电化学方法制取硫酸.装置如下 :

①电解质溶液中SO 离子向
离子向___ (填“A极”或“B极” )移动;
②请写出负极电极反应式__________ 。
③用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为____ ,析出银的质量______ g。
(2)我国科学家提出,用间接电化学法对大气污染物 NO 进行无害化处理 ,原理如下图:
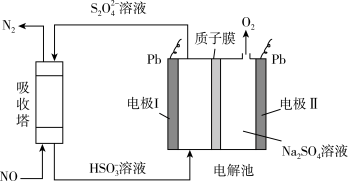
①吸收塔中发生的反应离子方程式为_____ 。
②电极I 的电极反应式为______ 。
③每处理2 molNO,电解池中产生标准状况下氧气的体积为__________ L。
(1)某兴趣小组以SO2为原料,采用电化学方法制取硫酸.装置如下 :

①电解质溶液中SO
 离子向
离子向②请写出负极电极反应式
③用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
(2)我国科学家提出,用间接电化学法对大气污染物 NO 进行无害化处理 ,原理如下图:

①吸收塔中发生的反应离子方程式为
②电极I 的电极反应式为
③每处理2 molNO,电解池中产生标准状况下氧气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“化学为了使生活更美好”。人们应用原电池原理制作了多种电池,以满足不同的需要。现有以下三种乙醇燃料电池。

(1)碱性乙醇燃料电池中,电极a上发生的电极反应式为_______ 。
(2)酸性乙醇燃料电池中,电极b上发生的电极反应式为_______ 。
(3)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极_______ 移动(填“a”或“b”),电极b上发生的电极反应式为_______ 。
(4)铅酸蓄电池放电时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。若电解液体积为2L(忽略溶液体积变化),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol·L-1下降到_______ mol·L-1。

(1)碱性乙醇燃料电池中,电极a上发生的电极反应式为
(2)酸性乙醇燃料电池中,电极b上发生的电极反应式为
(3)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极
(4)铅酸蓄电池放电时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。若电解液体积为2L(忽略溶液体积变化),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol·L-1下降到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将质量相等的锌片和铜片用导线相连浸入500 mL硫酸铜溶液中构成如图的装置。
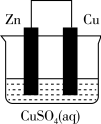
(1)此装置为___________ ,该装置中发生反应总的离子方程式为___________ ,铜片周围溶液会出现___________ 的现象。
(2)Cu电极是___________ (填“正极”或“负极”),写出其电极反应式___________ 。
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为___________ mol。

(1)此装置为
(2)Cu电极是
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)

a.碳棒 b.锌板 c.铜板 d.铝镁合金
这种电化学防腐方法称为_______ 。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的_______ 极,F电极上的电极反应式为_______ 。
②常温下,若用该燃料电池电解500mL饱和食盐水,当产生标准状况下1120mL气体时,溶液的pH为_______ 。(忽略电解前后溶液体积的变化)
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.碳棒 b.锌板 c.铜板 d.铝镁合金
这种电化学防腐方法称为
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的
②常温下,若用该燃料电池电解500mL饱和食盐水,当产生标准状况下1120mL气体时,溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按图进行电解实验(A、B、C、D均为惰性电极):

可供选择的电解质溶液列于表中:
要求满足的条件是:
①工作一段时间后甲中溶液的pH上升,乙中溶液的pH下降;
②B、C两极上放电的离子的物质的量相等。
(1)应选择的电解质溶液是________ 组。
(2)B极的电极反应式为_______ ;D极的电极反应式为_______ 。
(3)当B极上析出3.55g电解产物时,C极将析出______ (填物质名称)的质量为______ g。

可供选择的电解质溶液列于表中:
| 组别 | ① | ② | ③ | ④ |
| 甲烧杯 | NaOH溶液 | NaCl溶液 | H2SO4溶液 | AgNO3溶液 |
| 乙烧杯 | CuSO4溶液 | AgNO3溶液 | AgNO3溶液 | CuCl2溶液 |
要求满足的条件是:
①工作一段时间后甲中溶液的pH上升,乙中溶液的pH下降;
②B、C两极上放电的离子的物质的量相等。
(1)应选择的电解质溶液是
(2)B极的电极反应式为
(3)当B极上析出3.55g电解产物时,C极将析出
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。
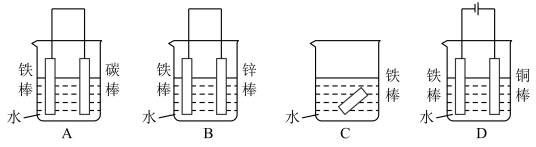
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的________ 极相连(写正或负),B电极的电极反应式是______ 。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为________ mol。
③电镀结束后CuSO4溶液的浓度______ (填变大,变小,不变)
④镀层破损后,铁不易被腐蚀的是___________ (填序号)。
A 镀铜铁 B 镀锌铁 C 镀锡铁
(1)下列哪个装置可防止铁棒被腐蚀
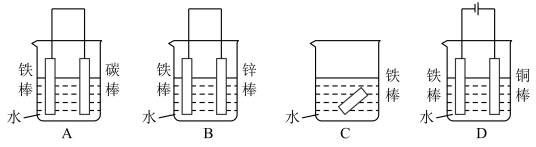
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为
③电镀结束后CuSO4溶液的浓度
④镀层破损后,铁不易被腐蚀的是
A 镀铜铁 B 镀锌铁 C 镀锡铁
您最近一年使用:0次



