将质量相等的锌片和铜片用导线相连浸入500 mL硫酸铜溶液中构成如图的装置。
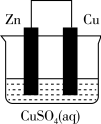
(1)此装置为___________ ,该装置中发生反应总的离子方程式为___________ ,铜片周围溶液会出现___________ 的现象。
(2)Cu电极是___________ (填“正极”或“负极”),写出其电极反应式___________ 。
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为___________ mol。

(1)此装置为
(2)Cu电极是
(3)若2 min后测得锌片质量减少13 g,则导线中流过的电子为
19-20高一下·广东梅州·期末 查看更多[2]
更新时间:2021-12-13 21:07:50
|
相似题推荐
【推荐1】Ⅰ.CO2作为化石燃料燃烧产生的废气,是主要的温室气体之一,使用电化学方法能够对CO2进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-CO2电池。其中一种Li-CO2电池的模型如下图所示:(图中 Li2CO3是固体)。

(1)下列有关该原电池的说法中,正确的是___________。
(2)给出该原电池的正极反应以及总反应。正极:___________ ;总反应:___________
(3)原电池中每转移1mol电子, 能够吸收___________ molCO2。
(4)若二氧化碳中混有氧气,那么在a电极上可能会出现的杂质是______ 。
Ⅱ.利用电解池,通过电化学还原,CO2能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸(HCOOH),该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
(5)在该装置中, 应该向___________ 极(填“阴”或“阳”)附近通入CO2气体。
(6)写出CO2在该电极上反应的电极反应式:___________ 。
(7)下列做法中,能够加快CO2吸收速率的是___________。
(8)当电极上生成5.6L(标准状况)的氧气时,生成甲酸的质量为________ g。

(1)下列有关该原电池的说法中,正确的是___________。
| A.该原电池工作时,电子由正极向负极移动 |
| B.在该原电池中,石墨作为负极 |
| C.原电池工作时,正离子一定向正极方向移动 |
| D.原电池工作时,b电极发生氧化反应 |
(3)原电池中每转移1mol电子, 能够吸收
(4)若二氧化碳中混有氧气,那么在a电极上可能会出现的杂质是
Ⅱ.利用电解池,通过电化学还原,CO2能够被还原为低价碳化合物。一种电化学还原二氧化碳的装置能够将二氧化碳还原为甲酸(HCOOH),该装置中,石墨作为阳极,单质银作为阴极,电解质溶液是硫酸溶液。
(5)在该装置中, 应该向
(6)写出CO2在该电极上反应的电极反应式:
(7)下列做法中,能够加快CO2吸收速率的是___________。
| A.适当增大电源电压 |
| B.适当降低电解液温度 |
| C.适当缩小两电极间距 |
| D.适当降低通入CO2的速度 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】正确认识和使用电池有利于我们每一个人的日常生活。电化学处理SO2是目前研究的热点,利用双氧水氧化吸收SO2是目前研究的热点。
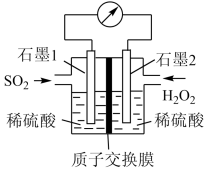
(1)反应的总化学方程式为___ ,正极的电极反应式为___ 。
(2)H+的迁移方向为由___ 到___ (填“左”或“右”)。
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为___ 。
(4)下列化学电池不易造成环境污染的是___ (填字母)。
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有___ (填序号)。
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极

(1)反应的总化学方程式为
(2)H+的迁移方向为由
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
(4)下列化学电池不易造成环境污染的是
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极
您最近一年使用:0次
【推荐1】(1)一种甲醇燃料电池以稀硫酸为电解质溶液,其中一个电极上加入甲醇(CH3OH),同时另一个电极通入空气:
①此电池的负极反应式是_________________________________ ;
②总反应方程式式是_____________________________________ ;
③电解质溶液中的H+向_____________ (填“甲醇”或“空气”)极移动。
(2)氯碱工业中,用惰性电极电解精制饱和食盐水
①电解总离子反应是____________________________________ ;
②阴极离子反应式是____________________________________ ;
③电解过程中阴极PH_____________ (填“增大”、“减小”或“不变”)
(3)碱性锌锰电池(负极Zn,正极MnO2,电解质溶液KOH溶液)
①总反应化学方程式是_______________________________________ ;
②负极反应是___________________________________________ 。
①此电池的负极反应式是
②总反应方程式式是
③电解质溶液中的H+向
(2)氯碱工业中,用惰性电极电解精制饱和食盐水
①电解总离子反应是
②阴极离子反应式是
③电解过程中阴极PH
(3)碱性锌锰电池(负极Zn,正极MnO2,电解质溶液KOH溶液)
①总反应化学方程式是
②负极反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一种高性能的碱性硼化钒( )—空气电池如下图所示,其中在
)—空气电池如下图所示,其中在 电极发生反应
电极发生反应
 。请回答下列问题:
。请回答下列问题:

(1)复合碳电极是_______ (填“正极”或者“负极”),此电极所发生的反应式为:_______ 。
(2)该电池在工作过程中,负极区溶液的pH_______ (填“降低”、“升高”或“不变”)。当外电路通过0.8mol电子时,消耗标准状况下 的体积为
的体积为_______ 。
(3)该电池的总反应式为:_______ 。
 )—空气电池如下图所示,其中在
)—空气电池如下图所示,其中在 电极发生反应
电极发生反应
 。请回答下列问题:
。请回答下列问题:
(1)复合碳电极是
(2)该电池在工作过程中,负极区溶液的pH
 的体积为
的体积为(3)该电池的总反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
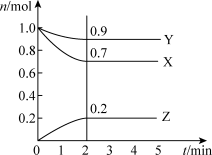
(1)该反应的化学方程式为_______ 。
(2)反应开始至2 min,用Y表示的平均反应速率为_______ 。
II.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(3)电解质溶液中 离子向
离子向_______ (填“A极”或“B极” )移动。
(4)请写出负极电极反应式_______ 。
(5)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为_______ ,析出银的质量_______ g。
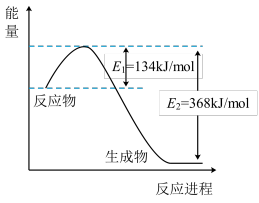
(6)如图是 1 mol NO2(g)和1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。请写出反应的热化学方程式_______ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,用Y表示的平均反应速率为
II.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(3)电解质溶液中
 离子向
离子向(4)请写出负极电极反应式
(5)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
(6)如图是 1 mol NO2(g)和1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。请写出反应的热化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铅蓄电池是典型的可充电电池,电池总反应式为:Pb+PbO2+2H2SO4  2PbSO4+2H2O。回答下列问题:
2PbSO4+2H2O。回答下列问题:

(1)放电时,负极为_______ 电极,试写出该电极的电极反应式是___________ 。电解液中H2SO4的浓度将变____________ 。(填“升高”、 “降低” 或“不变”)
(2)电池放电时,当外电路通过0.1 mol电子时,理论上负极板的质量增加________ g,电池中消耗的硫酸物质的量为_______ mol。
 2PbSO4+2H2O。回答下列问题:
2PbSO4+2H2O。回答下列问题:
(1)放电时,负极为
(2)电池放电时,当外电路通过0.1 mol电子时,理论上负极板的质量增加
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为 。
。
(1)放电时,正极的电极反应式:______ ,电解质溶液中硫酸的浓度______ (填“增大”“减小”或“不变”),当外电路通过1mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加______ g。
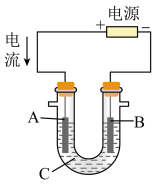
(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用______ 溶液,A电极的材料是______ ,B电极反应式是______ 。
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
 。
。(1)放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(1)丙装置中负极反应式为_________________ ,丁装置中负极反应式为__________________ 。
(2)电池的放电过程中,甲装置中溶液质量________ (填“增加”或“减少”);丁装置中溶液碱性________ (填“增强”或“减弱”)。
(3)当甲装置导线中转移0.3 mol电子时,正极生成气体________ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3 mol电子时,两电极质量相差________ g。


(1)丙装置中负极反应式为
(2)电池的放电过程中,甲装置中溶液质量
(3)当甲装置导线中转移0.3 mol电子时,正极生成气体
您最近一年使用:0次

 片作
片作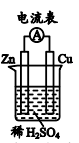
 片上发生反应的电极反应式为
片上发生反应的电极反应式为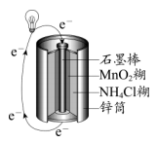
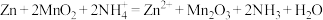
 发生氧化反应
发生氧化反应


