化学电池的发明,改变了人们的生活。
(1)如图所示装置中, 片作
片作___________ (填“正极”或“负极”)。
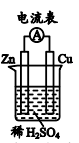
(2) 片上发生反应的电极反应式为
片上发生反应的电极反应式为___________ ;能证明化学能转化为电能的实验现象是:___________ 、铜片上产生大量气泡。
(3)常见的锌锰干电池构造示意图如下。
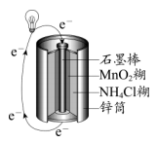
已知:电池的总反应为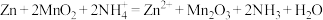
下列说法正确的是___________ (填字母)。
a.锌筒作负极
b. 发生氧化反应
发生氧化反应
(1)如图所示装置中,
 片作
片作
(2)
 片上发生反应的电极反应式为
片上发生反应的电极反应式为(3)常见的锌锰干电池构造示意图如下。

已知:电池的总反应为
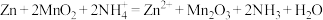
下列说法正确的是
a.锌筒作负极
b.
 发生氧化反应
发生氧化反应
更新时间:2023-05-23 22:17:33
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同___________ (填“相同”或“不相同”)。
(2)实验3中铝为___________ 极,电极反应式为___________ ;石墨为___________ 极,电极反应式为___________ ;电池总反应为(离子方程式)___________ 。
(3)实验4中铝为___________ 极,原因是___________ ;写出铝电极的电极反应式:___________ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同
(2)实验3中铝为
(3)实验4中铝为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为________ (填“原电池”“电解池”或“电镀池”),通入O2电极的电极反应式________ 。
(2)乙池中C(石墨)电极的名称为________ (填“正极”“负极”或“阴极”“阳极”),总反应的离子方程式为________ 。
(3)当乙池中D极质量增加10.8g时,甲池中理论上消耗O2的体积为___________ mL(标准状况),转移的电子数为___________ 。
(4)丙池中___________ (填“E”或“F”)极析出铜。
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将___________ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池中C(石墨)电极的名称为
(3)当乙池中D极质量增加10.8g时,甲池中理论上消耗O2的体积为
(4)丙池中
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】认真观察图中装置,回答下列问题:
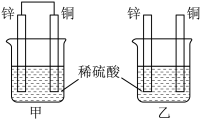
(1)下列说法中正确的是_________ (填序号)。
a.甲中铜片质量减少 b.乙中锌片质量减少
c.乙中铜片上没有明显变化 d.甲装置为原电池,乙装置为电解池
(2)同等条件下,两烧杯中产生气泡的速率:甲______ (填“>”“<”或“=”)乙。
(3)甲烧杯中锌电极为_______ (正极或负极),写出铜极的反应电极方程式_______ 。
(4)当甲中产生2.24 L(标准状况)气体时,理论上通过导线的电子数目为_______ mol。

(1)下列说法中正确的是
a.甲中铜片质量减少 b.乙中锌片质量减少
c.乙中铜片上没有明显变化 d.甲装置为原电池,乙装置为电解池
(2)同等条件下,两烧杯中产生气泡的速率:甲
(3)甲烧杯中锌电极为
(4)当甲中产生2.24 L(标准状况)气体时,理论上通过导线的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】探究原电池原理并应用原电池原理制作多种电池,对现实生活具有重要的意义。
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:
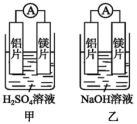
①甲、乙两装置工作时,电流计指针的偏转方向是否相同?_______ 。乙装置中负极的电极反应式是_______ 。
②根据上述实验结果分析,下列说法正确的是__________
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为_______ ;该电池充电时,其能量转化形式为_______ 。
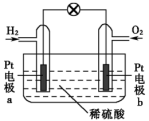
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:铂电极b上的电极反应式为_______ ,室温下,若该电池消耗1molH2时可提供电能257.4kJ的能量,则该燃料电池的能量转化率为_______ 。(已知:室温下,1molH2完全燃烧生成液态水时,释放286.0kJ的能量。)
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:

①甲、乙两装置工作时,电流计指针的偏转方向是否相同?
②根据上述实验结果分析,下列说法正确的是
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:铂电极b上的电极反应式为

您最近一年使用:0次
【推荐3】一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的 、
、 转化为
转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
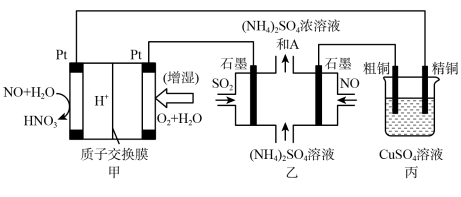
(1)燃料电池放电过程中负极的电极反应式___________ 。
(2)乙装置中物质A是___________ (填化学式),电解过程中阳极附近pH___________ (填“增大”“减小”或“不变”),阴极的电极反应式是___________ 。
(3)丙装置中如果粗铜中含有锌、银等杂质,则反应一段时间, 溶液的浓度将
溶液的浓度将___________ (填“增大”、“减小”或“不变”),若将两个电极材料改为石墨电极,则该电解池发生的离子方程式为___________ 。
(4)若在标准状况下,甲装置有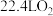 参加反应,则丙装置中阴极析出铜的质量为
参加反应,则丙装置中阴极析出铜的质量为___________  。
。
 、
、 转化为
转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
(1)燃料电池放电过程中负极的电极反应式
(2)乙装置中物质A是
(3)丙装置中如果粗铜中含有锌、银等杂质,则反应一段时间,
 溶液的浓度将
溶液的浓度将(4)若在标准状况下,甲装置有
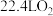 参加反应,则丙装置中阴极析出铜的质量为
参加反应,则丙装置中阴极析出铜的质量为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请仔细观察下列三种装置的构造示意图。根据要求回答问题:

(1)电解精炼铜(如图1)时,b极材料是________ (填“纯铜”或“粗铜”);其电解质溶液能否用CuCl2替代?答:________ (“能”或“否”)。
(2)碱性锌锰电池(如图2)的总反应式为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,该电池的负极反应式为______________________ 。若有0.65g锌参与了电池反应,则转移电子的物质的量为___________ mol。
(3)铅-硫酸蓄电池(如图3)放电过程中,负极的电极反应式为___________________ ,充电时,Pb电极应接电源的______ 极(填“正”或“负”)。

(1)电解精炼铜(如图1)时,b极材料是
(2)碱性锌锰电池(如图2)的总反应式为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,该电池的负极反应式为
(3)铅-硫酸蓄电池(如图3)放电过程中,负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据下表:
溶解度/(g/100g水)
(1)该电池的正极反应式为__________ 。
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过_____ 分离回收。
(3)用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入H2SO4和H2O2溶解,铁变为_____ ,加碱调节至pH为_____ 时,铁刚好完全沉淀(离子浓度小于1×10-5mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为_____ 时,锌开始沉淀(假定Zn2+浓度为0.1mol·L-1)。若上述过程不加H2O2,后果是______ ,原因是_____ 。
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 27.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Kap近似值 | 10-17 | 10-17 | 10-39 |
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过
(3)用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入H2SO4和H2O2溶解,铁变为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是____ ,负极发生的电极反应方程式为:____ 。若反应消耗32.5 g 负极材料,则电池中转移电子的数目为____ 。

(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____ 。
①上述反应可以在酸性条件下进行 ②上述反应不是可逆反应
③放电时正极金属Cd的质量增加 ④放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的_____ (填“正”或“负”)极,X极的电极反应方程为_______ 。

(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是

(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是①上述反应可以在酸性条件下进行 ②上述反应不是可逆反应
③放电时正极金属Cd的质量增加 ④放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的

您最近一年使用:0次

 如图
如图 ,则此原电池中锌电极上发生的是
,则此原电池中锌电极上发生的是 电子通过时,负极质量会变化
电子通过时,负极质量会变化 向
向


