正确认识和使用电池有利于我们每一个人的日常生活。电化学处理SO2是目前研究的热点,利用双氧水氧化吸收SO2是目前研究的热点。
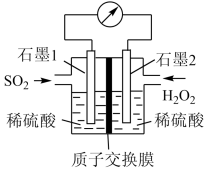
(1)反应的总化学方程式为___ ,正极的电极反应式为___ 。
(2)H+的迁移方向为由___ 到___ (填“左”或“右”)。
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为___ 。
(4)下列化学电池不易造成环境污染的是___ (填字母)。
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有___ (填序号)。
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极

(1)反应的总化学方程式为
(2)H+的迁移方向为由
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
(4)下列化学电池不易造成环境污染的是
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极
更新时间:2020-06-10 21:39:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
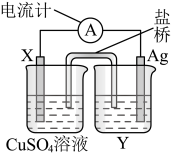
【推荐1】依据氧化还原反应:2Ag+(aq) +Cu(s) = Cu2+(aq) +2Ag(s)
设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是________ ;电解质溶液Y是___________ ;
(2)电极反应为: 正极:___________ 负极: ___________
(3)外电路中的电子是从_______ 电极流向________ 电极。
设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是
(2)电极反应为: 正极:
(3)外电路中的电子是从

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.“绿水青山就是金山银山”,利用电池原理治理污染是今后科研的重要课题。
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为_____ 极。
②请用离子方程式分析H2S气体去除的原理:___________ 。
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和 :
: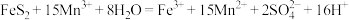 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
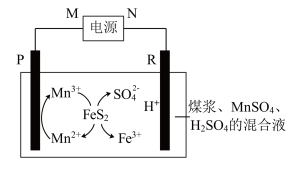
(2)电解池刚开始工作时,R上的电极反应式为_____ 。
(3)若电路中转移 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为_____ g(不考虑其他反应,下同),产生的气体的体积为______ L(已换算成标准状况)。
(4)电解过程中,混合溶液中的pH将_____ (填“变大”“变小”或“不变”),原因是___________ 。
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接_____ (填“M”或“N”)极。
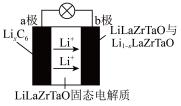
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为
②请用离子方程式分析H2S气体去除的原理:
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和
 :
: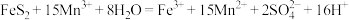 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
(2)电解池刚开始工作时,R上的电极反应式为
(3)若电路中转移
 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为(4)电解过程中,混合溶液中的pH将
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铝-空气电池是正在探索的车用新型电池。电池工作时,金属铝被氧化为 并形成
并形成 。空气中的氧气发生还原而生成
。空气中的氧气发生还原而生成 。
。
(1)写出铝-空气电池中的正、负极反应和总反应________ 。
(2)广泛采用铝-空气电池的好处有哪些?不足有哪些?就你的发现写出简要的报告,并预测其未来的应用前景________ 。
 并形成
并形成 。空气中的氧气发生还原而生成
。空气中的氧气发生还原而生成 。
。(1)写出铝-空气电池中的正、负极反应和总反应
(2)广泛采用铝-空气电池的好处有哪些?不足有哪些?就你的发现写出简要的报告,并预测其未来的应用前景
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
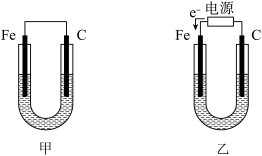
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________ 腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________ ;
②甲池铁棒腐蚀的速率比乙池铁棒_____ (填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________ ;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。

(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生
②甲池铁棒腐蚀的速率比乙池铁棒
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢氧燃料电池是的介色化学理的新型发电装置,下图为电池示意图,该电池电极表面镀一层细细的铂粉,吸附气体的能力强,性质稳定,请回答
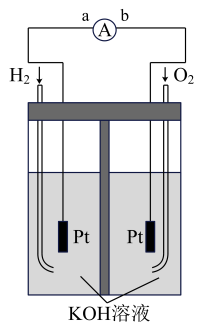
(1)氢氧燃料电量的转化形式是____ ,在导线中电子的流动方向为______ (用a,b表示)
(2)负极反应式为___________
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是______ ,反应II中的氧化剂是______
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为____ mol;将产生的电能用来电解饱和食盐水,产生的氢气体积(标准状况)为_____ L

(1)氢氧燃料电量的转化形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为原电池装置示意图。
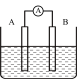
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是__ (填字母)。
A 铝片、铜片 B 铜片、铝片
C 铝片、铝片 D 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____ 。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:___ ;该电池在工作时,A电极的质量将_ (填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:_________ ;该电池在工作一段时间后,溶液的碱性将___ (填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:________ ;若该电池反应消耗了6.4克CH4,则转移电子的数目为__ 。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是
A 铝片、铜片 B 铜片、铝片
C 铝片、铝片 D 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)现有a.BaCl2 b.金刚石 c.NH4Cl d.Na2SO4 e.干冰 f.碘片六种物质,按下列要求回答(若有多个选项的,多选错选不给分):
①熔化时需要破坏共价键的是______ , 熔点最高的是_______ ,熔点最低的是_______ 。
②属于离子化合物的是________ ,只含有离子键的物质是________ ,含有两种化学键的物质是_________ ,含有分子间作用力的是__________ 。
(2)看下图回答下列问题
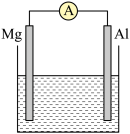
①若烧杯中溶液为稀硫酸,则观察到的现象是___________ ,负极反应式为___________ 。
②若烧杯中溶液为氢氧化钠溶液,则负极为_______ (填Mg或Al),总反应方程式为__________ 。
(1)现有a.BaCl2 b.金刚石 c.NH4Cl d.Na2SO4 e.干冰 f.碘片六种物质,按下列要求回答(若有多个选项的,多选错选不给分):
①熔化时需要破坏共价键的是
②属于离子化合物的是
(2)看下图回答下列问题

①若烧杯中溶液为稀硫酸,则观察到的现象是
②若烧杯中溶液为氢氧化钠溶液,则负极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)将Al片和Cu片用导线连接,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成原电池。写出插入稀NaOH溶液中形成原电池的负极反应________________ 。写出插入浓硝酸中形成原电池的正极反应______________ 。
(2)铅蓄电池是最常见的二次电池,由于其电压稳定、使用方便、安全可靠、价格低廉,所以在生产、生活中使用广泛,写出铅蓄电池放电时的正极反应______________________ ;充电时的阴极反应____________________ 。
(2)铅蓄电池是最常见的二次电池,由于其电压稳定、使用方便、安全可靠、价格低廉,所以在生产、生活中使用广泛,写出铅蓄电池放电时的正极反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】新型电池具有广阔的发展前景,根据所学知识回答下列问题:
(1)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如下图所示,写出放电过程中负极的电极反应式:___________ ,若过程中产生 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为___________ L。
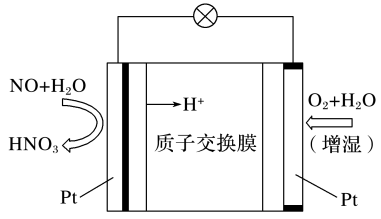
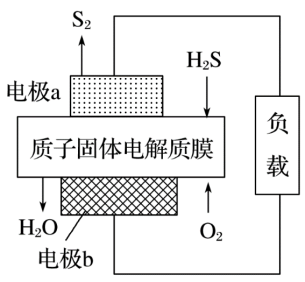
(2)科学家设计出质子膜 燃料电池,实现了利用
燃料电池,实现了利用 废气资源回收能量并得到单质破,质子膜
废气资源回收能量并得到单质破,质子膜 燃料电池的结构示意图如图所示,写出负极的电极反应式
燃料电池的结构示意图如图所示,写出负极的电极反应式___________ 。
(3)以 为燃料可以设计甲烷燃料电池,该电池以稀
为燃料可以设计甲烷燃料电池,该电池以稀 作电解质溶液,写出该电池正极电极反应式:
作电解质溶液,写出该电池正极电极反应式:___________
(1)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如下图所示,写出放电过程中负极的电极反应式:
 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为
(2)科学家设计出质子膜
 燃料电池,实现了利用
燃料电池,实现了利用 废气资源回收能量并得到单质破,质子膜
废气资源回收能量并得到单质破,质子膜 燃料电池的结构示意图如图所示,写出负极的电极反应式
燃料电池的结构示意图如图所示,写出负极的电极反应式
(3)以
 为燃料可以设计甲烷燃料电池,该电池以稀
为燃料可以设计甲烷燃料电池,该电池以稀 作电解质溶液,写出该电池正极电极反应式:
作电解质溶液,写出该电池正极电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】由铜片、锌片和200mL稀H2SO4组成的原电池中(如图所示装置),请按要求填空: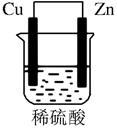
(1)______ 为正极,发生_______ 反应(“氧化”或“还原”),现象是________ ,电极反应式为_____________________ ;______ 为负极,发生_______ 反应(“氧化”或“还原”),现象是________ ,电极反应式为_____________________ 。
(2)H+向______ 极移动,电子流动方向为____ →导线→_____ (填电极材料)
(3)若锌片只发生电化学反应,则当铜片上共放出3.36L(标准状况)气体时,H2SO4恰好完全消耗。求:
①反应中消耗的锌的质量_____________
②有_______________ 个电子通过了导线.
③原稀H2SO4的物质的量浓度是________________

(1)
(2)H+向
(3)若锌片只发生电化学反应,则当铜片上共放出3.36L(标准状况)气体时,H2SO4恰好完全消耗。求:
①反应中消耗的锌的质量
②有
③原稀H2SO4的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是_______ (填字母)。
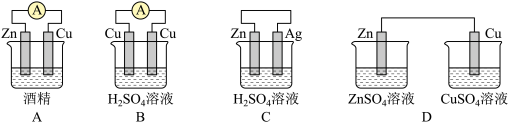
(2)该装置正极为_______ (填电极的化学式),写出该装置正极的电极反应式:_______ 。发生了_______ 反应(氧化或还原)。
(3)该装置溶液里的阴离子移向_______ 极(填电极的化学式)。
(4)若装置中转移了0.2mol电子,则理论上溶液增加的质量是_______ (写出具体过程)。
(1)下列装置中能够实现化学能转化为电能的是

(2)该装置正极为
(3)该装置溶液里的阴离子移向
(4)若装置中转移了0.2mol电子,则理论上溶液增加的质量是
您最近一年使用:0次

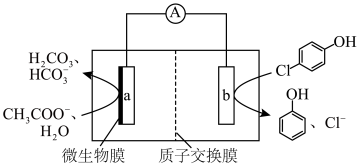
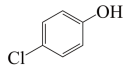 +2H++2e-=
+2H++2e-= +Cl-,经处理后的水样中要求对氯苯酚的含量小于mmol/L。若废水中对氯苯酚的含量是nmol/L,则处理1m3废水,至少添加CH3COO-的物质的量为
+Cl-,经处理后的水样中要求对氯苯酚的含量小于mmol/L。若废水中对氯苯酚的含量是nmol/L,则处理1m3废水,至少添加CH3COO-的物质的量为

