(1)现有a.BaCl2 b.金刚石 c.NH4Cl d.Na2SO4 e.干冰 f.碘片六种物质,按下列要求回答(若有多个选项的,多选错选不给分):
①熔化时需要破坏共价键的是
②属于离子化合物的是
(2)看下图回答下列问题
①若烧杯中溶液为稀硫酸,则观察到的现象是
②若烧杯中溶液为氢氧化钠溶液,则负极为
更新时间:2018-09-11 12:08:06
|
相似题推荐
填空题
|
适中
(0.65)
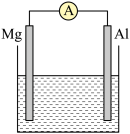
【推荐1】有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如下图所示:

(1)写出甲池中负极的电极反应式:_______ 。
(2)写出乙池中负极的电极材料和总反应的离子方程式:负极材料(化学式)_______ ;总反应的离子方程式_______ 。
(3)甲池溶液中阳离子的移动方向是_______ 。乙池外电路中电子的流动方向是_______ 。甲池中产生气泡的电极是_______ ;乙池外电路中电流的方向是_______ 。
(4)若甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出_______ 金属活动性更强,而乙会判断出_______ 金属活动性更强。
(5)由此实验,可得到如下哪些正确结论_______(填字母)。
(6)丙同学依据甲、乙同学的思路,设计如下实验:
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池,在这两个原电池中,负极分别为_______(填字母)。

(1)写出甲池中负极的电极反应式:
(2)写出乙池中负极的电极材料和总反应的离子方程式:负极材料(化学式)
(3)甲池溶液中阳离子的移动方向是
(4)若甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出
(5)由此实验,可得到如下哪些正确结论_______(填字母)。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序已过时,已没有实用价值 |
| D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析 |
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池,在这两个原电池中,负极分别为_______(填字母)。
| A.铝片、铜片 | B.铜片、铝片 | C.铝片、铝片 | D.铜片、铜片 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
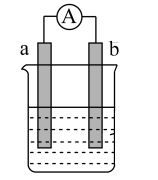
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为___ ,H+移向___ 极(填“a”或“b”)。
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入__ 极(填“a”或“b”)。
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是___ 。
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为___ mol。
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为__ g。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为________________________ 。放电一段时间后,负极附近溶液的pH________ (填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为________________________ 。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。_______

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
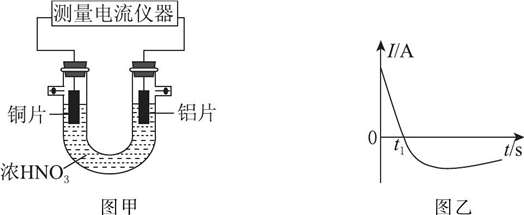
t1s前,原电池的负极是铝片,正极的电极反应式为____________ ,溶液中的H+向________ (填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是________________________ 。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

t1s前,原电池的负极是铝片,正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空:现有7个化学符号:18O;14C;32S8;23Na;14N;16O;1H2;12C60;32S2
(1)表示核素的符号共_______ 种;互为同位素的是_______ 和_______ 。
(2)互为同素异形体的是_______ 和_______ 。
(3)写出以下物质的电子式:PH3_______ ;CS2_______ 。
(4)2.2g铵根离子(14ND )的核外电子数是
)的核外电子数是_______ ;某单核微粒含有17个质子,20个中子,18个核外电子,则表示该粒子构成的化学符号是_______ 。
(5)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中由离子键和非极性共价键构成的物质是_______ (填序号,下同),属于共价化合物的是_______ 。
(1)表示核素的符号共
(2)互为同素异形体的是
(3)写出以下物质的电子式:PH3
(4)2.2g铵根离子(14ND
 )的核外电子数是
)的核外电子数是(5)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中由离子键和非极性共价键构成的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)已知甘氨酸的熔点是 233℃,而二苯胺的熔点只有 53℃,为什么甘氨酸的熔点高_______ 。
(2)相同条件下HF酸性比H2CO3强,请用一个化学方程式说明________ 。
(3)NF3的一种下游产品三聚氟氰(分子式为:C3N3F3),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式________ 。
(2)相同条件下HF酸性比H2CO3强,请用一个化学方程式说明
(3)NF3的一种下游产品三聚氟氰(分子式为:C3N3F3),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下面是同学们熟悉的物质:
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是_______ ;只含有离子键的是_______ ;既含有共价键又含有离子键的是_______ ;不存在化学键的是_______ ;电解质有_______ ;非电解质有_______ (填编号)
(2)NaHSO4在熔融状态下电离,破坏的化学键是_______ ,写出其电离方程式_______ 。
(3)写出②与⑨发生反应的化学方程式:_______ 。
(4)写出在稀溶液中⑥和⑩反应的离子方程式:_______ 。
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是
(2)NaHSO4在熔融状态下电离,破坏的化学键是
(3)写出②与⑨发生反应的化学方程式:
(4)写出在稀溶液中⑥和⑩反应的离子方程式:
您最近一年使用:0次



