回答下列问题:
(1)用28.4 g无水硫酸钠配制成500 mL溶液,其物质的量浓度为___________ mol·L-1;
(2)若从中取出50 mL,其物质的量浓度为___________ mol·L-1;溶质的质量为___________ g;
(3)若将这50 mL溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为___________ mol·L-1,SO 的物质的量浓度为
的物质的量浓度为___________ mol·L-1。
(1)用28.4 g无水硫酸钠配制成500 mL溶液,其物质的量浓度为
(2)若从中取出50 mL,其物质的量浓度为
(3)若将这50 mL溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为
更新时间:2021-11-04 15:56:01
|
【知识点】 物质的量浓度的计算
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室需要用容量瓶等仪器配制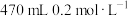 的NaCl溶液。
的NaCl溶液。
(1)配制上述NaCl溶液时,需利用托盘天平称取固体NaCl的质量为___________ g。
(2)以下操作会引起所配制溶液浓度偏低的是___________ ,偏高的是___________ 。(填序号)
a.未洗涤烧杯 b.容量瓶未烘干,底部有少量水
c.定容时俯视 d.定容摇匀后有溶液溅出
(3)现利用上述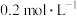 的NaCl溶液配制
的NaCl溶液配制 的NaCl溶液,需利用量筒量取
的NaCl溶液,需利用量筒量取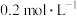 的NaCl溶液的体积为
的NaCl溶液的体积为___________ mL。
(4)某同学怀疑配制的NaCl溶液中可能混入了 ,可以利用
,可以利用___________ 的方法验证,证明存在 的实验现象为
的实验现象为___________ 。
(5)某工厂用电解NaCl溶液的方法制备氯气,其原理如下: ,请将此方程式补充完整
,请将此方程式补充完整___________ 。
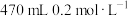 的NaCl溶液。
的NaCl溶液。(1)配制上述NaCl溶液时,需利用托盘天平称取固体NaCl的质量为
(2)以下操作会引起所配制溶液浓度偏低的是
a.未洗涤烧杯 b.容量瓶未烘干,底部有少量水
c.定容时俯视 d.定容摇匀后有溶液溅出
(3)现利用上述
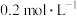 的NaCl溶液配制
的NaCl溶液配制 的NaCl溶液,需利用量筒量取
的NaCl溶液,需利用量筒量取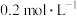 的NaCl溶液的体积为
的NaCl溶液的体积为(4)某同学怀疑配制的NaCl溶液中可能混入了
 ,可以利用
,可以利用 的实验现象为
的实验现象为(5)某工厂用电解NaCl溶液的方法制备氯气,其原理如下:
 ,请将此方程式补充完整
,请将此方程式补充完整
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】判断正误
1.取0.1 mol/L Na2CO3溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L______
2.把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度为1.5 mol·L-1______
3.把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%______
4.把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1______
5.把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%______
6.溶质的质量分数为w溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w______
7.将1 L 18.4 mol·L-1的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol·L-1______
8.V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1 倍,可将溶液加热浓缩到0.5 V L______
1.取0.1 mol/L Na2CO3溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L
2.把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度为1.5 mol·L-1
3.把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%
4.把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1
5.把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%
6.溶质的质量分数为w溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
7.将1 L 18.4 mol·L-1的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol·L-1
8.V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1 倍,可将溶液加热浓缩到0.5 V L
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】将4g铁粉与2.5g硫粉在研钵中充分混合后装入试管中,在试管口塞上带长导管的橡皮塞,并在导管末端放入一小团蘸有NaOH溶液的棉花,加热试管。


(1)写出铁与硫反应的化学方程式___________ 。
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜___________ 。
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式___________ 。
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为___________ 吨。已知98%的硫酸密度为1.84g/cm3,计算此溶液的物质的量浓度为___________ mol/L。


(1)写出铁与硫反应的化学方程式
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得质量分数为98%的浓硫酸为
您最近半年使用:0次



