题型:填空题
难度:0.85
引用次数:230
题号:14320754
用化学语言表达下列各微粒
(1)与氖原子电子层结构相同的-2价阴离子的电子式___________ 。
(2)第2层电子数为第1层、第3层电子数之和的原子的结构示意图___________ 。
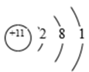
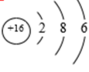
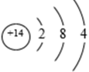
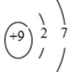
(3)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
A.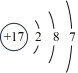 B.
B.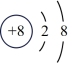 C.
C.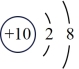 D.
D.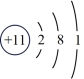 E.
E.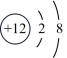
①属于离子结构示意图的是___________ (填编,下同)。
②属于金属元素的是___________ 。
③性质最稳定的原子是___________ ,最容易失去电子的原子是___________ ,最容易得到电子的原子是___________ 。
(1)与氖原子电子层结构相同的-2价阴离子的电子式
(2)第2层电子数为第1层、第3层电子数之和的原子的结构示意图
(3)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
A.
 B.
B.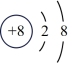 C.
C.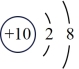 D.
D. E.
E.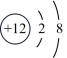
①属于离子结构示意图的是
②属于金属元素的是
③性质最稳定的原子是
21-22高一上·上海普陀·期中 查看更多[2]
更新时间:2021/11/08 21:55:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】填写下表中的空格:
| 微粒符号 | 质子数 | 中子数 | 质量数 | 核外电子数 | 电子式 | 结构示意图 |
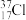 | 17 | |||||
| 9F- | 10 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表显示了元素周期表中的一部分。
请回答下列问题。
(1)硫元素的原子序数是_______ 。
(2)氟元素的原子结构示意图为_______ (填写字母)。
A.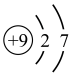 B.
B.
(3)镁元素在元素周期表的第_______ (填“二”或“三”)周期第_______ (填“ⅡA”或“ⅢA”)族。
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H_______ (填“<”或“>”)Na。
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是_______ (填“物理变化”或“化学变化”)。
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为_______ 。
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第一周期 | 1 H 氢 | 2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 | 4 Be 镀 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 第三周期1 | 1 Na 钠 | 12 Mg 镁 | 33 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 C 氯 | 18 Ar 氩 |
(1)硫元素的原子序数是
(2)氟元素的原子结构示意图为
A.
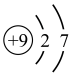 B.
B.
(3)镁元素在元素周期表的第
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】请回答下列问题:
(1)①氧化钙的化学式是___________ ;②钠离子的离子结构示意图___________ 。
(2)硫酸钠溶液与氯化钡溶液反应的离子方程式是___________ 。
(3)把一块绿豆大小的钠迅速投到热坩埚中,观察到的现象是___________ 。
(1)①氧化钙的化学式是
(2)硫酸钠溶液与氯化钡溶液反应的离子方程式是
(3)把一块绿豆大小的钠迅速投到热坩埚中,观察到的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
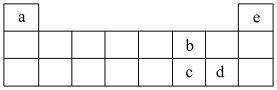
【推荐2】揭示物质结构的内部特征,有助我们更加准确的理解物质世界。下表是元素周期表的一部分,请回答有关问题。_____ 。
a.门捷列夫 b.道尔顿 c.汤姆生 d.凯库勒
(2)
①a和b化合形成生活中最常见的物质分子式为_____ 。
②上述分子中半径较小的是原子_____ (填元素符号)。
③上述原子结构示意图为_____ 。
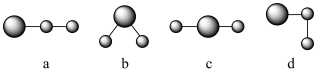
④该分子结构用球棍模型表示正确的是_____ 。
(3)上表中c元素在元素周期表中的位置是_____ ,其简单氢化物的电子式是_____ ,此氢化物的热稳定性比d元素的氢化物热稳定性_____ (填“强”或“弱”)。
a.门捷列夫 b.道尔顿 c.汤姆生 d.凯库勒
(2)

①a和b化合形成生活中最常见的物质分子式为
②上述分子中半径较小的是原子
③上述原子结构示意图为
④该分子结构用球棍模型表示正确的是
(3)上表中c元素在元素周期表中的位置是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图为元素周期表的一部分,请参照①-⑨在表中的位置,回答下列问题:(用元素符号或化学用语回答)
(1)由①②⑧三种元素形成的常见化合物的电子式为_____ ,其包含的化学键类型为_____ (填“离子键”、“共价键”)。
(2)⑦和⑨能以原子个数1:2形成化合物,用电子式表示其形成过程_____ 。
(3)金属性最强是_____ 。
(4)③的简单氢化物的沸点比⑦的简单氢化物的沸点_____ (填“高”或“低”),
(5)含氧酸酸性最强的是_____ 。(填分子式)
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
⑨ |
(1)由①②⑧三种元素形成的常见化合物的电子式为
(2)⑦和⑨能以原子个数1:2形成化合物,用电子式表示其形成过程
(3)金属性最强是
(4)③的简单氢化物的沸点比⑦的简单氢化物的沸点
(5)含氧酸酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】填空题。
(1)在①NaCl、②NaOH、③Na2O2、④N2、⑤H2S、⑥H2O2,只含有离子键的是__ ;只含有共价键的是__ ;既含有离子键,又含有共价键的是__ 。
(2)请用电子式表示NaCl的形成过程:___ 。
(3) N2的结构式为:__ ;H2O2的结构式为:__ 。
(4)写出下列微粒的电子式。
①CO2__ ;
②NH
___ 。
(1)在①NaCl、②NaOH、③Na2O2、④N2、⑤H2S、⑥H2O2,只含有离子键的是
(2)请用电子式表示NaCl的形成过程:
(3) N2的结构式为:
(4)写出下列微粒的电子式。
①CO2
②NH

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)碱金属元素原子最外层的电子都是_______ 个,在化学反应中它们容易失去_______ 个电子;卤族原子最外层的电子都是_______ 个,在化学反应中它们得到_______ 个电子。
(2)用电子式表示:N2_____________ ,CH4__________________ ,KCl_________
(2)用电子式表示:N2
您最近一年使用:0次