下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) △H=−57.3 kJ∙mol−1,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的△H |
| B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量。则Fe(s)+S(s)=FeS(s) △H=−95.6 kJ∙mol−1 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=−38.6 kJ∙mol−1 2NH3(g) △H=−38.6 kJ∙mol−1 |
| D.相同条件下,在两个相同的恒容密闭容器中,2molN2和6molH2反应放出的热量是1molN2和3molH2反应放出的热量的2倍 |
更新时间:2021-11-10 11:29:54
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】联氨(N2H4)常温下为无色液体,可用作火箭燃料。下列说法不正确的是
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)= N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=−1048.9 kJ·mol-1
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)= N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=−1048.9 kJ·mol-1
| A.ΔH4﹦2ΔH3−2ΔH2−ΔH1 |
B.O2(g)+2H2(g) 2H2O(l) ΔH5,ΔH5>ΔH3 2H2O(l) ΔH5,ΔH5>ΔH3 |
| C.1 mol O2(g)和 2 mol H2(g)具有的总能量高于 2 mol H2O(g) |
| D.联氨和 N2O4 作火箭推进剂的原因之一是反应放出大量的热且产物无污染 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.化学反应的反应热等于反应的焓变 |
| B.决定化学反应速率的主要因素是体系的温度 |
| C.对于需经过多个步骤的化学反应而言,活化能最小的那个步骤是决速步骤 |
| D.有气体参加的反应,压缩容器体积,单位体积内活化分子数增多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知 的氢气在足量氧气中燃烧生成
的氢气在足量氧气中燃烧生成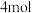 的液态水时,放出热量
的液态水时,放出热量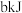 ,下列热化学方程式书写正确的是
,下列热化学方程式书写正确的是
 的氢气在足量氧气中燃烧生成
的氢气在足量氧气中燃烧生成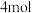 的液态水时,放出热量
的液态水时,放出热量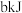 ,下列热化学方程式书写正确的是
,下列热化学方程式书写正确的是A.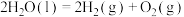  |
B.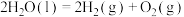 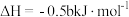 |
C.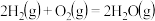 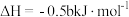 |
D.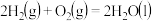 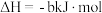 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】完全燃烧5.6L标准状况下的 ,冷却至室温放出222.4kJ热量,下列热化学方程式正确的是
,冷却至室温放出222.4kJ热量,下列热化学方程式正确的是
 ,冷却至室温放出222.4kJ热量,下列热化学方程式正确的是
,冷却至室温放出222.4kJ热量,下列热化学方程式正确的是A.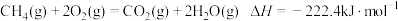 |
B.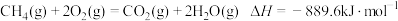 |
C.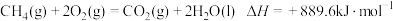 |
D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关中和热的说法正确的是
| A.在测定中和热时,使用稀醋酸代替稀盐酸,所测中和热数值偏大 |
| B.1mol硫酸与1molBa(OH)2完全中和所放出的热量为中和热 |
| C.在测定中和热时,用铜质搅拌棒代替环形玻璃搅拌棒,对测定结果无影响 |
| D.在测定中和热时,分多次将NaOH溶液加入盐酸中,所测中和热数值偏小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
| A.新制氯水具有漂白性,故无法测定其pH值 |
| B.中和热测定实验中,应迅速将稀的NaOH溶液和稀的盐酸在测定装置中混合 |
| C.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2ml 5% H2O2和lmL FeCl3溶液,观察并比较实验现象 |
| D.已知4H++4I-+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol·L-1 KI溶液、0.1 mol·L-1稀硫酸外,还需要用到淀粉溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】人体内葡萄糖的消耗可用下列热化学方程式表示:C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(1) △H=-2800.6kJ•mol-1;如果某人每天消耗12540kJ热量,则他每天至少相当于要摄入葡萄糖的质量约为
| A.700g | B.806g | C.1000g | D.1250g |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】火箭发射时可用肼(N2H4)为燃料和NO2作氧化剂,这两者反应生成氮气和水蒸气。
已知:
N2 (g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol
则1摩尔气体肼和NO2完全反应时放出的热量为
已知:
N2 (g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol
则1摩尔气体肼和NO2完全反应时放出的热量为
| A.100.3kJ | B.567.85kJ | C.500.15kJ | D.601.7kJ |
您最近一年使用:0次
【推荐3】在298K、101kPa下,将4.4gCO2通入150mL1mol·L-1KOH溶液中充分反应(不考虑气体逸出),测得反应放出akJ的热量,已知该条件下,0.5molCO2通入1L1mol·L-1KOH溶液中充分反应放出bkJ的热量。则下列表示CO2与KOH溶液反应生成KHCO3溶液的热化学方程式书写正确的是
| A.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(5b-a)kJ·mol-1 |
| B.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(5a-4b)kJ·mol-1 |
| C.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-(20b-a)kJ·mol-1 |
| D.CO2(g)+KOH(aq)=KHCO3(aq) ∆H=-2(10a-b)kJ·mol-1 |
您最近一年使用:0次

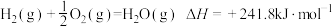

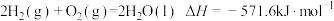

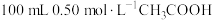 溶液与
溶液与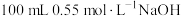 溶液混合,温度从25.0℃升高到27.7℃。下列说法错误的是
溶液混合,温度从25.0℃升高到27.7℃。下列说法错误的是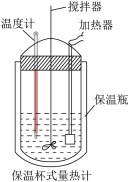
 偏大
偏大 溶液完全被中和
溶液完全被中和

