按要求填空
(1)Cr2O 的颜色是
的颜色是___________ 。
(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式___________ 。
(1)Cr2O
 的颜色是
的颜色是(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式
更新时间:2021-11-29 15:19:03
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)已知H2、CO、CH4的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1、890.3kJ·mol-1。
①相同条件下,等质量的H2、CO、CH4分别完全燃烧,放出热量最多的是_______ 。
②2CH4(g)+3O2(g)=2CO(g)+4H2O(l) ΔH=_______ kJ·mol-1。
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a_______ 途径b(填“>”、“<”或“=”)
途径a:CH4 CO+H2
CO+H2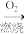 CO2+H2O
CO2+H2O
途径b:CH4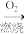 CO2+H2O
CO2+H2O
(2)已知白磷(P4)和P4O6的分子结构和部分化学键的键能分别如下图、表所示:

①写出白磷与氧气反应生成P4O6固体的热化学方程式:_______ 。
②已知P4(白磷,s)=4P(红磷,s)ΔH=-16.7kJ·mol-1.等质量的白磷、红磷分别完全燃烧,放出热量更多的是_______ 。
(1)已知H2、CO、CH4的燃烧热分别为285.8kJ·mol-1、283.0kJ·mol-1、890.3kJ·mol-1。
①相同条件下,等质量的H2、CO、CH4分别完全燃烧,放出热量最多的是
②2CH4(g)+3O2(g)=2CO(g)+4H2O(l) ΔH=
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a
途径a:CH4
 CO+H2
CO+H2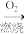 CO2+H2O
CO2+H2O途径b:CH4
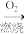 CO2+H2O
CO2+H2O(2)已知白磷(P4)和P4O6的分子结构和部分化学键的键能分别如下图、表所示:

| 化学键 | P-P | O=O | P-O |
| 键能(kJ·mol-1) | a | b | c |
②已知P4(白磷,s)=4P(红磷,s)ΔH=-16.7kJ·mol-1.等质量的白磷、红磷分别完全燃烧,放出热量更多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】北京时间2021年10月16日,搭载神舟十三号载人飞船的长征二号F遥十三运载火箭,在酒泉卫星发射中心发射成功。
(1)我国使用的推进器主要是以液体火箭推进器为主,推进器以液态偏二甲肼和四氧化二氮为主要燃料,其反应方程式为C2H8N2(l)+2N2O4(l) 3N2(g)+2CO2(g)+4H2O(l)。根据以下热化学方程式求出该热化学方程式的焓变△H=
3N2(g)+2CO2(g)+4H2O(l)。根据以下热化学方程式求出该热化学方程式的焓变△H=_____ 。
①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) △H1=a kJ∙mol−1
②N2(g)+O2(g)=2NO(g) △H2=b kJ∙mol−1
③2NO(g)+O2(g)=N2O4(l) △H3=c kJ∙mol−1
(2)因偏二甲肼和四氧化二氮有剧毒且价格昂贵,逐渐被其它燃料替代。如肼(N2H4)和强氧化剂过氧化氢(H2O2)反应产生大量N2和H2O,并放出大量热。已知:1.28g液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,放出25.6kJ的热量。则该反应的热化学方程式:_____ 。
(3)液氧甲烷火箭发动机是介于液氧煤油和液氧液氢之间的一个选择,其燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=−802.3 kJ∙mol−1,根据以下信息,求算C=O的键能:_____ 。
(1)我国使用的推进器主要是以液体火箭推进器为主,推进器以液态偏二甲肼和四氧化二氮为主要燃料,其反应方程式为C2H8N2(l)+2N2O4(l)
 3N2(g)+2CO2(g)+4H2O(l)。根据以下热化学方程式求出该热化学方程式的焓变△H=
3N2(g)+2CO2(g)+4H2O(l)。根据以下热化学方程式求出该热化学方程式的焓变△H=①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) △H1=a kJ∙mol−1
②N2(g)+O2(g)=2NO(g) △H2=b kJ∙mol−1
③2NO(g)+O2(g)=N2O4(l) △H3=c kJ∙mol−1
(2)因偏二甲肼和四氧化二氮有剧毒且价格昂贵,逐渐被其它燃料替代。如肼(N2H4)和强氧化剂过氧化氢(H2O2)反应产生大量N2和H2O,并放出大量热。已知:1.28g液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,放出25.6kJ的热量。则该反应的热化学方程式:
(3)液氧甲烷火箭发动机是介于液氧煤油和液氧液氢之间的一个选择,其燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=−802.3 kJ∙mol−1,根据以下信息,求算C=O的键能:
| 共价键 | C-H | O=O | H-O |
| 键能(kJ∙mol−1) | 413 | 498 | 464 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在1.01×105 Pa时,16 g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S燃烧的热化学方程式为: ____________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知水的比热容为4.18×10-3kJ•(g•℃)-1,10g硫磺在O2中完全燃烧生成气态SO2,放出的热量能量使500gH2O温度由18℃升至62.4℃,则硫磺的燃烧热为___________ ,热化学方程式为___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.按要求书写热化学方程式
(1)一定条件下,由 SO2和CO反应生成 S 和 CO2的能量变化如图所示,写出该反应的热化学方程式_______

(2)已知 H2O(g)=H2O(l) ΔH= -44 kJ∙mol−1
则表示氢气燃烧热的热化学方程式为___________
Ⅱ.根据下列图示回答相关问题:

(1)写出 Fe(OH)2被空气中的氧气氧化生成 Fe(OH)3的方程式___________ 。
(2)将 FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得 Fe(OH)3胶体,写出制取 Fe(OH)3胶体反应的离子方程式:___________ ,区分 FeCl3溶液、Fe(OH)3胶体的实验操作名称为___________ 。
Ⅲ.磷化氢(PH3)是粮食储备常用的高效熏蒸杀虫剂,下图为制备 PH3的流程。

(1)次磷酸属于___________ 元酸。
(2)白磷和烧碱溶液反应的化学方程式为:___________ 。
(3)若起始时有 1 mol P4参加反应,则整个工业流程中共生成___________ mol PH3。
(1)一定条件下,由 SO2和CO反应生成 S 和 CO2的能量变化如图所示,写出该反应的热化学方程式

(2)已知 H2O(g)=H2O(l) ΔH= -44 kJ∙mol−1
| 化学键 | O=O(g) | H—H | H—O |
| 键能/(kJ·mol-1) | 496 | 436 | 463 |
则表示氢气燃烧热的热化学方程式为
Ⅱ.根据下列图示回答相关问题:

(1)写出 Fe(OH)2被空气中的氧气氧化生成 Fe(OH)3的方程式
(2)将 FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得 Fe(OH)3胶体,写出制取 Fe(OH)3胶体反应的离子方程式:
Ⅲ.磷化氢(PH3)是粮食储备常用的高效熏蒸杀虫剂,下图为制备 PH3的流程。

(1)次磷酸属于
(2)白磷和烧碱溶液反应的化学方程式为:
(3)若起始时有 1 mol P4参加反应,则整个工业流程中共生成
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】4.0 g硫粉在O2中完全燃烧生成SO2,放出37 kJ热量,计算S的燃烧热?___________
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】乙炔( )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
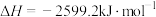 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热__________ ?

 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
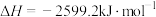 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求完成填空。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:_______ ;又已知H2O(l)=H2O(g) ΔH=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______ kJ。
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2 2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是
2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是_______ 。
(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:_______ 。若1g水蒸气转化成液态水放热2.444kJ,写出表示氢气燃烧热的热化学方程式: _______ 。
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为_______ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______ 。
(1)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水放出649.5kJ热量,其热化学方程式为:
(2)已知H—H键键能为436kJ·mol-1,H—N键键能为391kJ·mol-1,根据化学方程式:N2+3H2
 2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是
2NH3 ΔH=-92.4kJ·mol-1,则N≡N键键能是(3)1mol氧气与足量氢气反应生成水蒸气放热483.6kJ,写出该反应的热化学方程式:
(4)含11.2gKOH的稀溶液与1L0.1mol·L-1的H2SO4溶液反应放出11.46kJ的热量,该离子反应的热化学方程式为
(5)已知:①C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3=+141kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
【推荐1】回答下列问题
(1)白磷与氧可发生如下反应: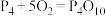 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O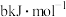 、P=O
、P=O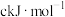 、O=O
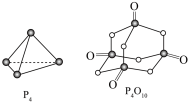
、O=O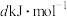 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为_______ 。
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为_______ 。
(3)氮氧化物能破坏臭氧层: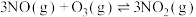

_______ 。
已知:反应Ⅰ: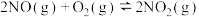
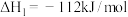
反应Ⅱ: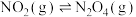
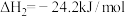
反应Ⅲ: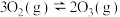
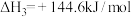
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①

②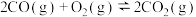

③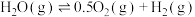

则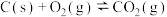

_______ ( 、
、 、
、 表示)。
表示)。
(1)白磷与氧可发生如下反应:
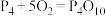 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O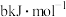 、P=O
、P=O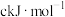 、O=O
、O=O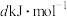 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为
(3)氮氧化物能破坏臭氧层:
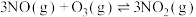

已知:反应Ⅰ:
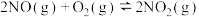
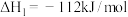
反应Ⅱ:
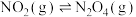
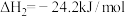
反应Ⅲ:
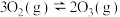
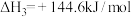
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①


②
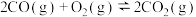

③
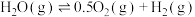

则
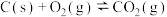

 、
、 、
、 表示)。
表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图1是反应A(g)+3B(g) 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。

(1)由示意图知,反应物的总能量____ (填“>”、“<”或“=”)生成物的总能量,此反应中反应物的总键能____ (填“>”、“<”或“=”)生成物的总键能。
(2)a=____ (用Ec和Ec′表示)。
(3)加入催化剂对该反应的ΔH____ 影响(填“有”或“无”)。
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:_____ 。
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:_____ 。
 2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
2C(g) ΔH=-akJ•mol-1在反应过程中的能量变化关系图,回答下列问题。
(1)由示意图知,反应物的总能量
(2)a=
(3)加入催化剂对该反应的ΔH
(4)已知:
2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-akJ•mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=-bkJ•mol-1;
H2O(g)=H2O(l) ΔH3=-ckJ•mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为:
(5)工业上用H2(g)和Cl2(g)反应制HCl(g),各键能为H-H:436kJ/mol,Cl-Cl:243kJ/mol,H-Cl:431kJ/mol。该反应的热化学方程式是
(6)298K时,0.5molC2H4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出表示C2H4(g)燃烧热的热化学方程式:
您最近一年使用:0次
【推荐3】生物天然气是一种生物质能,它是由秸秆、杂草等废弃物经微生物发酵后产生的,主要成分为 。回答下列问题:
。回答下列问题:
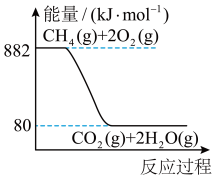
(1)甲烷燃烧时的能量变化如图所示。下列说法正确的是_______ (填字母)。
A.甲烷是一种清洁能源
B.甲烷完全燃烧时,化学能全部转化为热能
C.该反应的热化学方程式为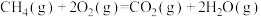
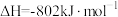
(2)若1mol水蒸气转化为液态水放热44kJ,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(3)利用 催化还原
催化还原 ,可消除氮氧化物的污染。
,可消除氮氧化物的污染。
已知:①
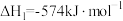
②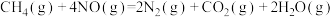

若 将
将 还原为
还原为 ,整个过程中放出的热量为867kJ,则
,整个过程中放出的热量为867kJ,则
_______ 。
(4)甲烷可用于生产合成气,其反应为
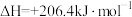 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:
则a=_______ 。
 。回答下列问题:
。回答下列问题:
(1)甲烷燃烧时的能量变化如图所示。下列说法正确的是
A.甲烷是一种清洁能源
B.甲烷完全燃烧时,化学能全部转化为热能
C.该反应的热化学方程式为
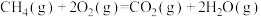
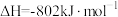
(2)若1mol水蒸气转化为液态水放热44kJ,则表示
 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)利用
 催化还原
催化还原 ,可消除氮氧化物的污染。
,可消除氮氧化物的污染。已知:①

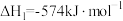
②
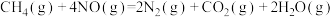

若
 将
将 还原为
还原为 ,整个过程中放出的热量为867kJ,则
,整个过程中放出的热量为867kJ,则
(4)甲烷可用于生产合成气,其反应为

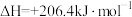 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:| 化学键 |  |  |  |  |
键能/ | 436 | 465 | a | 1076 |
您最近一年使用:0次



