生物天然气是一种生物质能,它是由秸秆、杂草等废弃物经微生物发酵后产生的,主要成分为 。回答下列问题:
。回答下列问题:
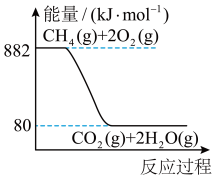
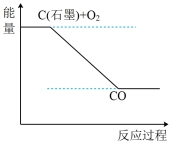
(1)甲烷燃烧时的能量变化如图所示。下列说法正确的是_______ (填字母)。
A.甲烷是一种清洁能源
B.甲烷完全燃烧时,化学能全部转化为热能
C.该反应的热化学方程式为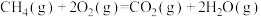
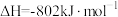
(2)若1mol水蒸气转化为液态水放热44kJ,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(3)利用 催化还原
催化还原 ,可消除氮氧化物的污染。
,可消除氮氧化物的污染。
已知:①
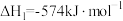
②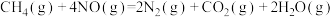

若 将
将 还原为
还原为 ,整个过程中放出的热量为867kJ,则
,整个过程中放出的热量为867kJ,则
_______ 。
(4)甲烷可用于生产合成气,其反应为
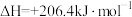 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:
则a=_______ 。
 。回答下列问题:
。回答下列问题:
(1)甲烷燃烧时的能量变化如图所示。下列说法正确的是
A.甲烷是一种清洁能源
B.甲烷完全燃烧时,化学能全部转化为热能
C.该反应的热化学方程式为
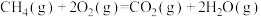
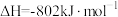
(2)若1mol水蒸气转化为液态水放热44kJ,则表示
 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)利用
 催化还原
催化还原 ,可消除氮氧化物的污染。
,可消除氮氧化物的污染。已知:①

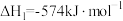
②
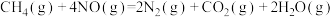

若
 将
将 还原为
还原为 ,整个过程中放出的热量为867kJ,则
,整个过程中放出的热量为867kJ,则
(4)甲烷可用于生产合成气,其反应为

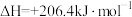 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:| 化学键 |  |  |  |  |
键能/ | 436 | 465 | a | 1076 |
更新时间:2022-11-11 20:47:56
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】热化学方程式的书写
书写表示燃烧热的热化学方程式时,以燃烧_____ 可燃物为标准来配平其余物质的化学计量数,同时可燃物要完全燃烧且生成_____ 。例如:H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
书写表示燃烧热的热化学方程式时,以燃烧
 O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求填空
(1)Cr2O 的颜色是
的颜色是___________ 。
(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式___________ 。
(1)Cr2O
 的颜色是
的颜色是(2)已知:16.0g甲烷气体完全燃烧生成液态水放出的热量为890.3kJ(298K、1.01×105Pa时测定)。写出该条件下,甲烷燃烧的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求写出下列反应的热化学方程式。
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为_____________________
(2)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1 mol CuCl(s),放热444 kJ,该反应的热化学方程式是_____________________
(3)LiH可作飞船的燃料,已知下列反应
①2Li(s)+H2(g)=2LiH(s) △H= −182 kJ/mol;②2H2(g)+O2(g)=2H2O(l) △H= −572 kJ/mol ③4Li(s)+O2(g)=2Li2O(s) △H= −1196 kJ/mol
试写出25℃、101kPa下,LiH在O2中燃烧的热化学方程式______________
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为
(2)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1 mol CuCl(s),放热444 kJ,该反应的热化学方程式是
(3)LiH可作飞船的燃料,已知下列反应
①2Li(s)+H2(g)=2LiH(s) △H= −182 kJ/mol;②2H2(g)+O2(g)=2H2O(l) △H= −572 kJ/mol ③4Li(s)+O2(g)=2Li2O(s) △H= −1196 kJ/mol
试写出25℃、101kPa下,LiH在O2中燃烧的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求回答下列问题:
(1)已知下列物质电离平衡常数
①次氯酸的电离方程式为___________ 。
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为___________ 。
③下列实验事实不能证明醋酸是弱酸的是___________ 。
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是___________ 。
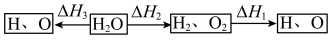
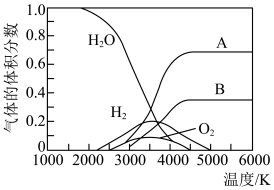
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是___________ 。等物质的量的A、H2相比,化学能较低的物质是___________ 。
(1)已知下列物质电离平衡常数
| 化学式 | HF |  |  |  |
| 电离平衡常数 | 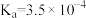 |  | 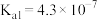  | 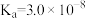 |
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为
③下列实验事实不能证明醋酸是弱酸的是
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是
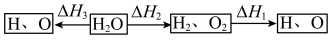
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是

您最近一年使用:0次
【推荐3】H2O2在Fe2+、Cu2+的存在下生成具有强氧化性的·OH(羟基自由基),·OH可将有机物氧化降解。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+ O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-1
2CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=________ kJ·mol-1。
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为_______ 。
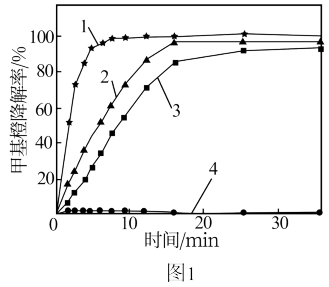
实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
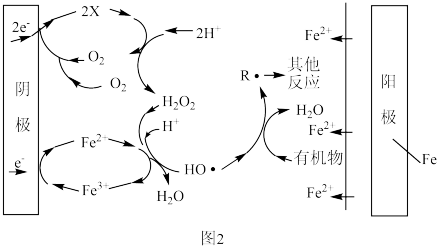
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为______ ,X微粒的化学式为________ ,阴极附近Fe2+参与反应的离子方程式为_______ 。
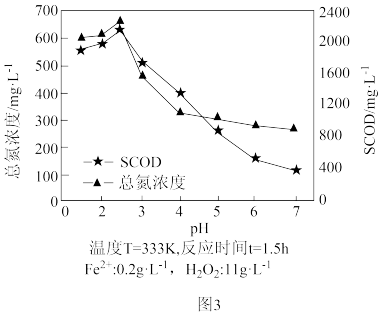
(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是__________ 。
(1)Cu2+-H2O2体系中存在下列反应:
Cu2+(aq)+H2O2(aq)= CuOOH+(aq)+H+(aq) ΔH1=a kJ·mol-1
CuOOH+(aq)=Cu+(aq)+·OH(aq)+
 O2(g) ΔH2=b kJ·mol-1
O2(g) ΔH2=b kJ·mol-12CuOOH+(aq)=2Cu+(aq)+H2O2(aq)+O2(g) ΔH3=c kJ·mol-1
则H2O2(aq)=2·OH(aq) ΔH=
(2)为探究Fe2+-Cu2+-H2O2能够协同催化氧化降解甲基橙,某研究小组的实验结果如图1所示。得出“Fe2+-Cu2+-H2O2催化氧化降解甲基橙效果优于单独加入Fe2+或Cu2+”结论的证据为

实验条件:200 mL甲基橙模拟废水(1.5 g·L-1,pH=3.0),温度60 ℃、V(H2O2)=2.0 mL
1—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0.4
2—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0.02∶0
3—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0.4
4—V(H2O2)∶m(FeSO4)∶m(CuSO4)=2∶0∶0
(3)EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图2所示。阳极的电极反应式为

(4)SCOD是指溶解性化学需氧量,是衡量水中有机物质含量多少的指标。水体SCOD越大,说明其有机物含量越高。用Fe2+-H2O2法氧化破解啤酒工业污泥中的微生物,释放出有机物和氮等。测得不同初始pH下污泥经氧化破解后上层清液中的SCOD及总氮浓度如图3所示。当pH>2.5时,总氮浓度、SCOD均降低,其原因可能是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】完成下列问题。
(1)汽车尾气主要含有一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一、已知汽缸中氮气和氧气反应生成一氧化氮的能量变化值如图所示,则由该反应生成1molNO时,应_________ (填“释放”或“吸收”) ________ kJ能量。

(2)用氮化硅( )陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下: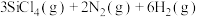
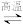
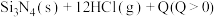 ,完成下列填空:
,完成下列填空:
①写出 的电子式:
的电子式:___________ 。
②在一定温度下进行上述反应,若反应容器的容积为2L,3min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率___________ 。
③一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是___________ 。
a. b.容器内压强保持不变
b.容器内压强保持不变
c.混合气体密度保持不变 d.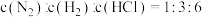
(3)CO2/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。 研究 HCOOH燃料电池性能的装置如图所示,两电极区间用允许K+、H+通过的半透膜隔开。
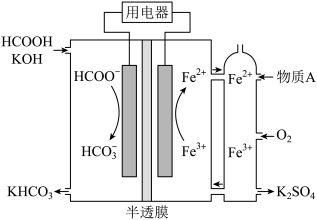
①电池负极电极反应式为___________ ;放电过程中需补充的物质A为___________ (填化学式)。
②图中所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为___________ 。
(1)汽车尾气主要含有一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一、已知汽缸中氮气和氧气反应生成一氧化氮的能量变化值如图所示,则由该反应生成1molNO时,应

(2)用氮化硅(
 )陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下: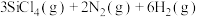
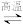
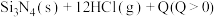 ,完成下列填空:
,完成下列填空:①写出
 的电子式:
的电子式:②在一定温度下进行上述反应,若反应容器的容积为2L,3min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率
③一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.混合气体密度保持不变 d.
(3)CO2/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。 研究 HCOOH燃料电池性能的装置如图所示,两电极区间用允许K+、H+通过的半透膜隔开。

①电池负极电极反应式为
②图中所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氨气是一种重要的化学物质,可用于制取化肥和硝酸,也可用于燃料电池等。
(1)工业合成氨的热化学方程式为:
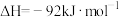
表中a为_______ 。
(2)合成氨原料中的 可用CO在高温下与水蒸气反应制得。已知在25℃、101kPa下:
可用CO在高温下与水蒸气反应制得。已知在25℃、101kPa下:
Ⅰ.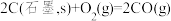
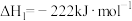
Ⅱ.
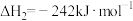
Ⅲ.

①25℃、101kPa下CO与水蒸气反应转化为 的热化学方程式为
的热化学方程式为_______ 。
②根据反应Ⅰ、Ⅱ、Ⅲ,下列说法正确的是_______ (填选项字母)。
a.由反应Ⅱ可以推知:
 ,则
,则 小于
小于
b.反应III的反应热等于 分子中化学键断裂时所吸收的总能量与
分子中化学键断裂时所吸收的总能量与 分子中化学键形成时所释放的总能量的差
分子中化学键形成时所释放的总能量的差
c.如图可表示反应Ⅰ的反应过程和能量的关系
(3)以氨气代替氢气研发氨燃料电池是当前科研的一个热点,氨燃料电池使用的电解质溶液是 的KOH溶液,生成的产物无污染。以此燃料电池,采用电解法制备
的KOH溶液,生成的产物无污染。以此燃料电池,采用电解法制备 ,装置如图所示。
,装置如图所示。
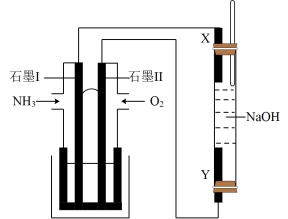
①石墨Ⅰ电极上的电极反应式为_______ 。
②Y电极的电极材料是_______ 。
③通电一段时间后,若右侧玻璃管中产生 白色沉淀,理论上石墨Ⅱ上通入
白色沉淀,理论上石墨Ⅱ上通入 的体积至少为
的体积至少为_______ L(标准状况下)。
(1)工业合成氨的热化学方程式为:

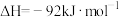
| 化学键 |  |  |  |
| 断开1mol化学键需要吸收的能量/kJ | a | 436 | 946 |
表中a为
(2)合成氨原料中的
 可用CO在高温下与水蒸气反应制得。已知在25℃、101kPa下:
可用CO在高温下与水蒸气反应制得。已知在25℃、101kPa下:Ⅰ.
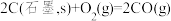
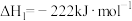
Ⅱ.

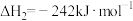
Ⅲ.


①25℃、101kPa下CO与水蒸气反应转化为
 的热化学方程式为
的热化学方程式为②根据反应Ⅰ、Ⅱ、Ⅲ,下列说法正确的是

a.由反应Ⅱ可以推知:

 ,则
,则 小于
小于
b.反应III的反应热等于
 分子中化学键断裂时所吸收的总能量与
分子中化学键断裂时所吸收的总能量与 分子中化学键形成时所释放的总能量的差
分子中化学键形成时所释放的总能量的差c.如图可表示反应Ⅰ的反应过程和能量的关系
(3)以氨气代替氢气研发氨燃料电池是当前科研的一个热点,氨燃料电池使用的电解质溶液是
 的KOH溶液,生成的产物无污染。以此燃料电池,采用电解法制备
的KOH溶液,生成的产物无污染。以此燃料电池,采用电解法制备 ,装置如图所示。
,装置如图所示。
①石墨Ⅰ电极上的电极反应式为
②Y电极的电极材料是
③通电一段时间后,若右侧玻璃管中产生
 白色沉淀,理论上石墨Ⅱ上通入
白色沉淀,理论上石墨Ⅱ上通入 的体积至少为
的体积至少为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态。
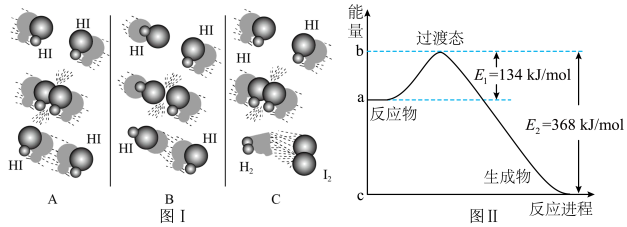
⑴图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是______(选填“A”、“B”或“C”);
⑵图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的
热化学方程式:___________________________________;
⑶下表是部分化学键的键能数据:
已知白磷的燃烧热为2982kJ/mol,白磷(P4)、P4O6、P4O10结构如下图所示,
则上表中X=_______________。
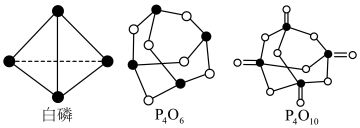
⑷0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为___________kJ。

⑴图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是______(选填“A”、“B”或“C”);
⑵图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的
热化学方程式:___________________________________;
⑶下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/ kJ·mol–1 | 198 | 360 | 498 | X |
则上表中X=_______________。

⑷0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为___________kJ。
您最近一年使用:0次

 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
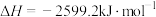 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热


