乙炔( )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
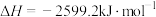 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热__________ ?

 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
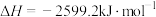 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热
更新时间:2022-11-24 17:19:41
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ΔH=﹣570
②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6
③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8
④C(s)+O2(g)=CO2(g)ΔH=﹣393.5
回答下列问题:
(1)上述反应中属于吸热反应的是___________ 。(填写序号)。
(2)H2的燃烧热为___________ 。
(3)燃烧10 g H2生成液态水,放出的热量为___________ 。
(4)CO的燃烧热的热化学方程式为:___________ 。
①2H2(g)+O2(g)=2H2O(l) ΔH=﹣570

②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6

③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8

④C(s)+O2(g)=CO2(g)ΔH=﹣393.5

回答下列问题:
(1)上述反应中属于吸热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)CO的燃烧热的热化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】适量 (g)在1mol
(g)在1mol (g)中完全燃烧,生成2mol
(g)中完全燃烧,生成2mol (l),放出571.6kJ的热量。请写出表示
(l),放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式___________ 。
 (g)在1mol
(g)在1mol (g)中完全燃烧,生成2mol
(g)中完全燃烧,生成2mol (l),放出571.6kJ的热量。请写出表示
(l),放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为_______ 。
(2)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式_______ 。
(3)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式_______ 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是_______ 。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(2)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式
(3)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是
您最近一年使用:0次
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)实验测得,5g甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则甲醇的燃烧热ΔH=___________ 。
(2)今有如下两个热化学方程式:则a___________ b(填>,=,<)
H2(g)+ O2(g)=H2O(g) ΔH1=akJ·mol -1
O2(g)=H2O(g) ΔH1=akJ·mol -1
H2(g)+ O2(g)=H2O(l) ΔH2=bkJ·mol -1
O2(g)=H2O(l) ΔH2=bkJ·mol -1
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g) 2NH3(g) △H=a kJ·mol -1 。试根据表中所列键能数据估算a的值:
2NH3(g) △H=a kJ·mol -1 。试根据表中所列键能数据估算a的值:___________ 。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol -1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol -1
2C2H2(g)+5O2(g)=4CO2(g)+2H 2O(l) △H3=-2599kJ·mol -1
根据盖斯定律,计算298K时由C(s)和H2(g)生成1molC2H2(g)反应的反应热△H=___________ 。
(1)实验测得,5g甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则甲醇的燃烧热ΔH=
(2)今有如下两个热化学方程式:则a
H2(g)+
 O2(g)=H2O(g) ΔH1=akJ·mol -1
O2(g)=H2O(g) ΔH1=akJ·mol -1 H2(g)+
 O2(g)=H2O(l) ΔH2=bkJ·mol -1
O2(g)=H2O(l) ΔH2=bkJ·mol -1(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g)
 2NH3(g) △H=a kJ·mol -1 。试根据表中所列键能数据估算a的值:
2NH3(g) △H=a kJ·mol -1 。试根据表中所列键能数据估算a的值:| 化学键 | H-H | N-H | N≡N |
| 键能/kJ/mol | 436 | 391 | 945 |
已知:C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol -1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol -1
2C2H2(g)+5O2(g)=4CO2(g)+2H 2O(l) △H3=-2599kJ·mol -1
根据盖斯定律,计算298K时由C(s)和H2(g)生成1molC2H2(g)反应的反应热△H=
您最近一年使用:0次

 的燃烧热为
的燃烧热为 ,则
,则
 。
。 ,若将这些甲醇完全燃烧生成二氧化碳气体和液态水,放出
,若将这些甲醇完全燃烧生成二氧化碳气体和液态水,放出 热量,则甲醇的燃烧热为
热量,则甲醇的燃烧热为 丁烷完全燃烧生成二氧化碳气体和液态水时,放出
丁烷完全燃烧生成二氧化碳气体和液态水时,放出 热量。根据上述信息写出表示丁烷燃烧热的热化学方程式:
热量。根据上述信息写出表示丁烷燃烧热的热化学方程式:

