依据事实,写出下列反应的热化学方程式。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为_______ 。
(2)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式_______ 。
(3)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式_______ 。
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是_______ 。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(2)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式
(3)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式
(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是
更新时间:2022-08-18 08:17:44
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知C、H2、CO发生燃烧反应时的反应热数据如下表所示:
(1)写出C完全燃烧的热化学方程式:____________________________________ 。
(2)现以H2或CO为燃料来提供热能,从热能的角度考虑,你认为应该选择________ (填写序号)。A.H2 B.CO C.均可以
理由是________________________________________ 。
| 物质 | C | H2 | CO |
| ΔH/(kJ·mol-1) | -393.5 | -285.8 | -283.0 |
(1)写出C完全燃烧的热化学方程式:
(2)现以H2或CO为燃料来提供热能,从热能的角度考虑,你认为应该选择
理由是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)根据如图所示情况,判断下列说法中正确的是____ 。
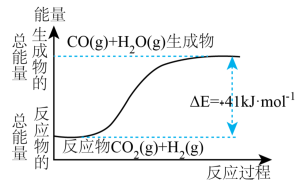
A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) △H=41kJ•mol﹣1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为△H2,则△H2>△H
(2)25℃、101kPa下,已知1g氢气完全燃烧生成液态水时放出142.9kJ的热量,表示氢气燃烧热的热化学方程式是_____ 。
(3)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为:__ (用含△H1、△H2、△H3的式子表示)。
(4)已知反应2HI(g)⇌H2(g)+I2(g)的△H=+11kJ•mol﹣1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___ kJ。

A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) △H=41kJ•mol﹣1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为△H2,则△H2>△H
(2)25℃、101kPa下,已知1g氢气完全燃烧生成液态水时放出142.9kJ的热量,表示氢气燃烧热的热化学方程式是
(3)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为:
(4)已知反应2HI(g)⇌H2(g)+I2(g)的△H=+11kJ•mol﹣1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ΔH=-570 kJ/mol
②2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ/mol
③2CO(g)=2C(s)+O2(g) ΔH=+220.8 kJ/mol
④2C(s)+2O2(g)=2CO2(g) ΔH=-787 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是___________ (填写序号)。
(2)H2的燃烧热为___________ 。
(3)燃烧10 g H2生成液态水,放出的热量为___________ 。
(4)C(s)的燃烧热的热化学方程式为___________ 。
(5)已知:1 L1 mol/LH2SO4溶液与2 L1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为___________ 。
①2H2(g)+O2(g)=2H2O(l) ΔH=-570 kJ/mol
②2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ/mol
③2CO(g)=2C(s)+O2(g) ΔH=+220.8 kJ/mol
④2C(s)+2O2(g)=2CO2(g) ΔH=-787 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)C(s)的燃烧热的热化学方程式为
(5)已知:1 L1 mol/LH2SO4溶液与2 L1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】50 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液在简易量热计中进行中和反应。通过测定反应过程中所放出的热量可计算中和热ΔH。回答下列问题:
(1)该实验中往往用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度的作用是_______ ,当室温低于10 ℃时进行,对实验结果会造成较大的误差,原因是_______ 。
(2)实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_______ (填“相等”或“不相等”),理由是_______ 。
(3)若50 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液的密度都约为1 g·mL-1,起始温度都为T1,反应后最高温度为T2,计算中和热ΔH_______ 。
(1)该实验中往往用0.50 mol·L-1HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度的作用是
(2)实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热
(3)若50 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1NaOH溶液的密度都约为1 g·mL-1,起始温度都为T1,反应后最高温度为T2,计算中和热ΔH
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cρV总△T计算获得。
(1)盐酸浓度的测定:移取20.00mL特测液,加入指示利,用0.500mol/LNaOH溶液滴定至终点消耗NaOH溶液22.00mL。该盐酸浓度为_____ mol/L。
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,则该过程放出的热量为_____ J(c和ρ分别取4.18J/g·℃和1.0g/mL,忽略水以外各物质吸收的热量,下同)。
(3)借鉴(2)的方法,甲同学测量放热反应Fe(s)+CuSO4 (aq)=FeSO4(aq)+Cu(s)的焓变△H(忽略温度对焓变的影响,下同)。实验结果见如表。
①温度:b_____ c(填“>”“<”或“=”)。
②△H=_____ (选择表中一组数据计算)。结果表明,该方法可行。
(4)乙同学也借鉴(2)的方法,测量反应A:Fe(s)+Fe2(SO4)3(aq)=3FeSO4(aq)的焓变。
查阅资料:配制Fe2(SO4)3溶液时需加入酸。加酸的目的是抑制Fe3+水解。
提出猜想:Fe粉与Fe2(SO4)3溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
验证猜想:用pH试纸测得Fe2(SO4)3溶液的pH不大于1;向少量Fe2(SO4)3溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和_____ (用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为_____ 。
(5)化学能可转化为热能,写出其在生产或生活中的一种应用_____ 。
(1)盐酸浓度的测定:移取20.00mL特测液,加入指示利,用0.500mol/LNaOH溶液滴定至终点消耗NaOH溶液22.00mL。该盐酸浓度为
(2)热量的测定:取上述NaOH溶液和盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,则该过程放出的热量为
(3)借鉴(2)的方法,甲同学测量放热反应Fe(s)+CuSO4 (aq)=FeSO4(aq)+Cu(s)的焓变△H(忽略温度对焓变的影响,下同)。实验结果见如表。
| 反应试剂 | 体系温度/℃ | |||
| 反应前 | 反应后 | |||
| ⅰ | 0.20mol/LCuSO4溶液100mL | 1.20gFe粉 | A | b |
| ⅱ | 0.56gFe粉 | a | C | |
②△H=
(4)乙同学也借鉴(2)的方法,测量反应A:Fe(s)+Fe2(SO4)3(aq)=3FeSO4(aq)的焓变。
查阅资料:配制Fe2(SO4)3溶液时需加入酸。加酸的目的是抑制Fe3+水解。
提出猜想:Fe粉与Fe2(SO4)3溶液混合,在反应A进行的过程中,可能存在Fe粉和酸的反应。
验证猜想:用pH试纸测得Fe2(SO4)3溶液的pH不大于1;向少量Fe2(SO4)3溶液中加入Fe粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为
(5)化学能可转化为热能,写出其在生产或生活中的一种应用
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)写出Al和氢氧化钾溶液反应的化学方程式___________ 。
(2)比较结合OH-能力的相对强弱:Al3+___________  (填“>”“<”或“=”),用一个离子方程式说明
(填“>”“<”或“=”),用一个离子方程式说明___________ 。
(3)实验测得,1g H2(g)完全燃烧生成液态水时放出142.9 kJ的热量,则氢气燃烧的热化学方程式为___________ 。
(4)常温下,氨气极易溶于水的原因是___________ 。
(2)比较结合OH-能力的相对强弱:Al3+
 (填“>”“<”或“=”),用一个离子方程式说明
(填“>”“<”或“=”),用一个离子方程式说明(3)实验测得,1g H2(g)完全燃烧生成液态水时放出142.9 kJ的热量,则氢气燃烧的热化学方程式为
(4)常温下,氨气极易溶于水的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】依据事实写出下列反应的热化学方程式:
(1)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量_______
(2)1molC(石墨,s)与适量H2O(g)完全反应生成CO(g)和H2(g),吸收131.3KJ热量;_______
(3)25℃,101KPa条件下,1g甲醇燃烧生成CO2(g)和H2O(l)放热22.68KJ,则甲醇的燃烧热的热方程式为_______
(1)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量
(2)1molC(石墨,s)与适量H2O(g)完全反应生成CO(g)和H2(g),吸收131.3KJ热量;
(3)25℃,101KPa条件下,1g甲醇燃烧生成CO2(g)和H2O(l)放热22.68KJ,则甲醇的燃烧热的热方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.化学反应在发生物质变化的同时伴随着能量变化,请回答下列问题:
(1)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是___________ ,图中对应反应的热化学方程式为___________ 。 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。
已知25℃,101 时:
时:
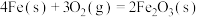
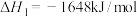


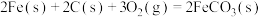
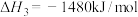
则

___________ 。
Ⅱ.某实验小组设计用0.55 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。___________ ,装置中还存在的错误有___________ ;大烧杯杯口若不盖泡沫塑料板,测得中和反应的反应热 将
将___________ (填“偏大”、“偏小”或“无影响”)。
(4)实验中,所用 稍过量的原因是
稍过量的原因是___________ 。
(5)该实验小组做了三次实验,每次取盐酸和 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:
已知盐酸、 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
___________ 。(保留到小数点后1位)
(1)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是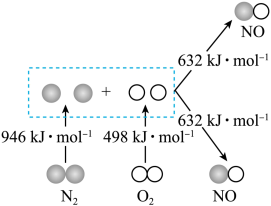
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。已知25℃,101
 时:
时: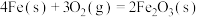
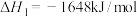


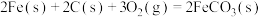
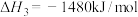
则


Ⅱ.某实验小组设计用0.55
 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。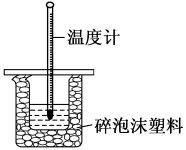
 将
将(4)实验中,所用
 稍过量的原因是
稍过量的原因是(5)该实验小组做了三次实验,每次取盐酸和
 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温差 /℃ /℃ | ||
| 盐酸 |  溶液 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.0 | 2.9 |
 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。回答下列问题:
(1)已知298K时,白磷、红磷完全燃烧的热化学方程式如下:
P4(白磷,s)+5O2(g)=P4O10(s) △H1=-2983.2kJ•mol-1
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) △H2=-738.5kJ•mol-1
P4O10(s) △H2=-738.5kJ•mol-1
则该温度下,白磷转化为红磷的热化学方程式为___ 。
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) △H=-1638kJ•mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为___ ,反应过程中放出的热量为___ kJ(保留2位小数)。
(1)已知298K时,白磷、红磷完全燃烧的热化学方程式如下:
P4(白磷,s)+5O2(g)=P4O10(s) △H1=-2983.2kJ•mol-1
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) △H2=-738.5kJ•mol-1
P4O10(s) △H2=-738.5kJ•mol-1则该温度下,白磷转化为红磷的热化学方程式为
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) △H=-1638kJ•mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
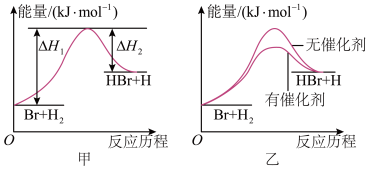
【推荐3】(1)根据反应Br+H2⇌HBr+H的能量对反应历程的示意图甲进行判断,该反应为_______ 反应(填“吸热”或“放热”)
(2)常温下0.01mol·L-1 NaOH溶液的pH=_______ 。
(3)已知下列反应:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+ O2(g)=H2O(l) ΔH3=-285.8kJ/mol
O2(g)=H2O(l) ΔH3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的反应热为ΔH=_______ kJ/mol

(2)常温下0.01mol·L-1 NaOH溶液的pH=
(3)已知下列反应:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
③H2(g)+
 O2(g)=H2O(l) ΔH3=-285.8kJ/mol
O2(g)=H2O(l) ΔH3=-285.8kJ/mol则反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的反应热为ΔH=
您最近一年使用:0次

 时,
时, 燃烧生成
燃烧生成 放热
放热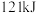 ,
,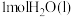 蒸发吸热
蒸发吸热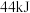 ,表示
,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为

