对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,一定有 |
B.加入盐酸酸化的氯化钡溶液有白色沉淀产生,一定有 |
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有 |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定含有Ca2+ |
更新时间:2021-11-17 10:20:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案、现象、结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向待测液中滴加NaOH浓溶液,微热,再将湿润的红色石蕊试纸靠近试管口 | 红色石蕊试纸变蓝 | 待测液一定是铵盐溶液 |
| B | 用铂丝蘸取某溶液进行焰色试验,观察火焰颜色 | 火焰呈黄色 | 溶液中存在钠盐 |
| C | 取少许久置的Na2SO3粉末配成溶液,滴加盐酸酸化的BaCl2溶液 | 有气泡和白色沉淀产生 | Na2SO3粉末部分变质 |
| D | 向Na2SO3溶液和盐酸反应后的溶液中加入紫色石蕊试液 | 溶液变红 | 说明盐酸已经过量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】a、b、c、d、e为原子序数依次增大的五种常见短周期元素,可组成一种化合物A,其化学式为ba4d(ec4)2。A能够发生如下转化关系:
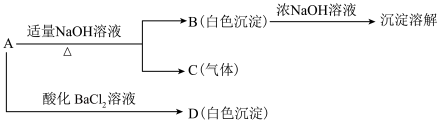
已知C的分子式为ba3,能使湿润的红色石蕊试纸变蓝。则下列说法正确的是

已知C的分子式为ba3,能使湿润的红色石蕊试纸变蓝。则下列说法正确的是
| A.原子半径b>c |
| B.e的氧化物的水化物为强酸 |
| C.化合物A为共价化合物 |
| D.元素非金属性强弱c<e |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列根据实验现象所得出的结论中,正确的是( )
| A.向某晶体的溶液中加入SCN-后溶液无明显变化,当滴加几滴氯水后,溶液出现红色。结论:该晶体中一定含有Fe3+ |
| B.无色试液加入NaOH溶液、加热,产生的气体使湿润的红色石蕊实质变蓝。结论:试液中一定含有NH4+ |
| C.无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊。结论:原溶液一定含有CO32- |
| D.无色溶液中加入BaCl2溶液有白色沉淀产生,再加稀盐酸,沉淀不消失。结论:原溶液一定含有SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】粗盐中除 外,还含有
外,还含有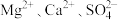 以及泥沙等杂质。粗盐提纯的操作流程如下:
以及泥沙等杂质。粗盐提纯的操作流程如下:
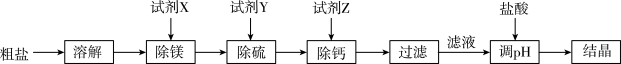
下列说法正确的是
 外,还含有
外,还含有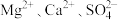 以及泥沙等杂质。粗盐提纯的操作流程如下:
以及泥沙等杂质。粗盐提纯的操作流程如下:
下列说法正确的是
A.试剂 分别为过量的 分别为过量的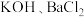 和 和 |
B.为确认 是否完全沉淀,可向上层清液中继续滴加 是否完全沉淀,可向上层清液中继续滴加 溶液 溶液 |
| C.“结晶”方式为蒸发浓缩、冷却结晶 |
D.滤液中含有的阴离子有两种: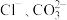 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验结论正确的是( )
| A.向某溶液中加入稀盐酸,产生无色无味的气体,将该气体通入澄清石灰水中,石灰水变浑浊,证明该溶液中一定含有CO32- |
| B.向某溶液中加入稀硝酸和硝酸银溶液,产生白色沉淀,证明该溶液中一定含有Cl- |
| C.向某溶液中加入CCl4,CCl4层显紫色,证明该溶液中存在I- |
| D.向某溶液中加入氯化钡溶液,有白色沉淀产生,再加入稀盐酸,沉淀不消失,则该溶液中含有SO42- |
您最近一年使用:0次
【推荐1】根据下列实验操作及现象,所得实验结论正确的是
| 实验操作及现象 | 实验结论 | |
| A | 用某物质的溶液进行焰色实验,焰色反应为黄色 | 该物质中一定含Na+ |
| B | 向某溶液中加入几滴H2O2溶液,再向溶液中加入2滴KSCN溶液,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO |
| D | 向某溶液中加入足量盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有CO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某溶液中可能存在I-、CO32-、SO32-、Al3+、Cl-、K+ 等六种离子中的某几种。现取该溶液进行实验,得到如下现象:实验1:向溶液中滴加足量氯水后,溶液变黄色,且有无色气体逸出;实验2:向所得黄色溶液中加CCl4萃取后,取水层滴加AgNO3溶液,出现白色沉淀;实验3:向实验1所得溶液中加入足量BaCl2溶液,无沉淀生成。根据上面的操作和现象推断,下列说法正确的是
| A.溶液中一定存在I-、CO32-,不存在Al3+、SO32- |
| B.溶液变黄色时发生反应的离子方程式为I-+Cl2== I+2Cl- |
| C.产生的无色气体中一定有CO2,可能有SO2 |
| D.溶液中一定存在K+,可能存在Al3+、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外活动小组的同学从某地颗粒采集器中获得雾霾颗粒样品,然后用蒸馏水浸取。在探究雾霾颗粒可溶性成分的实验中,下列根据实验现象得出的结论错误的是( )
| A.向浸取液中滴入硝酸酸化后,加入AgNO3溶液有白色沉淀产生,说明雾霾中一定含有Cl- |
| B.向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有NH4+ |
| C.向浸取液中加入Cu和浓H2SO4,试管口有红棕色气体产生,说明雾霾中可能含有NO3- |
| D.向浸取液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,说明雾霾中一定含SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】通过实验得出的以下结论中,正确的是
| A.将某固体试样完全溶于盐酸,无明显现象,再滴加BaCl2溶液,出现白色沉淀,则该固体试样中存在SO42- |
| B.将该固体试样完全溶于盐酸,产生无色气体,该气体能使澄清石灰水变浑浊,则该固体试样中一定存在CO32- |
| C.将某固体加水完全溶解,滴加氢氧化钠溶液,没有产生使湿润的红色石蕊试纸变蓝的气体,该固体试样中仍可能存在NH4+ |
| D.将某固体进行焰色反应实验,透过蓝色钴玻璃观察得火焰呈紫色,则该固体中不存在Na+ |
您最近一年使用:0次

 通入
通入 溶液②
溶液② 溶液③
溶液③ ④新制氯水⑤
④新制氯水⑤



