高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 。
。

请回答下列问题:
(1)写出D的名称___________ ,E的俗称___________ 。Na2FeO4中Fe元素的化合价为___________ 。
(2)写出反应②的离子方程式:___________ 。
(3)反应③,F在A中点燃的反应现象为:___________ 。
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:_____
2 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O
(5)写出反应⑤的化学方程式:___________ 。
 。
。
请回答下列问题:
(1)写出D的名称
(2)写出反应②的离子方程式:
(3)反应③,F在A中点燃的反应现象为:
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:
2
 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O(5)写出反应⑤的化学方程式:
更新时间:2021-11-20 20:39:48
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: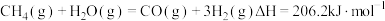
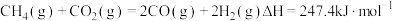
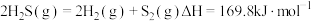
(1) 热分解制氢时常向反应器中通入一定比例空气,使部分
热分解制氢时常向反应器中通入一定比例空气,使部分 燃烧,其目的是
燃烧,其目的是___________ 。燃烧生成的 与
与 进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为
进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为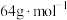 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(2) 的热分解也可得到
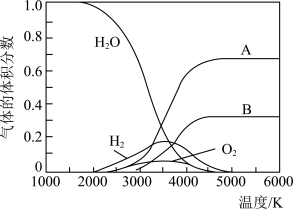
的热分解也可得到 ,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是___________ 。
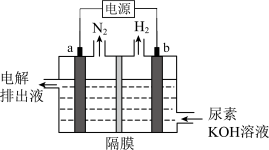
(3)电解尿素 的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为___________ 。
(4)镁铝合金(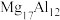 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为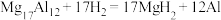 。得到的混合物
。得到的混合物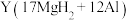 在一定条件下释放出氢气。
在一定条件下释放出氢气。
①熔炼制备镁铝合金(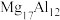 )时通入氩气的目的是
)时通入氩气的目的是___________ 。
②在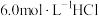 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。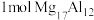 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为___________ 。
③在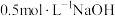 和
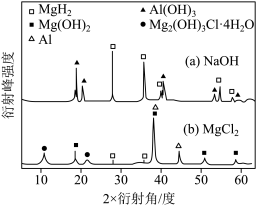
和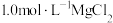 溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述
溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述 溶液中,混合物Y中产生氢气的主要物质是
溶液中,混合物Y中产生氢气的主要物质是_________ 。(填化学式)。
已知:
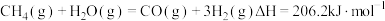
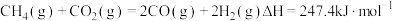
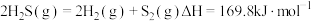
(1)
 热分解制氢时常向反应器中通入一定比例空气,使部分
热分解制氢时常向反应器中通入一定比例空气,使部分 燃烧,其目的是
燃烧,其目的是 与
与 进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为
进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为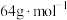 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)
 的热分解也可得到
的热分解也可得到 ,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
(3)电解尿素
 的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
(4)镁铝合金(
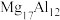 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为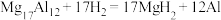 。得到的混合物
。得到的混合物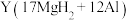 在一定条件下释放出氢气。
在一定条件下释放出氢气。①熔炼制备镁铝合金(
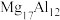 )时通入氩气的目的是
)时通入氩气的目的是②在
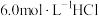 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。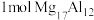 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为③在
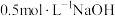 和
和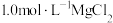 溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述
溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述 溶液中,混合物Y中产生氢气的主要物质是
溶液中,混合物Y中产生氢气的主要物质是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】某电子厂腐蚀废液含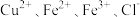 ,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得
,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得 溶液,请根据以下流程图,回答下列问题。
溶液,请根据以下流程图,回答下列问题。
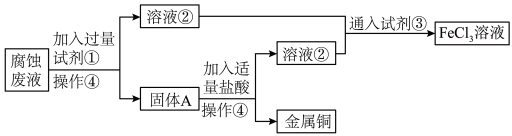
(1)②_______ (化学式)、③_______ (化学式)、④_______ (操作)。
(2)腐蚀废液中加入过量试剂①,写出发生反应的离子方程式_______ 。
(3)证明溶液②中不含 ,可往溶液中滴加
,可往溶液中滴加_______ (化学式)溶液。
(4)若已知处理前原腐蚀废液中 的质量
的质量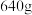 ,固体A的质量
,固体A的质量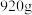 ,则流程图中加入适量盐酸(浓度
,则流程图中加入适量盐酸(浓度 )的体积至少
)的体积至少_______ L。
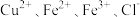 ,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得
,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得 溶液,请根据以下流程图,回答下列问题。
溶液,请根据以下流程图,回答下列问题。
(1)②
(2)腐蚀废液中加入过量试剂①,写出发生反应的离子方程式
(3)证明溶液②中不含
 ,可往溶液中滴加
,可往溶液中滴加(4)若已知处理前原腐蚀废液中
 的质量
的质量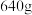 ,固体A的质量
,固体A的质量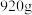 ,则流程图中加入适量盐酸(浓度
,则流程图中加入适量盐酸(浓度 )的体积至少
)的体积至少
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】图示各个物质间的转化关系中,X、Y、Z包含相同的元素

(1)气体Z是______________ 色,具有______________ 气味的气体。
(2)固体X______________ 溶于水(填“能”或“不”)。
(3)请写出Z与O2生成Y的化学方程式___________________________ 。
(4)请写出X与浓硫酸反应生成Y的化学方程式________________________ 。
(5)请写出Z与Y反应生成X的化学方程式____________________________ 。
(6)将Y通入到溴水当中发现溴水褪色,请写出其离子方程式________________________ ,这体现了Y具有___________ 性。

(1)气体Z是
(2)固体X
(3)请写出Z与O2生成Y的化学方程式
(4)请写出X与浓硫酸反应生成Y的化学方程式
(5)请写出Z与Y反应生成X的化学方程式
(6)将Y通入到溴水当中发现溴水褪色,请写出其离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】在实验室里制取少量FeCl3,可按照一定顺序连接下图中所列装置,所通过的气体过量且反应充分。试回答以下问题:

(1)实验时,各装置接口的连接顺序为___________________________ (用a、b、c、d等字母表示);
(2)C装置的作用是________________________ ;
(3)D装置的作用是_____________________________________ ;
(4)检验B装置中反应后铁是否有剩余的方法是:_______________________ ;
(5)用此方法可制得无水氯化铁。你认为能否改用Fe和盐酸反应,再通入过量氯气、蒸干溶液的方法来制取无水氯化铁,________ (答:是或否);说明理由:_________________ 。

(1)实验时,各装置接口的连接顺序为
(2)C装置的作用是
(3)D装置的作用是
(4)检验B装置中反应后铁是否有剩余的方法是:
(5)用此方法可制得无水氯化铁。你认为能否改用Fe和盐酸反应,再通入过量氯气、蒸干溶液的方法来制取无水氯化铁,
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】水合肼(N2H4·H2O)可用作抗氧剂等,工业上常用尿素[CO(NH2)2]和 NaClO溶液反应制备水合肼。
已知:Ⅰ.N2H4·H2O 的结构如图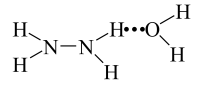 (…表示氢键)。
(…表示氢键)。
Ⅱ.N2H4·H2O 沸点 118 ℃,具有强还原性。
(1)将 Cl2 通入过量 NaOH 溶液中制备 NaClO,得到溶液 X,离子方程式是__ 。
(2)制备水合肼:将溶液 X 滴入尿素水溶液中,控制一定温度,装置如图 a(夹持及控温装置已略)。充分反应后,A 中的溶液经蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品 NaCl 和Na2CO3·10H2O。

①A 中反应的化学方程式是__ 。
②冷凝管的作用是__ 。
③若滴加 NaClO 溶液的速度较快时,水合肼的产率会下降,原因是__ 。
④NaCl 和 Na2CO3 的溶解度曲线如图 b。由蒸馏后的剩余溶液获得 NaCl 粗品的操作是__ 。
(3)水合肼在溶液中可发生类似 NH3·H2O 的电离,呈弱碱性;其分子中与 N 原子相连的 H 原子易发生取代反应。
①水合肼和盐酸按物质的量之比 1∶1 反应的离子方程式是__ 。
②碳酰肼(CH6N4O)是目前去除锅炉水中氧气的最先进材料,由水合肼与 DEC(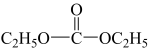 )发生取代反应制得。碳酰肼的结构简式是
)发生取代反应制得。碳酰肼的结构简式是__ 。
已知:Ⅰ.N2H4·H2O 的结构如图
 (…表示氢键)。
(…表示氢键)。Ⅱ.N2H4·H2O 沸点 118 ℃,具有强还原性。
(1)将 Cl2 通入过量 NaOH 溶液中制备 NaClO,得到溶液 X,离子方程式是
(2)制备水合肼:将溶液 X 滴入尿素水溶液中,控制一定温度,装置如图 a(夹持及控温装置已略)。充分反应后,A 中的溶液经蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品 NaCl 和Na2CO3·10H2O。

①A 中反应的化学方程式是
②冷凝管的作用是
③若滴加 NaClO 溶液的速度较快时,水合肼的产率会下降,原因是
④NaCl 和 Na2CO3 的溶解度曲线如图 b。由蒸馏后的剩余溶液获得 NaCl 粗品的操作是
(3)水合肼在溶液中可发生类似 NH3·H2O 的电离,呈弱碱性;其分子中与 N 原子相连的 H 原子易发生取代反应。
①水合肼和盐酸按物质的量之比 1∶1 反应的离子方程式是
②碳酰肼(CH6N4O)是目前去除锅炉水中氧气的最先进材料,由水合肼与 DEC(
 )发生取代反应制得。碳酰肼的结构简式是
)发生取代反应制得。碳酰肼的结构简式是
您最近一年使用:0次
【推荐3】Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反映均为放热反应)。生成物中含有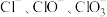 三种含氯元素的离子,其中
三种含氯元素的离子,其中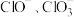 两种离子的物质的量
两种离子的物质的量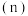 与反应时间(
与反应时间( )的曲线如图所示。
)的曲线如图所示。

(1) 时刻之前发生的反应是:
时刻之前发生的反应是:_______ 。
(2) 时,
时, 与
与 发生反应的总化学方程式为
发生反应的总化学方程式为 ,该反应中氯气的作用是
,该反应中氯气的作用是_______ ;则该石灰乳中含有 的物质的量是
的物质的量是_______ mol。
(3)据分析,生成 的反应是由温度升高引起的,通入
的反应是由温度升高引起的,通入 的速度不同,
的速度不同, 和
和 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后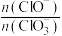
_______ 2(填“>”“<”或“=”);氯酸钙 为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施
为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施_______ (写一条即可)。
(4)请配平一下化学方程式: 。若反应过程中转移
。若反应过程中转移 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为_______ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
① ;
;
②
③
请根据上述反应分析推断后回答下列问题:
(5) 的氧化性由强到弱依次是
的氧化性由强到弱依次是_______ 。
(6)在酸性溶液中存在大量的 ,则
,则 中能与
中能与 大量共存的离子是
大量共存的离子是_______ 。
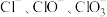 三种含氯元素的离子,其中
三种含氯元素的离子,其中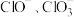 两种离子的物质的量
两种离子的物质的量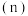 与反应时间(
与反应时间( )的曲线如图所示。
)的曲线如图所示。
(1)
 时刻之前发生的反应是:
时刻之前发生的反应是:(2)
 时,
时, 与
与 发生反应的总化学方程式为
发生反应的总化学方程式为 ,该反应中氯气的作用是
,该反应中氯气的作用是 的物质的量是
的物质的量是(3)据分析,生成
 的反应是由温度升高引起的,通入
的反应是由温度升高引起的,通入 的速度不同,
的速度不同, 和
和 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后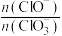
 为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施
为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施(4)请配平一下化学方程式:
 。若反应过程中转移
。若反应过程中转移 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①
 ;
;②

③

请根据上述反应分析推断后回答下列问题:
(5)
 的氧化性由强到弱依次是
的氧化性由强到弱依次是(6)在酸性溶液中存在大量的
 ,则
,则 中能与
中能与 大量共存的离子是
大量共存的离子是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】高铁酸钾( )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
①不溶于乙醚、醇和氯仿等有机溶剂。
②极易溶于水。
③热稳定性差,在低温、强碱性溶液中相当稳定。
请结合其制备方法,回答下列问题:
I.干法制备:将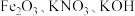 混合加热共熔,发生的反应为:
混合加热共熔,发生的反应为: (未配平)
(未配平)
(1)上述反应中作氧化剂的物质为_______ (填化学式),制备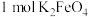 理论上需
理论上需 的物质的量为
的物质的量为_______ 。
Ⅱ.湿法制备:利用 、
、 和
和 等为原料制备,其生产流程如下:
等为原料制备,其生产流程如下:
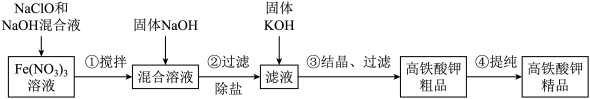
(2) 溶液的浓度和配比对产品的产率有较大的影响,现要配制
溶液的浓度和配比对产品的产率有较大的影响,现要配制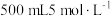 的
的 溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和_______ ,若 加入过量,在碱性介质中
加入过量,在碱性介质中 与
与 发生氧化还原反应生成
发生氧化还原反应生成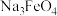 ,此反应的离子方程式为
,此反应的离子方程式为_______ 。
(3)将固体 加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除
加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除 外,主要是指
外,主要是指 和
和_______ (填化学式),此操作是利用了钠盐杂质在强碱溶液中溶解度_______ (填“大”或“小”)的性质从而实现与高铁酸钠分离。
(4)将固体 加入到滤液中发生了物质的转化,写出该反应的化学方程式
加入到滤液中发生了物质的转化,写出该反应的化学方程式_______ 。
(5)关于高铁酸钾的制备,下列说法错误的是_______(填字母)。
 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。它可通过干法和湿法等途径来制备。已知它的相关性质:①不溶于乙醚、醇和氯仿等有机溶剂。
②极易溶于水。
③热稳定性差,在低温、强碱性溶液中相当稳定。
请结合其制备方法,回答下列问题:
I.干法制备:将
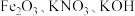 混合加热共熔,发生的反应为:
混合加热共熔,发生的反应为: (未配平)
(未配平)(1)上述反应中作氧化剂的物质为
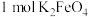 理论上需
理论上需 的物质的量为
的物质的量为Ⅱ.湿法制备:利用
 、
、 和
和 等为原料制备,其生产流程如下:
等为原料制备,其生产流程如下:
(2)
 溶液的浓度和配比对产品的产率有较大的影响,现要配制
溶液的浓度和配比对产品的产率有较大的影响,现要配制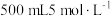 的
的 溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
溶液,需要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和 加入过量,在碱性介质中
加入过量,在碱性介质中 与
与 发生氧化还原反应生成
发生氧化还原反应生成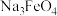 ,此反应的离子方程式为
,此反应的离子方程式为(3)将固体
 加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除
加入混合液中是为了除去高铁酸钠中混有的钠盐杂质(除盐),钠盐杂质除 外,主要是指
外,主要是指 和
和(4)将固体
 加入到滤液中发生了物质的转化,写出该反应的化学方程式
加入到滤液中发生了物质的转化,写出该反应的化学方程式(5)关于高铁酸钾的制备,下列说法错误的是_______(填字母)。
| A.干法制备的优点是步骤简单,但反应温度难以控制,熔融态的强碱存在严重腐蚀反应容器;湿法制备的优点是工艺成熟,但步骤多、操作较困难。 |
B.在湿法制备中,往滤液中加入固体 时,要在冰水浴中缓慢分多次加入。 时,要在冰水浴中缓慢分多次加入。 |
| C.在湿法制备中,第④步提纯需要采用重结晶操作,该操作第一步是将粗产品加水溶解。 |
| D.在湿法制备中,第④步提纯需将结晶的高铁酸钾过滤、洗涤、干燥,洗涤、干燥的目的是脱碱、脱水,洗涤时可用异丙醇洗涤。 |
您最近一年使用:0次
【推荐2】制备高铁酸钾[K2FeO4]并用其除去土壤和废水中的有机砷(HAPA)与无机砷[+3价砷表示As(Ⅲ)]的流程如图所示:
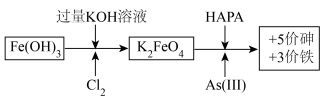
已知:酸性越强,K2FeO4越容易发生反应生成O2。
回答下列问题:
(1)生成K2FeO4的化学方程式为___ 。
(2)K2FeO4去除砷污染时作__ (填“氧化剂”或“还原剂”)。若污染物中的砷全部以Na3AsO3计,则去除全部污染时Na3AsO3与K2FeO4的物质的量之比为__ 。
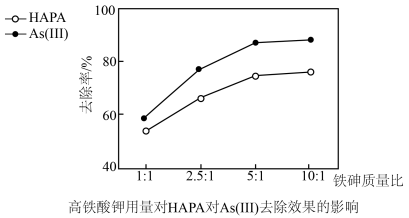
(3)氢离子浓度、高铁酸钾的用量对HAPA和As(Ⅲ)去除效果的影响如图所示。
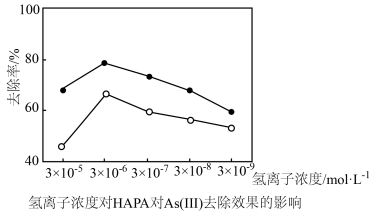
①氢离子浓度为3×10-5mol•L-1时去除率低,原因是(用离子方程式表示)__ 。
②最佳铁砷质量比为___ ,理由是__ 。

已知:酸性越强,K2FeO4越容易发生反应生成O2。
回答下列问题:
(1)生成K2FeO4的化学方程式为
(2)K2FeO4去除砷污染时作
(3)氢离子浓度、高铁酸钾的用量对HAPA和As(Ⅲ)去除效果的影响如图所示。


①氢离子浓度为3×10-5mol•L-1时去除率低,原因是(用离子方程式表示)
②最佳铁砷质量比为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】高铁酸钾(K2FeO4)是一种新型绿色、高效的水处理剂,对病毒的去除率可达99.95%。某兴趣小组设计如下实验制备K2FeO4并探究其性质。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
② 具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
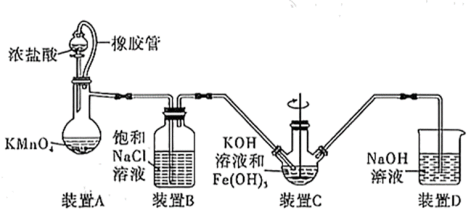
(1)制备K2FeO4(夹持装置略)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是_______ 。
②装置B的作用是_______ 。
③装置C中的KOH溶液需过量,目的是________ 。
④C中得到紫色固体和溶液。则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为______
(2)探究K2FeO4的性质甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该现象______ (填“能”或“不能”)证明“酸性条件下 氧化性强于Cl2”,并说明理由:
氧化性强于Cl2”,并说明理由:______ 。
(3)测定K2FeO4的产率若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体9.9g,则K2FeO4的产率为________ 。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
②
 具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是
②装置B的作用是
③装置C中的KOH溶液需过量,目的是
④C中得到紫色固体和溶液。则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为
(2)探究K2FeO4的性质甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该现象
 氧化性强于Cl2”,并说明理由:
氧化性强于Cl2”,并说明理由:(3)测定K2FeO4的产率若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体9.9g,则K2FeO4的产率为
您最近一年使用:0次



