下列有关测定中和反应反应热实验的说法正确的是
| A.用铜丝代替环形玻璃搅拌棒,测得的△H偏大 |
| B.强酸的稀溶液与强碱的稀溶液反应生成1mol H2O的△H均为—57.3kJ/mol |
| C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度 |
D.某同学通过实验测出稀盐酸和稀NaOH溶液反成1mol H2O反应热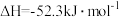 ,造成这一结果的原因一定是用测量过稀盐酸温度的温度计直接测量稀NaOH溶液的温度 ,造成这一结果的原因一定是用测量过稀盐酸温度的温度计直接测量稀NaOH溶液的温度 |
更新时间:2021-12-02 14:25:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各项表述正确的是( )
A.次氯酸的电子式: |
| B.表示中和热的热化学方程式:NaOH(aq)+HF(aq)=NaF(aq)+H2O(1)△H=-57.3kJmol |
C.H2S电离的方程式为:H2S 2H++S2- 2H++S2- |
D.标准状况下,1.12L 和1.12L 和1.12L 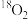 ,均含有0.1NA个氧原子 ,均含有0.1NA个氧原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
③H2(g)+ O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
④H2O(g)=H2O(l)ΔH=-44.0 kJ·mol-1
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
③H2(g)+
 O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1④H2O(g)=H2O(l)ΔH=-44.0 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热小于-110.5 kJ·mol-1 |
| B.浓硫酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
| C.氢气的燃烧热为-241.8 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(l)的反应热为ΔH=+571.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列有关能量的判断或表示方法正确的是( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| B.已知C(石墨)=C(金刚石) △H>0,则可知石墨比金刚石更稳定 |
| C.由H+(aq)+OH−(aq)=H2O(l);△H=−57.3kJ⋅mol−1,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
D.已知H2燃烧热△H=−285.8 kJ⋅mol−1,则氢气燃烧的热化学方程式为:H2(g)+ O2(g)=H2O(g) △H=−285.8 kJ⋅mol−1 O2(g)=H2O(g) △H=−285.8 kJ⋅mol−1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验装置及其应用的描述均正确的是


| A.用①装置验证铁钉的析氢腐蚀 |
| B.用②装置进行强酸强碱稀溶液的中和热测定 |
| C.用③装置测定未知稀盐酸的物质的量浓度 |
| D.用④装置探究反应物浓度对反应速率的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关中和热的实验操作正确的是


| A.去掉两烧杯间的碎泡沫塑料 |
| B.记录反应的最高温度 |
| C.向烧杯中加碱时有碱液溅到烧杯外 |
| D.酸碱混合后不及时搅拌 |
您最近一年使用:0次
【推荐3】根据实验目的,实验方法、操作或现象均正确的是
| 实验目的 | 实验方法、操作或现象 | |
| A | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中。一段时间后,取溶液加入 溶液,无蓝色沉淀生成 溶液,无蓝色沉淀生成 |
| B | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的 溶液,分别加入等体积等浓度的 溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 |
| C | 测定中和反应的反应热 | 往烧杯中缓慢加入NaOH溶液,用温度传感器采集烧杯内溶液的温度的变化 |
| D | 探究温度对化学平衡的影响 | 在试管中加入2 mL 0.5 mol/L  溶液,加热试管,观察到溶液从蓝色变成黄色 溶液,加热试管,观察到溶液从蓝色变成黄色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



