已知:
①
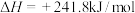
②
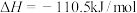
③
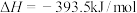
请填写下列空白。
(1)上述反应中属于吸热反应的是___________ (填序号)。
(2)表示C的燃烧热的热化学方程式为___________ (填序号)。
(3)10g 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为___________ 。
①

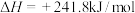
②

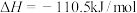
③

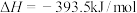
请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)表示C的燃烧热的热化学方程式为
(3)10g
 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为
更新时间:2021-12-01 23:39:28
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列热化学方式
(1)在101 kPa时,4.0 g硫粉在氧气中完全燃烧生成二氧化硫,放出27 kJ的热量,硫燃烧的热化学方程式为___________ 。
(2)在101 kPa时,氢气在1.0 mol氧气中完全燃烧,生成2.0 mol液态水,放出571.6 kJ的热量,表示氢气燃烧的热化学方程式为___________ 。
(3)稀的强酸与稀的强碱反应生成生成1molH2O(l)时放出的热称为中和热。已知含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量。写出表示中和热的热化学方程式:
___________ 。
(4)已知:0.4 mol液态肼(N2H4)与足量的液态双氧水反应,生成氮气和水蒸气,并放出256.65 kJ的热量,反应的热化学方程式为___________ 。
(5)已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,乙炔燃烧的热化学方程式为___________ 。
(1)在101 kPa时,4.0 g硫粉在氧气中完全燃烧生成二氧化硫,放出27 kJ的热量,硫燃烧的热化学方程式为
(2)在101 kPa时,氢气在1.0 mol氧气中完全燃烧,生成2.0 mol液态水,放出571.6 kJ的热量,表示氢气燃烧的热化学方程式为
(3)稀的强酸与稀的强碱反应生成生成1molH2O(l)时放出的热称为中和热。已知含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量。写出表示中和热的热化学方程式:
(4)已知:0.4 mol液态肼(N2H4)与足量的液态双氧水反应,生成氮气和水蒸气,并放出256.65 kJ的热量,反应的热化学方程式为
(5)已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,乙炔燃烧的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
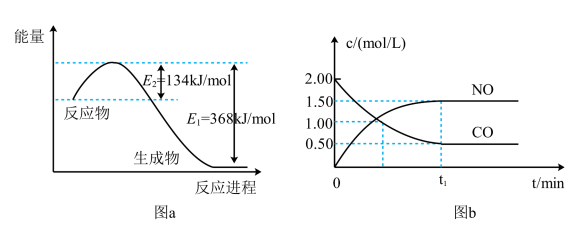
(1)写出NO2和CO反应的热化学方程式_______________ 。
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=__________ 。
(3)此温度下该反应的平衡常数K=_________ ;温度降低,K________ (填“变大”、“变小”或“不变”)

(1)写出NO2和CO反应的热化学方程式
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=
(3)此温度下该反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)在25℃、1.01×105Pa时,16g S粉在足量的氧气中充分燃烧生成二氧化硫气体,放出148.5kJ的热量,则S的燃烧热的热化学方程式为:___ 。
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:___ 。
(3)已知如图所示的可逆反应:
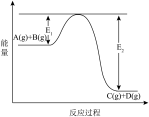
①A(g)+B(g) 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q___ 0(填“>”、“<”或“=”)
②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1___ ,ΔH的变化是:ΔH___ (填“增大”“减小”“不变”)。
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=___ kJ/mol。
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1___ △H2
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=___ kJ/mol;
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为___ (填序号)
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:
(3)已知如图所示的可逆反应:

①A(g)+B(g)
 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】填空
(1)氢气燃烧放出能量,生成物总能量_____ 反应物总能量(高于、低于)
下列反应中,也放出能量的是_____ 。
①断裂化学键②分解反应③碳与 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应
(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应: 的放出热量=
的放出热量=_____ 。(用a、b、c表示)
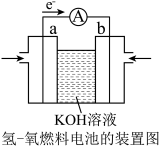
(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的_____ (a或b)极。
(1)氢气燃烧放出能量,生成物总能量
下列反应中,也放出能量的是
①断裂化学键②分解反应③碳与
 生成CO④燃料燃烧⑤酸碱中和反应⑥
生成CO④燃料燃烧⑤酸碱中和反应⑥ 与Mg反应
与Mg反应(2)已知断裂1molH-H键、1mol氧氧键、1molO-H键需要吸收的能量分别为akJ、bkJ、ckJ。则反应:
 的放出热量=
的放出热量=(3)航天技术上使用的一种氢-氧燃料电池原理可以简单看作如图,则:工作时,氢燃料通入该电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙烯可用作合成纤维、合成橡胶、塑料的原料。回答下列问题:
(1)用CrO3做催化剂,CO2重整C2H6制乙烯的反应过程如下:
C2H6(g) C2H4(g)+H2(g) ΔH1;
C2H4(g)+H2(g) ΔH1;
3H2(g)+2CrO3(s)=3H2O(g)+Cr2O3(s) ΔH2;
Cr2O3(s)+3CO2(g)=3CO(g)+2CrO3(s) ΔH3。
反应C2H6(g)+CO2(g) C2H4(g)+CO(g)+H2O(g)的ΔH=
C2H4(g)+CO(g)+H2O(g)的ΔH=_____ (用含ΔH1、ΔH2、ΔH3的代数式表示)。
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
已知上述反应中相关的化学键键能数据如下:
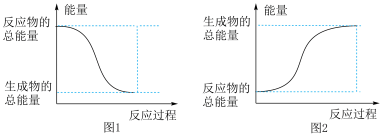
则该反应的ΔH=_____ ,该反应_____ (填“放热”或“吸热”),能正确表示该反应的图示是_____ (填标号)。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的燃烧热热化学方程式为_____ 。
(1)用CrO3做催化剂,CO2重整C2H6制乙烯的反应过程如下:
C2H6(g)
 C2H4(g)+H2(g) ΔH1;
C2H4(g)+H2(g) ΔH1;3H2(g)+2CrO3(s)=3H2O(g)+Cr2O3(s) ΔH2;
Cr2O3(s)+3CO2(g)=3CO(g)+2CrO3(s) ΔH3。
反应C2H6(g)+CO2(g)
 C2H4(g)+CO(g)+H2O(g)的ΔH=
C2H4(g)+CO(g)+H2O(g)的ΔH=(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C O O | H—H | C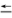 O(CO) O(CO) |
| 键能/kJ·mol-1 | 413 | 745 | 436 | 1075 |

(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2gSiH4自燃放出热量89.2kJ。SiH4自燃的燃烧热热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是________ 反应(填“吸热”、“放热”)。
(2)反应体系中加入催化剂对反应热是否有影响?_________ (填“有”、“无”),原因是______________________________________________________________________ 。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________________ ,E2___________ (填“增大”、“减小”、“不变”)。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)反应体系中加入催化剂对反应热是否有影响?
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)溶液pH可以用pH试纸测量,也可以用____ 测量。
(2)NaNH2是离子化合物,各原子均满足稳定结构,写出NaNH2的电子式____ 。
(3)已知双氧水(H2O2)时一种极弱的电解质,若把H2O2看成二元弱酸,请写出其在水中的电离方程式:____ ,____ 。
(4)适量H2(g)在1molO2(g)中完全燃烧,生成2molH2O(l),放出571.6kJ的热量,请写出表示H2(g)燃烧热的热化学方程式____ 。
(1)溶液pH可以用pH试纸测量,也可以用
(2)NaNH2是离子化合物,各原子均满足稳定结构,写出NaNH2的电子式
(3)已知双氧水(H2O2)时一种极弱的电解质,若把H2O2看成二元弱酸,请写出其在水中的电离方程式:
(4)适量H2(g)在1molO2(g)中完全燃烧,生成2molH2O(l),放出571.6kJ的热量,请写出表示H2(g)燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究化学反应中的能量变化有重要意义,请根据学过的知识回答下列问题。
(1)已知CH3OH(1)的燃烧热△H = - 238.6 kJ·mol-1,CH3OH(1)+ O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a
O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a___________ (填“> ”“<”或“=”) 238. 6。
(2)已知:H2(g)+ O2(g)
O2(g)  H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为___________ 。
(3)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:___________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H = - 1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为___________ kJ。
(5)已知25℃、101 kPa时,1 g甲烷不完全燃烧生成CO和液态水时放出37.96 kJ热量,则该条件下反应2CH4(g) +3O2(g)=2CO(g)+4H2O(l)的△H =___________ kJ·mol-1。
(1)已知CH3OH(1)的燃烧热△H = - 238.6 kJ·mol-1,CH3OH(1)+
 O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a
O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a(2)已知:H2(g)+
 O2(g)
O2(g)  H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为(3)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H = - 1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
(5)已知25℃、101 kPa时,1 g甲烷不完全燃烧生成CO和液态水时放出37.96 kJ热量,则该条件下反应2CH4(g) +3O2(g)=2CO(g)+4H2O(l)的△H =
您最近一年使用:0次

 汽化时吸收的热量为
汽化时吸收的热量为 ,
, 的燃烧热为
的燃烧热为 ,请写出
,请写出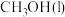 燃烧热的热化学方程式
燃烧热的热化学方程式

