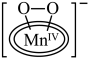
已知下列反应的热化学方程式:


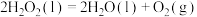

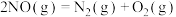

则反应 的
的 为
为


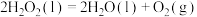

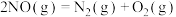

则反应
 的
的 为
为A.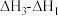 | B.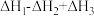 |
C.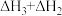 | D.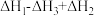 |
更新时间:2021-12-04 07:23:00
|
【知识点】 盖斯定律及其有关计算
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:①N2(g)+O2(g)=2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)⇌2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是

②N2(g)+3H2(g)⇌2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是

| A.反应②中的能量变化如上图所示,则ΔH2=E1-E3 |
| B.H2的燃烧热为241.8 kJ·mol-1 |
| C.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2=2Q1 |
| D.氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=-906 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃、101kPa 下:
①2Na(s)+ O2(g)=Na2O(s) ΔH1=-414 kJ/mol
O2(g)=Na2O(s) ΔH1=-414 kJ/mol
② 2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ/mol
下列说法正确的是
①2Na(s)+
 O2(g)=Na2O(s) ΔH1=-414 kJ/mol
O2(g)=Na2O(s) ΔH1=-414 kJ/mol② 2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ/mol
下列说法正确的是
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s) =-317kJ/mol =-317kJ/mol |
您最近一年使用:0次


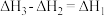
 中
中 的化合价为
的化合价为 价
价