实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以在常温下利用反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,装置如图所示:
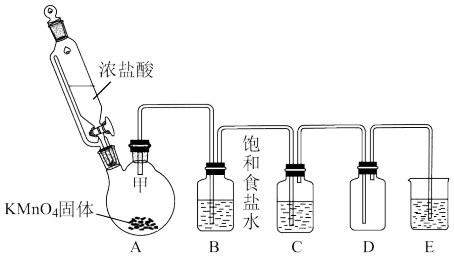
(1)装置A中盛放浓盐酸的仪器名称是___ ,该装置相比普通分液漏斗的优点是___ 。
(2)装置B的作用是___ ,装置C中盛装的药品是___ 。
(3)D装置收集氯气采用了___ 方法。
a.向下排空气法 b.向上排空气法 c.排水法 d.排饱和食盐水
(4)装置E中发生反应的化学方程式是___ 。
(5)某同学在实验室配制80mL1mol/L的NaOH溶液用于上述实验:
①该同学应选择___ mL的容量瓶,需称取NaOH的质量为___ g。
②若该同学所配溶液浓度偏大,请写出可能的一个原因是___ 。

(1)装置A中盛放浓盐酸的仪器名称是
(2)装置B的作用是
(3)D装置收集氯气采用了
a.向下排空气法 b.向上排空气法 c.排水法 d.排饱和食盐水
(4)装置E中发生反应的化学方程式是
(5)某同学在实验室配制80mL1mol/L的NaOH溶液用于上述实验:
①该同学应选择
②若该同学所配溶液浓度偏大,请写出可能的一个原因是
更新时间:2021-12-10 19:01:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,B为日常生活中最常见无色无味液体, E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,G为黄绿色气体单质,H是漂白液的有效成分,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
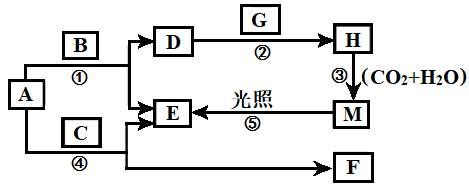
请回答下列问题:
(1)写出G、H的化学式:G________ ,H________ 。D的俗名是__________ 。
(2)写出反应②的离子方程式:_________________________________________ 。
(3)利用下图装置进行实验,证明氧化性强弱:KMnO4>Cl2>Br2。
限选试剂:KBr溶液、KMnO4、浓盐酸。

已知:2KMnO4+16HCl(浓)=2KCl+ 2MnCl2+5Cl2↑+8H2O
请回答下列问题:
装置a 的名称是____________________ ,d中盛放的试剂是____________ 。

请回答下列问题:
(1)写出G、H的化学式:G
(2)写出反应②的离子方程式:
(3)利用下图装置进行实验,证明氧化性强弱:KMnO4>Cl2>Br2。
限选试剂:KBr溶液、KMnO4、浓盐酸。

已知:2KMnO4+16HCl(浓)=2KCl+ 2MnCl2+5Cl2↑+8H2O
请回答下列问题:
装置a 的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氯气是重要的化工原料,在生产和生活中应用广泛。兴趣小组以“氯气的制备、收集及性质”为主题开展探究性学习。
(1)氯气的制备与收集。实验装置如下图所示。

①装置A中反应的化学方程式是__________ 。
②装置B的作用是__________ 。
③装置C中盛放的物质X是__________ 。
④装置E用于吸收尾气,E中反应的离子方程式是__________ 。
(2)影响氯气溶解性的因素。为了探究影响氯气在 溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
实验测得 在不同浓度的
在不同浓度的 、
、 溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
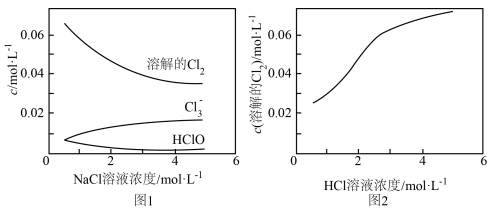
图1 图2
①从图1可以看出,氯气溶于 溶液时主要发生了两个反应,一是
溶液时主要发生了两个反应,一是 与水的反应,二是
与水的反应,二是__________ (填反应的离子方程式)。随着 溶液浓度的增大,
溶液浓度的增大, 与水的反应受到了抑制,证据是
与水的反应受到了抑制,证据是___________ 。
②结合图1、2可知,导致 在
在 溶液中溶解性随
溶液中溶解性随 溶液浓度增大而变小的微粒应是
溶液浓度增大而变小的微粒应是___________ (填微粒符号)。
(1)氯气的制备与收集。实验装置如下图所示。

①装置A中反应的化学方程式是
②装置B的作用是
③装置C中盛放的物质X是
④装置E用于吸收尾气,E中反应的离子方程式是
(2)影响氯气溶解性的因素。为了探究影响氯气在
 溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:实验测得
 在不同浓度的
在不同浓度的 、
、 溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
图1 图2
①从图1可以看出,氯气溶于
 溶液时主要发生了两个反应,一是
溶液时主要发生了两个反应,一是 与水的反应,二是
与水的反应,二是 溶液浓度的增大,
溶液浓度的增大, 与水的反应受到了抑制,证据是
与水的反应受到了抑制,证据是②结合图1、2可知,导致
 在
在 溶液中溶解性随
溶液中溶解性随 溶液浓度增大而变小的微粒应是
溶液浓度增大而变小的微粒应是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某小组同学在实验室制备、收集氯气,并进行氯水中相关物质的性质探究,回答下列问题。
(1)制备 。装置Ⅰ中发生如下反应:
。装置Ⅰ中发生如下反应: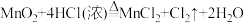 。盛放浓盐酸的仪器名称是
。盛放浓盐酸的仪器名称是_______ 。
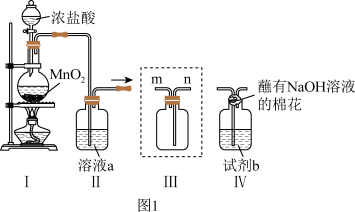
(2)装置Ⅱ中溶液a为饱和食盐水,作用为_______ 。
(3)收集 。装置Ⅲ中气体应该从集气瓶的
。装置Ⅲ中气体应该从集气瓶的_______ (选“m”或“n”)口进入。
(4)氯水相关物质的性质探究。
①若装置Ⅳ中试剂b为 ,制得氯水。氯水呈黄绿色是由于其中含有
,制得氯水。氯水呈黄绿色是由于其中含有_______ ; 与
与 反应的化学方程式为
反应的化学方程式为_______ 。
②若装置Ⅳ中试剂b为 ,可制得
,可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,且不与
,且不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到
溶液,分别滴在三张红色纸条上,可观察到_______ 现象,证明氯水中HClO具有漂白性作用。
③若要模拟工业制备漂白粉,装置Ⅳ中试剂b为_______ ,制备漂白粉的化学方程式为_______ 。
④验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图2),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

若能够证明氯水中HClO在光照下发生了分解反应,则图3中纵坐标可以表示的物理量是_______ (填字母)。(注:酸性溶液中, 越大,pH越小,溶液酸性越强)。据此数据,可分析得到HClO在光照下发生的化学反应方程式为
越大,pH越小,溶液酸性越强)。据此数据,可分析得到HClO在光照下发生的化学反应方程式为_______ 。
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数 e.溶液的颜色
(1)制备
 。装置Ⅰ中发生如下反应:
。装置Ⅰ中发生如下反应: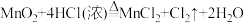 。盛放浓盐酸的仪器名称是
。盛放浓盐酸的仪器名称是
(2)装置Ⅱ中溶液a为饱和食盐水,作用为
(3)收集
 。装置Ⅲ中气体应该从集气瓶的
。装置Ⅲ中气体应该从集气瓶的(4)氯水相关物质的性质探究。
①若装置Ⅳ中试剂b为
 ,制得氯水。氯水呈黄绿色是由于其中含有
,制得氯水。氯水呈黄绿色是由于其中含有 与
与 反应的化学方程式为
反应的化学方程式为②若装置Ⅳ中试剂b为
 ,可制得
,可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,且不与
,且不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到
溶液,分别滴在三张红色纸条上,可观察到③若要模拟工业制备漂白粉,装置Ⅳ中试剂b为
④验证氯水中HClO光照分解的产物。将装置Ⅳ广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图2),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

若能够证明氯水中HClO在光照下发生了分解反应,则图3中纵坐标可以表示的物理量是
 越大,pH越小,溶液酸性越强)。据此数据,可分析得到HClO在光照下发生的化学反应方程式为
越大,pH越小,溶液酸性越强)。据此数据,可分析得到HClO在光照下发生的化学反应方程式为a.氯水的pH b.氢离子的浓度 c.氯离子的浓度 d.氧气的体积分数 e.溶液的颜色
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】 在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程利用如图装置制备无水
在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程利用如图装置制备无水 。
。

【查阅资料】
a.浓盐酸和 在加热条件下可生成
在加热条件下可生成 :
: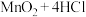 (浓)
(浓)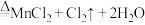
b.无水 在潮湿空气中易潮解,加热易升华。
在潮湿空气中易潮解,加热易升华。
c.向炽热的铁屑中通入 可生产无水
可生产无水 ;向炽热的铁屑中通入
;向炽热的铁屑中通入 可生产无水
可生产无水 。
。
(1)按图示组装好仪器,在添加药品前应先进行的操作是_______ 。
(2)开始实验时,应先点燃装置_______ (填“Ⅰ”或“Ⅲ”)处的酒精灯,待_______ (填实验现象)后再点燃另一装置的酒精灯。
(3)D中发生反应的化学方程式为_______ 。
(4)F中浓硫酸的作用是_______ 。
(5)在综合考虑各因素后,同学们提出了如下改进意见:
①甲建议,在装置Ⅰ和装置Ⅱ间增加盛有饱和食盐水的洗气瓶,其作用是_______ 。
②乙建议,将装置Ⅲ和Ⅳ改成装置Ⅴ。反应管G中生成的 大部分进入收集器中,少量沉积在G的右端,要使沉积的
大部分进入收集器中,少量沉积在G的右端,要使沉积的 进入收集器,可进行的操作是
进入收集器,可进行的操作是_______ ;K中 溶液的作用是
溶液的作用是_______ (用化学方程式表示)。
③丙建议,装置Ⅴ中的H、K可精简为H,但需将H中的药品换为_______ (填药品名称)。
 在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程利用如图装置制备无水
在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程利用如图装置制备无水 。
。
【查阅资料】
a.浓盐酸和
 在加热条件下可生成
在加热条件下可生成 :
: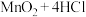 (浓)
(浓)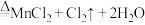
b.无水
 在潮湿空气中易潮解,加热易升华。
在潮湿空气中易潮解,加热易升华。c.向炽热的铁屑中通入
 可生产无水
可生产无水 ;向炽热的铁屑中通入
;向炽热的铁屑中通入 可生产无水
可生产无水 。
。(1)按图示组装好仪器,在添加药品前应先进行的操作是
(2)开始实验时,应先点燃装置
(3)D中发生反应的化学方程式为
(4)F中浓硫酸的作用是
(5)在综合考虑各因素后,同学们提出了如下改进意见:
①甲建议,在装置Ⅰ和装置Ⅱ间增加盛有饱和食盐水的洗气瓶,其作用是
②乙建议,将装置Ⅲ和Ⅳ改成装置Ⅴ。反应管G中生成的
 大部分进入收集器中,少量沉积在G的右端,要使沉积的
大部分进入收集器中,少量沉积在G的右端,要使沉积的 进入收集器,可进行的操作是
进入收集器,可进行的操作是 溶液的作用是
溶液的作用是③丙建议,装置Ⅴ中的H、K可精简为H,但需将H中的药品换为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等。
Ⅰ.氯气的制备
氯气在实验室中可通过MnO2和浓盐酸混合加热制备,实验装置见图;在工业上可通过电解饱和NaCl溶液获得。
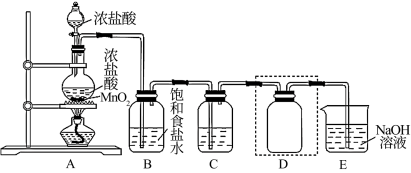
(1)装置A中发生反应的离子方程式是___ 。
(2)装置B的作用是___ 。
(3)装置D用于收集Cl2,请将装置D中的导气管补充完整:___ 。
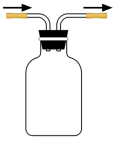
(4)装置E用于吸收尾气Cl2,E中发生反应的化学方程式是___ 。
(5)电解饱和NaCl溶液对应的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,则该反应中转移的电子数为1.204×1023时,溶液质量减少
2NaOH+H2↑+Cl2↑,则该反应中转移的电子数为1.204×1023时,溶液质量减少___ g。(假设生成的气体全部逸出)
Ⅱ.氯气的应用
(6)可用Cl2和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是___ 。(填化学式)
(7)向KI溶液滴加过量氯水会生成IO ,发生反应的离子方程式如下:
,发生反应的离子方程式如下:
 Cl2+
Cl2+ I-+
I-+ H2O=
H2O= IO
IO +
+ Cl-+
Cl-+ ____
____
请补全产物,并将离子方程式配平___ 。
(8)Cl2O是次氯酸的酸酐,其制备方法之一是将Cl2通入HgO中即可制得,同时生成HgO•HgCl2。请写出对应的化学方程式并用双线桥表示电子的转移:____ 。
Ⅰ.氯气的制备
氯气在实验室中可通过MnO2和浓盐酸混合加热制备,实验装置见图;在工业上可通过电解饱和NaCl溶液获得。

(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置D用于收集Cl2,请将装置D中的导气管补充完整:

(4)装置E用于吸收尾气Cl2,E中发生反应的化学方程式是
(5)电解饱和NaCl溶液对应的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑,则该反应中转移的电子数为1.204×1023时,溶液质量减少
2NaOH+H2↑+Cl2↑,则该反应中转移的电子数为1.204×1023时,溶液质量减少Ⅱ.氯气的应用
(6)可用Cl2和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是
(7)向KI溶液滴加过量氯水会生成IO
 ,发生反应的离子方程式如下:
,发生反应的离子方程式如下: Cl2+
Cl2+ I-+
I-+ H2O=
H2O= IO
IO +
+ Cl-+
Cl-+ ____
____请补全产物,并将离子方程式配平
(8)Cl2O是次氯酸的酸酐,其制备方法之一是将Cl2通入HgO中即可制得,同时生成HgO•HgCl2。请写出对应的化学方程式并用双线桥表示电子的转移:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】学习化学的捷径——化学实验
化学是一门以实验为基础的科学,化学的许多重大发现和研究都是通过实验得到的。化学实验是化学科学赖以产生和发展的基础,化学的每一次重大突破,长期以来,化学被称为“实验的科学”。
学习化学的一个重要途径是实验,通过实验以及对实验现象的观察、记录和分析等,可以发现和验证物质的性质和化学原理,并应用化学知识来指导化工实践。
(1)在实验室制Cl2并回收MnCl2的实验中,下列装置能达到目的的是_____。

(2)唐代孙思选撰著的《备急千金要方》中记载:“枸杞根一百斤,曹蒲五斤。上二味细判,以水四石煮取一石六斗,去滓,酿二斛米酒,熟,稍稍饮之。”
①上述过程中蕴含的实验操作依次为碾碎、_____ 、_____ 、_____ 。
②取20mL碘,置于分液漏斗中,然后注入5mLCCl4,振荡后静置,观察到的实验现象是_____ 。
(3)现有一混有少量氯化钾的硝酸钾粉末,提纯硝酸钾的步骤为:溶解,蒸发浓缩,_____ ,结晶,过滤。
(4)实验室用2.0mol•L﹣1NaCl溶液配100mL0.50mol•L﹣1NaCl溶液
①需要量取2.0mol•L﹣1NaCl溶液_____ mL:
②配制上述溶除需要玻璃棒、量筒外,还需要的仪器有_____ 、_____ 、_____ 。
③配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”):
a.没有洗涤烧杯和玻璃棒。_____ 。
b.定容时俯视容量瓶的刻度线。_____ 。
c.如果加水超过了刻度线,取出部分水使液面恰好达到刻度线。_____ 。
化学是一门以实验为基础的科学,化学的许多重大发现和研究都是通过实验得到的。化学实验是化学科学赖以产生和发展的基础,化学的每一次重大突破,长期以来,化学被称为“实验的科学”。
学习化学的一个重要途径是实验,通过实验以及对实验现象的观察、记录和分析等,可以发现和验证物质的性质和化学原理,并应用化学知识来指导化工实践。
(1)在实验室制Cl2并回收MnCl2的实验中,下列装置能达到目的的是_____。

| A.用装置甲制取Cl2 |
| B.用装置乙可以收集氯气 |
| C.用装置丙分离MnO2固体和MnCl2溶液 |
| D.用装置丁蒸干MnCl2溶液制MnCl2•4H2O |
(2)唐代孙思选撰著的《备急千金要方》中记载:“枸杞根一百斤,曹蒲五斤。上二味细判,以水四石煮取一石六斗,去滓,酿二斛米酒,熟,稍稍饮之。”
①上述过程中蕴含的实验操作依次为碾碎、
②取20mL碘,置于分液漏斗中,然后注入5mLCCl4,振荡后静置,观察到的实验现象是
(3)现有一混有少量氯化钾的硝酸钾粉末,提纯硝酸钾的步骤为:溶解,蒸发浓缩,
(4)实验室用2.0mol•L﹣1NaCl溶液配100mL0.50mol•L﹣1NaCl溶液
①需要量取2.0mol•L﹣1NaCl溶液
②配制上述溶除需要玻璃棒、量筒外,还需要的仪器有
③配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”):
a.没有洗涤烧杯和玻璃棒。
b.定容时俯视容量瓶的刻度线。
c.如果加水超过了刻度线,取出部分水使液面恰好达到刻度线。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室需使用80mL3mol/L稀硫酸进行有关实验,请你用98%的浓硫酸进行配制。
(1)需量取98%的浓硫酸(密度为1.84g/cm3)___________ mL。
(2)配制操作可分解成如下几步,其中正确的操作顺序是___________ 。
A.用约30mL蒸馏水,分成三次洗涤烧杯及玻璃棒,将每次洗涤液注入容量瓶中,并重复操作两次
B.将已冷却的稀硫酸小心地用玻璃棒引流入经检查不漏水的容量瓶中
C.根据(1)计算,用量筒量取一定体积的浓硫酸
D.将浓硫酸沿烧杯内壁缓缓注入盛有约50mL蒸馏水的烧杯中,并不断用玻璃棒搅拌
E.盖上容量瓶塞子,反复倾倒振荡,摇匀溶液
F.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶瓶颈上的刻度线相切
G.继续往容量瓶中小心地滴加蒸馏水,使液面接近瓶颈上环形刻度线1~2cm处
(3)进行D步操作时,必须___________ 后,才能进行后面的操作。
(4)配制上述溶液时,下列操作会导致所配溶液的浓度偏高的是___________ (填标号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
(5)若实验过程中出现以下情况,应该如何处理?
①加蒸馏水时不慎超过了容量瓶瓶颈上的刻度线:___________ 。
②向容量瓶中转移溶液时(操作C)不慎将少量溶液洒在容量瓶外面:___________ 。
(1)需量取98%的浓硫酸(密度为1.84g/cm3)
(2)配制操作可分解成如下几步,其中正确的操作顺序是
A.用约30mL蒸馏水,分成三次洗涤烧杯及玻璃棒,将每次洗涤液注入容量瓶中,并重复操作两次
B.将已冷却的稀硫酸小心地用玻璃棒引流入经检查不漏水的容量瓶中
C.根据(1)计算,用量筒量取一定体积的浓硫酸
D.将浓硫酸沿烧杯内壁缓缓注入盛有约50mL蒸馏水的烧杯中,并不断用玻璃棒搅拌
E.盖上容量瓶塞子,反复倾倒振荡,摇匀溶液
F.用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶瓶颈上的刻度线相切
G.继续往容量瓶中小心地滴加蒸馏水,使液面接近瓶颈上环形刻度线1~2cm处
(3)进行D步操作时,必须
(4)配制上述溶液时,下列操作会导致所配溶液的浓度偏高的是
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
(5)若实验过程中出现以下情况,应该如何处理?
①加蒸馏水时不慎超过了容量瓶瓶颈上的刻度线:
②向容量瓶中转移溶液时(操作C)不慎将少量溶液洒在容量瓶外面:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂。
(1)K2FeO4可以去除水中的重金属,主要依靠其在水中分解后产生的Fe(OH)3胶体沉淀的吸附和共沉作用。可通过___________ 鉴别Fe(OH)3胶体和K2FeO4溶液。
(2)在碱性条件下,KClO饱和溶液可将Fe(NO3)3转化为K2FeO4,K2FeO4中Fe的化合价为___________ 价,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)K2FeO4可利用Na2FeO4制得。干法制备Na2FeO4的主要反应为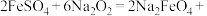
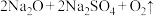 。该反应中氧化产物为
。该反应中氧化产物为___________ (填化学式),每生成1molO2,反应中转移的电子数为___________  。
。
(4)实验室需要使用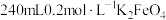 溶液。
溶液。
①配制K2FeO4溶液的过程中需要使用的玻璃仪器有烧杯、量筒、胶头滴管、___________ 和___________ 。
②用托盘天平称量___________ gK2FeO4固体。
③定容时,俯视刻度线将导致配得的溶液浓度___________ (填“偏低”“偏高”或“无影响”)。
(1)K2FeO4可以去除水中的重金属,主要依靠其在水中分解后产生的Fe(OH)3胶体沉淀的吸附和共沉作用。可通过
(2)在碱性条件下,KClO饱和溶液可将Fe(NO3)3转化为K2FeO4,K2FeO4中Fe的化合价为
(3)K2FeO4可利用Na2FeO4制得。干法制备Na2FeO4的主要反应为
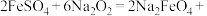
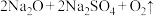 。该反应中氧化产物为
。该反应中氧化产物为 。
。(4)实验室需要使用
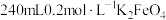 溶液。
溶液。①配制K2FeO4溶液的过程中需要使用的玻璃仪器有烧杯、量筒、胶头滴管、
②用托盘天平称量
③定容时,俯视刻度线将导致配得的溶液浓度
您最近一年使用:0次

 MnCl2+Cl2↑+2H2O制备纯净干燥的氯气,设计的实验装置如图:
MnCl2+Cl2↑+2H2O制备纯净干燥的氯气,设计的实验装置如图:


