Ⅰ.使用正确的化学用语填空。
(1)写出下列物质的电子式:
氮气___________ ;过氧化钠___________ ;四氯化碳___________ 。
(2)写出下列物质的结构式:
二氧化碳___________ ;过氧化氢___________ ;次氯酸___________ 。
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:___________ 。
②原子半径由大到小的顺序:___________ 。
③离子半径由大到小的顺序:___________ 。
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F___________ Cl- ②Fe2+___________ Fe3+ ③O2-___________ Mg2+。
(1)写出下列物质的电子式:
氮气
(2)写出下列物质的结构式:
二氧化碳
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:
②原子半径由大到小的顺序:
③离子半径由大到小的顺序:
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F
2021高一·全国·专题练习 查看更多[1]
(已下线)专题5 微观结构与物质的多样性 综合评价(1)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)
更新时间:2021-12-27 08:50:07
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】下列表格是元素周期表的一部分。请按要求填空。
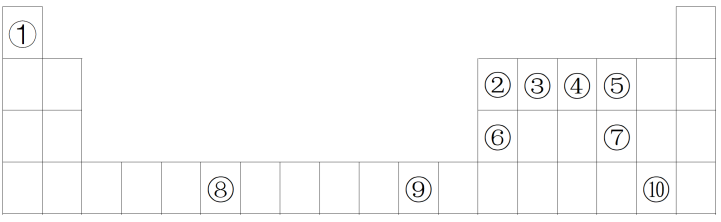
(1)写出一种由元素①和⑤形成的常见化合物的电子式为_______
(2)由②形成的单质是一种是硬度很大,熔点很高的晶体,则该晶体属于_______ 晶体。
(3)③④⑤三种元素的第一电离能从大到小排序为_______ 。
(4)写出工业上冶炼⑥单质的化学方程式_______ 。
(5)列举元素⑦形成的最高价含氧酸的用途_______ (至少列举两种)。
(6)元素⑧的核外电子排布式为_______ 。
(7)下图为⑨晶体的晶胞结构。若晶胞的棱长为acm,则两个最近的⑨原子之间的距离是_______ cm,晶胞密度为_______ g·cm-3(⑨的摩尔质量用M表示,阿伏加德罗常数的值用NA表示)。

(8)天津市有着丰富的海水资源,海水中含有丰富的各种元素,化学兴趣小组采用“空气吹出法”从浓海水吹出元素⑩形成的单质Br2,常温下,Br2的颜色为深红棕色液体,吹出的溴用纯碱溶液吸收,吸收溴的主要反应为:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),当吸收1molBr2时,转移电子的物质的量为_______ mol。反应产物 的VSEPR模型名称为
的VSEPR模型名称为_______

(1)写出一种由元素①和⑤形成的常见化合物的电子式为
(2)由②形成的单质是一种是硬度很大,熔点很高的晶体,则该晶体属于
(3)③④⑤三种元素的第一电离能从大到小排序为
(4)写出工业上冶炼⑥单质的化学方程式
(5)列举元素⑦形成的最高价含氧酸的用途
(6)元素⑧的核外电子排布式为
(7)下图为⑨晶体的晶胞结构。若晶胞的棱长为acm,则两个最近的⑨原子之间的距离是

(8)天津市有着丰富的海水资源,海水中含有丰富的各种元素,化学兴趣小组采用“空气吹出法”从浓海水吹出元素⑩形成的单质Br2,常温下,Br2的颜色为深红棕色液体,吹出的溴用纯碱溶液吸收,吸收溴的主要反应为:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),当吸收1molBr2时,转移电子的物质的量为
 的VSEPR模型名称为
的VSEPR模型名称为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表列出了A~M 13种元素在周期表中的位置:
(1)这些元素中,金属性最强的元素是___________ (填元素符号,下同),非金属性最强的是___________ ,最不活泼的元素是___________ 。
(2)写出H元素的最高价氧化物对应的水合物与J元素氢化物的水溶液反应的离子方程式___________ 。
(3)I2-、J-、L+、M2+等微粒中,半径最大的是___________ ,最小的是___________ 。
(4)A与D形成的化合物A2D2是___________ 化合物,其电子式为___________ 。
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
(2)写出H元素的最高价氧化物对应的水合物与J元素氢化物的水溶液反应的离子方程式
(3)I2-、J-、L+、M2+等微粒中,半径最大的是
(4)A与D形成的化合物A2D2是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X是一种日常生活中常见的金属,它既能与盐酸反应生成X3+和H2,又能与烧碱溶液反应生成XO2-和H2O.X的氢氧化物具有两性,但不与氨水反应;而Zn(OH)2与氨水反应生成[Zn(NH3)4]2+.试回答下列问题:
(1)X元素在元素周期表中的位置是______ 。
(2)X的氧化物也具有两性,写出其溶于烧碱溶液的离子方程式:_______ 。
(3)分离X3+与Zn2+的最佳方法是加入过量的____________ 。
(4)与O同周期的第VA族元素Z形成的最常见氢化物也可表示为ZH3,Z还可形成多种氢化物及其微粒,如Z2H4、Z2H5+、ZH4+等.
①写出Z2H4的电子式:________ 。
工业上利用尿素[CO(NH2)2]、NaClO在NaOH溶液中发生反应生成水合肼(Z2H4·H2O)、Na2CO3等产物,则该反应的化学方程式为_________ 。
查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜。取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在搞完下恰好完全反应生成氮气等产物,写出该反应的化学方程式:_______ 。
②若某一物质组成为Z4H4,则它的一种离子化合物的化学式为______ .
(1)X元素在元素周期表中的位置是
(2)X的氧化物也具有两性,写出其溶于烧碱溶液的离子方程式:
(3)分离X3+与Zn2+的最佳方法是加入过量的
(4)与O同周期的第VA族元素Z形成的最常见氢化物也可表示为ZH3,Z还可形成多种氢化物及其微粒,如Z2H4、Z2H5+、ZH4+等.
①写出Z2H4的电子式:
工业上利用尿素[CO(NH2)2]、NaClO在NaOH溶液中发生反应生成水合肼(Z2H4·H2O)、Na2CO3等产物,则该反应的化学方程式为
查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜。取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在搞完下恰好完全反应生成氮气等产物,写出该反应的化学方程式:
②若某一物质组成为Z4H4,则它的一种离子化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表中位置为_______________ 。
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________ 。
(3)X、Y、Z的原子半径由小到大的顺序为_________________ 。
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为___________________ ,该产物化肥中含有的化学键有________________ 。
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是______ (填元素符号),反应的离子方程式为________________ 。
(1)元素W在周期表中位置为
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为
(3)X、Y、Z的原子半径由小到大的顺序为
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是
您最近一年使用:0次
【推荐2】元素周期表前四周期的元素 、
、 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 、
、 、
、 、
、 四种元素为短周期主族元素。
四种元素为短周期主族元素。 的核外电子总数与其周期序数相同,
的核外电子总数与其周期序数相同, 与
与 同周期,
同周期, 与
与 同族,且
同族,且 能与
能与 化合生成一种可溶性盐,该盐溶液与生石灰共热生成的气体能使湿润的红色石蕊试纸变蓝。
化合生成一种可溶性盐,该盐溶液与生石灰共热生成的气体能使湿润的红色石蕊试纸变蓝。 可用于制备波尔多液。
可用于制备波尔多液。
回答下列问题:
(1)元素 为
为___________ (填元素符号),e的价层电子排布式为___________ ,元素周期表中属于___________ 区元素,其基态原子有___________ 种不同空间运动状态的电子。
(2) 的电子式为
的电子式为 ___________
(3)试比较第一电离能b___________ c(填“>”或“<”)
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序为
三种元素的简单离子半径由大到小的顺序为___________ (填离子符号)。
(5)写出由 、
、 、
、 三种元素组成的离子晶体的化学式:
三种元素组成的离子晶体的化学式:___________ (写一种即可)。用___________ 方法验证物质属于晶体还是非晶体。
(6) 固体为白色,溶于水颜色变蓝,该颜色变化属于
固体为白色,溶于水颜色变蓝,该颜色变化属于________ 变化(填“物理”或“化学”)。
 、
、 、
、 、
、 、
、 的原子序数依次增大,其中
的原子序数依次增大,其中 、
、 、
、 、
、 四种元素为短周期主族元素。
四种元素为短周期主族元素。 的核外电子总数与其周期序数相同,
的核外电子总数与其周期序数相同, 与
与 同周期,
同周期, 与
与 同族,且
同族,且 能与
能与 化合生成一种可溶性盐,该盐溶液与生石灰共热生成的气体能使湿润的红色石蕊试纸变蓝。
化合生成一种可溶性盐,该盐溶液与生石灰共热生成的气体能使湿润的红色石蕊试纸变蓝。 可用于制备波尔多液。
可用于制备波尔多液。回答下列问题:
(1)元素
 为
为(2)
 的电子式为
的电子式为 (3)试比较第一电离能b
(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序为
三种元素的简单离子半径由大到小的顺序为(5)写出由
 、
、 、
、 三种元素组成的离子晶体的化学式:
三种元素组成的离子晶体的化学式:(6)
 固体为白色,溶于水颜色变蓝,该颜色变化属于
固体为白色,溶于水颜色变蓝,该颜色变化属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D、E五种单核微粒:①当A微粒失去3个电子后,电子层结构与氖原子的相同;②B微粒得到一个电子后,其电子层结构与氩原子相同;③C微粒带两个单位正电荷,核电荷数为12;④D微粒18个电子。带两个单位的负电荷;⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出各微粒的符号:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 。
(2)B微粒的结构示意图是_______ ,D微粒的结构示意图是_______ 。
(1)写出各微粒的符号:A
(2)B微粒的结构示意图是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的最外层电子数是次外层电子数的两倍;C的单质燃烧时呈现黄色火焰,C的单质在加热条件下与B的单质反应,可以得到与D单质颜色相同的固态化合物甲;D的最高价与最低价代数和为其最低价绝对值的两倍。据此,回答下列问题:
(1)写出A与B两元素所形成化合物AB2的电子式__________ ,该化合物分子属于______ 分子(极性或非极性)。
(2)用电子式表示形成C2D的形成过程:________________________ 。
(3)C、D两元素还可以形成化合物C2D2,该化合物性质类似于C2B2,试写出C2D2与稀盐酸反应的化学方程式_______________________ 。
(1)写出A与B两元素所形成化合物AB2的电子式
(2)用电子式表示形成C2D的形成过程:
(3)C、D两元素还可以形成化合物C2D2,该化合物性质类似于C2B2,试写出C2D2与稀盐酸反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。其中A与其他元素均不同周期;B的最外层电子数是其内层电子总数的2倍;由C、D组成的化合物D2C和D2C2均为离子晶体;E的内层电子数总和是其最外层电子数的5倍;基态F原子3p轨道上有2个未成对电子且其单质的晶体属于分子晶体。回答下列问题:
(1)基态F的价电子排布式为______ ;D位于第______ 周期______ 族。
(2)与E同周期的元素中,第一电离能小于E的元素有______ (填元素符号)。
(3)BC2分子中,B原子的轨道杂化类型为______ ,BC2属于______ (填“极性”或“非极性”)分子;A2C、A2F中沸点更高的是______ (填化学式),原因是______ ;D与氯元素形成的化合物DCl的熔点比B的氯化物BCl4的熔点高,原因是______ 。
(1)基态F的价电子排布式为
(2)与E同周期的元素中,第一电离能小于E的元素有
(3)BC2分子中,B原子的轨道杂化类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】阅读表中短周期主族元素的相关信息,用化学用语回答下列问题:
(1)E原子的结构示意图___________ ,B离子的电子式___________ ,D最高价氧化物的化学式___________ 。
(2)X的化学式为___________ ,其中含有的化学键种类有___________ 。
(3)A、B两种元素的简单离子的半径大小为___________ (用离子表示)。
(4)A、B两元素组成的化合物 属于
属于___________ 。
A.离子化合物 B.共价化合物
(5)D的单质与水反应的化学方程式为___________ 。
(6)列举一个事实说明D的非金属比E强___________ 。
(7)已知固体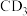 在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物___________ ,因而其为___________ 化合物。
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的3倍 |
| C | 在第3周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(2)X的化学式为
(3)A、B两种元素的简单离子的半径大小为
(4)A、B两元素组成的化合物
 属于
属于A.离子化合物 B.共价化合物
(5)D的单质与水反应的化学方程式为
(6)列举一个事实说明D的非金属比E强
(7)已知固体
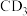 在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)下列变化过程中放出热的是___________ 。
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(2)下列变化:①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氯气溶于水⑥氯化铵受热分解,未发生化学键破坏的是___________ ;仅发生离子键破坏的是___________ 。上述涉及的主要物质为纯净物时,属于共价化合物的是___________ ;属于离子化合物的是___________ 。
(3)Q、W、X、Y、Z为5种短周期元素,且原子序数依次增大。W、X与Y同周期,Y与Z同主族。Q与W可以按照原子个数比4∶1形成化合物甲,且甲分子中含有10个电子。Q与X形成化合物乙,乙可与Z的最高价氧化物对应的水化物按照物质的量之比2∶1反应形成盐丙。甲的电子式是___________ 。Q和Y形成的原子个数之比为1∶1的化合物属于___________ (填“离子”或“共价”)化合物。盐丙中含有的化学键类型为___________ 。
(1)下列变化过程中放出热的是
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(2)下列变化:①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氯气溶于水⑥氯化铵受热分解,未发生化学键破坏的是
(3)Q、W、X、Y、Z为5种短周期元素,且原子序数依次增大。W、X与Y同周期,Y与Z同主族。Q与W可以按照原子个数比4∶1形成化合物甲,且甲分子中含有10个电子。Q与X形成化合物乙,乙可与Z的最高价氧化物对应的水化物按照物质的量之比2∶1反应形成盐丙。甲的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)②的元素符号是______ 。
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤______ ⑥。
(3)①和③两种元素组成的化合物中含有的化学键为________ (填“离子键”或“共价键”)。
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为__________ 。

(1)②的元素符号是
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤
(3)①和③两种元素组成的化合物中含有的化学键为
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下图是元素周期表的一部分:
用化学用语 回答下列问题:
(1)元素⑨在周期表中的位置为_______ 。
(2)④、⑦、⑨的最高价含氧酸的酸性由强到弱的顺序是_______ 。
(3)画这10种元素中,非金属性最强的元素的原子结构示意图_______
(4)①、②、⑥形成的化合物中存在的化学键类型有_______ 。
(5)Y由②⑥⑨三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______ 。
(6)请从原子结构的角度,解释元素⑨的非金属性比元素⑩强的原因_______ 。
| ① | |||||||||||||||||
| ④ | ⑤ | ⑥ | ⑧ | ||||||||||||||
| ② | ③ | ⑦ | ⑨ | ||||||||||||||
| ⑩ | |||||||||||||||||
(1)元素⑨在周期表中的位置为
(2)④、⑦、⑨的最高价含氧酸的酸性由强到弱的顺序是
(3)画这10种元素中,非金属性最强的元素的原子结构示意图
(4)①、②、⑥形成的化合物中存在的化学键类型有
(5)Y由②⑥⑨三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为
(6)请从原子结构的角度,解释元素⑨的非金属性比元素⑩强的原因
您最近一年使用:0次



