阅读表中短周期主族元素的相关信息,用化学用语回答下列问题:
(1)E原子的结构示意图___________ ,B离子的电子式___________ ,D最高价氧化物的化学式___________ 。
(2)X的化学式为___________ ,其中含有的化学键种类有___________ 。
(3)A、B两种元素的简单离子的半径大小为___________ (用离子表示)。
(4)A、B两元素组成的化合物 属于
属于___________ 。
A.离子化合物 B.共价化合物
(5)D的单质与水反应的化学方程式为___________ 。
(6)列举一个事实说明D的非金属比E强___________ 。
(7)已知固体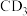 在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物___________ ,因而其为___________ 化合物。
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的3倍 |
| C | 在第3周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(2)X的化学式为
(3)A、B两种元素的简单离子的半径大小为
(4)A、B两元素组成的化合物
 属于
属于A.离子化合物 B.共价化合物
(5)D的单质与水反应的化学方程式为
(6)列举一个事实说明D的非金属比E强
(7)已知固体
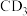 在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
在178℃时升华。再列举一个方法判断其为共价化合物还是离子化合物
更新时间:2024-04-30 08:08:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】随着原子序数的递增,A~G七种短周期主族元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为___________ 。
(2)元素A、F和G的最高价氧化物的水化物酸性由强到弱的顺序为___________ ,若用下图装置验证三者酸性强弱,则分液漏斗中所盛放的试剂为___________ ,装置B中观察到的现象为___________ 。(已知硅酸为白色胶状沉淀,B中为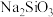 溶液)
溶液)
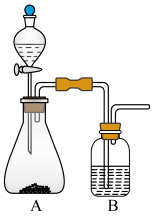
(3)元素E的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是___________ 。
(4)元素C与D按原子个数比1:1形成的化合物中所含的化学键类型有___________ 。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)元素A、F和G的最高价氧化物的水化物酸性由强到弱的顺序为
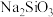 溶液)
溶液)
(3)元素E的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是
(4)元素C与D按原子个数比1:1形成的化合物中所含的化学键类型有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:__________ 种不同空间运动状态。⑨号元素在周期表中的位置是__________ ,基态时其最高能层的电子占据的原子轨道电子云轮廓为__________ 形。第二周期所有元素中第一电离能介于①②之间的有__________ 种。基态⑩原子的简化电子排布式__________ ,该元素位于__________ 区。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式__________ ,该分子为__________ (填“极性”或“非极性”)分子。
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
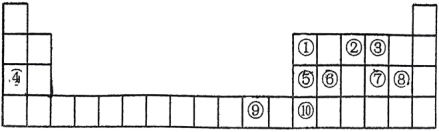
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
| A.非金属性:②>③ |
| B.气态最简单氢化物的稳定性:③>⑦ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ |
| D.最简单氢化物的沸点:③>⑦ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某校化学实验小组学生为了验证非金属元素氯的非金属性强于硫和氮,设计了一套实验装置如图(已知氯气能把氨气氧化生成氮气和氯化氢)。
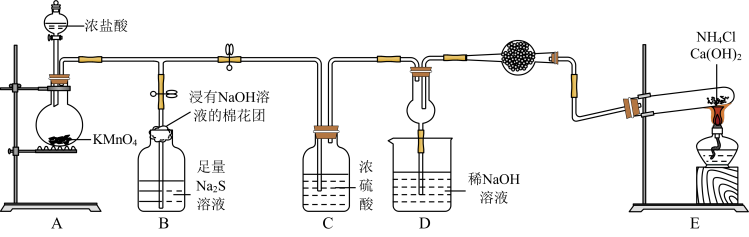
回答下列问题:
(1)配平A中反应的化学方程式:_______ _______HCl(浓)+_______KMnO4=_______MnCl2+_______KCl+_______Cl2↑+_______ H2O。该反应中氧化剂与还原剂物质的量之比为_______ 。
(2)B中浸有NaOH溶液的棉花团的作用为_______ ;B中的现象为_______ ,由该现象得非金属性:Cl>>S。
(3)E中反应化学方程式为_______ 。
(4)D中出现白烟,涉及的反应化学方程式为_______ 、_______ 。
(5)有同学认为D中的现象并不能说明氯的非金属性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂为_______ (填名称)。
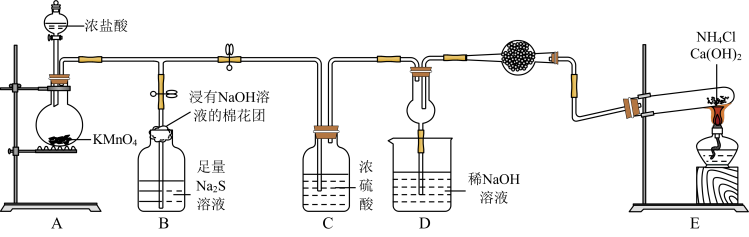
回答下列问题:
(1)配平A中反应的化学方程式:
(2)B中浸有NaOH溶液的棉花团的作用为
(3)E中反应化学方程式为
(4)D中出现白烟,涉及的反应化学方程式为
(5)有同学认为D中的现象并不能说明氯的非金属性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】下图是依据各种元素(原子)的性质与原子序数(1~20)的关系而绘制出来的,各图的纵轴可能代表下列某一性质:核电荷数,中子数、最高正化合价、原子半径、得电子能力,A、B、C分别代表三种元素.(注意:图3中原子序数为8、9的元素和图4中原子序数为2、10、18的元素在纵轴上没有对应的数值.)
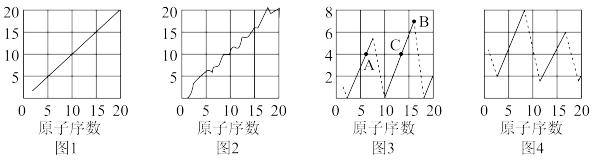
请回答下列问题:
(1)图2的纵轴代表的性质是______ ,图4的纵轴代表的性质是______ .
(2)A元素的最低负化合价为______ .
(3)B、C两种元素形成的化合物中,C显最高正化合价而B显最低负化合价,该化合物的化学式为______ .
(4)1~20号元素中,原子(稀有气体元素原子除外)半径最大的是__ (填元素符号)
(5)写出B的单质与NaOH溶液反应的离子方程式:____________________ .
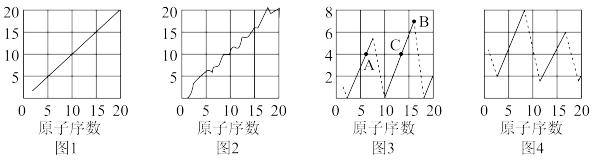
请回答下列问题:
(1)图2的纵轴代表的性质是
(2)A元素的最低负化合价为
(3)B、C两种元素形成的化合物中,C显最高正化合价而B显最低负化合价,该化合物的化学式为
(4)1~20号元素中,原子(稀有气体元素原子除外)半径最大的是
(5)写出B的单质与NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素 、
、 、
、 、
、 、
、 的原子序数依次增大,且位于三个周期,
的原子序数依次增大,且位于三个周期, 是地壳中含量最多的元素,Z、
是地壳中含量最多的元素,Z、 是金属元素且形成的最高价氧化物对应的水化物可以发生反应,
是金属元素且形成的最高价氧化物对应的水化物可以发生反应, 是同周期中原子半径最小的元素。
是同周期中原子半径最小的元素。
回答下列问题:
(1) 在周期表中的位置是
在周期表中的位置是_________ , 的最简单氢化物的结构式为
的最简单氢化物的结构式为_________ 。
(2) 的最高价氧化物对应水化物的电子式为
的最高价氧化物对应水化物的电子式为_________ ; 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为
___________________________ (用相应离子符号表示)。
(3)举例说明金属性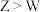 :
:____________________________________ ,写出 的最高价氧化物对应水化物与强碱反应的离子方程式:
的最高价氧化物对应水化物与强碱反应的离子方程式:____________________________________ 。
 、
、 、
、 、
、 、
、 的原子序数依次增大,且位于三个周期,
的原子序数依次增大,且位于三个周期, 是地壳中含量最多的元素,Z、
是地壳中含量最多的元素,Z、 是金属元素且形成的最高价氧化物对应的水化物可以发生反应,
是金属元素且形成的最高价氧化物对应的水化物可以发生反应, 是同周期中原子半径最小的元素。
是同周期中原子半径最小的元素。回答下列问题:
(1)
 在周期表中的位置是
在周期表中的位置是 的最简单氢化物的结构式为
的最简单氢化物的结构式为(2)
 的最高价氧化物对应水化物的电子式为
的最高价氧化物对应水化物的电子式为 、
、 、
、 的简单离子半径由大到小的顺序为
的简单离子半径由大到小的顺序为(3)举例说明金属性
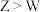 :
: 的最高价氧化物对应水化物与强碱反应的离子方程式:
的最高价氧化物对应水化物与强碱反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请回答下列问题:
(1)写出:X的原子结构示意图___________ ,R离子的电子式___________ ,Y在周期表中的位置___________ 。
(2)X、Y、Z三种元素形成的化合物属于___________ 化合物(填“离子”或“共价”),其电子式为___________ 。
(3)Z在Y单质中燃烧的产物电子式为___________ ,含有的化学键类型为___________ ,
(4)Y、Z、W、R形成的简单离子半径由大到小顺序为___________ 。(写具体离子符号)
(5)W单质与Z的高价氧化物对应的水化物反应的离子方程式为___________ 。
(1)写出:X的原子结构示意图
(2)X、Y、Z三种元素形成的化合物属于
(3)Z在Y单质中燃烧的产物电子式为
(4)Y、Z、W、R形成的简单离子半径由大到小顺序为
(5)W单质与Z的高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是______ (用元素符号表示)。
②M2Z中含有的化学键类型为__________ 。
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是_____ (写化学式)。
④GQ3溶液与过量的MZX溶液反应的化学方程式为________ 。
⑤常温下,不能与G的单质发生反应的是______ (填序号)。
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置_______ 。
②关于铷的下列说法中不正确的是________ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是___________________ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_______________ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________________ 。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是
②M2Z中含有的化学键类型为
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是
④GQ3溶液与过量的MZX溶液反应的化学方程式为
⑤常温下,不能与G的单质发生反应的是
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置
②关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W核电荷数为26,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)写出下列元素的名称X_______ ,Y_______ ,Z_______ ,W_______ 。
(2)X-H和Y-H属于极性共价键,其中极性较强的是_______ (X、Y用元素符号表示)。X的第一电离能比Y的_______ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:_______ 。
(4)W的基态原子的电子排布式为_______ 。
(5)Y元素的核外电子轨道表示式为_______ 。
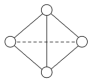
(6)已知一种Y4分子结构如图所示:_______ (填“吸收”或“放出”)_______ kJ。
(1)写出下列元素的名称X
(2)X-H和Y-H属于极性共价键,其中极性较强的是
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:
(4)W的基态原子的电子排布式为
(5)Y元素的核外电子轨道表示式为
(6)已知一种Y4分子结构如图所示:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E为前四周期元素,原子序数依次增大,A为短周期中离子半径最小的金属元素,B为短周期中金属性最强的元素,C元素的单质是一种淡黄色固体,D元素的基态原子在前四周期中未成对电子数最多。E位于元素周期表中第八列。
回答下列问题:
(1)B在焰色反应中发出黄光是一种______ (填字母)。
A.发射光谱 B.吸收光谱
(2)D元素在元素周期表中的位置为______ ,在同周期中,与D元素基态原子具有相同最外层电子数的元素为______ (填元素符号)。
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,这种相似性被称为对角线规则。请写出A元素与B元素最高价氧化物的水化物反应的离子方程式______ ,已知A元素与Cl元素的电负性分别为1.5和3.0,则它们所形成的化合物为______ (填“离子化合物”或“共价化合物”)。
(4)某同学画出C元素基态原子的价层电子轨道表示式为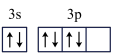 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了______ 。C原子能量最高的电子其电子云形状是______ 。
(5)写出E元素基态原子的电子排布式______ ,其两种简单离子中,更加稳定的是______ (填离子符号),理由是______ 。
回答下列问题:
(1)B在焰色反应中发出黄光是一种
A.发射光谱 B.吸收光谱
(2)D元素在元素周期表中的位置为
(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,这种相似性被称为对角线规则。请写出A元素与B元素最高价氧化物的水化物反应的离子方程式
(4)某同学画出C元素基态原子的价层电子轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(5)写出E元素基态原子的电子排布式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________ ;(用化学式表示)
(2)写出③形成的单质的结构式:____________________ ;
写出②的最高价氧化物的电子式:____________________ ;
写出⑧的最高价氧化物水化物的晶体类型:_______________________ ;
(3)写出工业制备⑦单质的化学方程式:_______________________ ;
(4)元素②和⑧的非金属性强弱,②的非金属性________ 于⑧(填“强”或“弱”),并用化学方程式证明上述结论_______________________ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)写出③形成的单质的结构式:
写出②的最高价氧化物的电子式:
写出⑧的最高价氧化物水化物的晶体类型:
(3)写出工业制备⑦单质的化学方程式:
(4)元素②和⑧的非金属性强弱,②的非金属性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表列出了部分前20号元素的一些性质:
下列问题用元素符号及化学式回答:
(1)②在周期表中的位置是___________ 。
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为___________ 。由①⑨组成的分子中,共含有18e-的化合物结构式为___________ 。
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为___________ 。
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为___________ 。
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 0.37 | 2.27 | 0.74 | 1.52 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +1 | +4 | +5 | +7 | +1 | - | |
| 最低价态 | -1 | - | -2 | - | -4 | -3 | -1 | - | -1 |
(1)②在周期表中的位置是
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】几种短周期元素的原子半径及主要化合价如下表:已知 X 是短周期中最活泼的金属,且与 R 同周期。(请用化学用语答题)
(1)M 在元素周期表中的位置为___________ 。
(2)X 与 Y 按原子个数比 1∶1 构成的物质的电子式为___________ ;所含化学键类型为___________ 。
(3)X+、 Y2-、M2-离子半径从大到小的顺序为___________ 。
(4)将 YM2 通入 FeCl3 溶液中的离子方程式:___________ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6,—2 | +5,—3 | —2 | +3 |
(2)X 与 Y 按原子个数比 1∶1 构成的物质的电子式为
(3)X+、 Y2-、M2-离子半径从大到小的顺序为
(4)将 YM2 通入 FeCl3 溶液中的离子方程式:
您最近一年使用:0次



