1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是______ (用元素符号表示)。
②M2Z中含有的化学键类型为__________ 。
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是_____ (写化学式)。
④GQ3溶液与过量的MZX溶液反应的化学方程式为________ 。
⑤常温下,不能与G的单质发生反应的是______ (填序号)。
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置_______ 。
②关于铷的下列说法中不正确的是________ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是___________________ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_______________ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________________ 。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是
②M2Z中含有的化学键类型为
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是
④GQ3溶液与过量的MZX溶液反应的化学方程式为
⑤常温下,不能与G的单质发生反应的是
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置
②关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
更新时间:2020-08-22 17:12:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z 是原子序数依次增大的同一短周期主族元素,W、X是金属元素,它们的最高价氧化物对应的水化物可以反应生成盐和水,Y、Z 是非金属元素。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为_______ 。
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为_______ 。
(3)比较 Y、Z 气态氢化物的稳定性:_______ >_______ (用化学式表示)。
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是_______ >_______ >_______ >_______ 。
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:_______ 。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为
(3)比较 Y、Z 气态氢化物的稳定性:
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16,单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答:

(1)Y2的电子式是__________ ;该分子中有______ 个σ键,______ 个π键。
(2)甲属于(填“极性”或“非极性”)______ 分子;晶体中甲分子的配位数为_______ 。
(3)乙分子的VSEPR模型名称为_________ ,分子的立体构型名称为__________ 。
(4)写出乙与Z2反应生成丙的化学方程式____________________ 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式:________________ ,氧化剂为_________ 。

(1)Y2的电子式是
(2)甲属于(填“极性”或“非极性”)
(3)乙分子的VSEPR模型名称为
(4)写出乙与Z2反应生成丙的化学方程式
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素,它们的核电荷数依次增大。已知:A失去一个电子后就成为一个质子;B有两个电子层,其最外层的电子数是次外层电子数的2倍;C的L层得2个电子后成为稳定结构;D是海水中含量第一位的金属元素;E的最外层电子比次外层电子少一个。请填写下列空格:
(1)A形成的单质的结构式为______ ; BC2的电子式_______________ 。
(2)D离子的结构示意图_________ ,D、E结合形成的化合物的电子式_____
(3)B、C、D三种元素可形成一种化合物,其化学式为_____ ,所含的化学键有____
(1)A形成的单质的结构式为
(2)D离子的结构示意图
(3)B、C、D三种元素可形成一种化合物,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D、E五种短周期元素, 它们的原子序数由A到E依次增大,已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D为原子核内有12个中子的二价金属,当2 .4克D与盐酸反应时,在标准状况下放出气体2.24L。
试根据以上叙述回答:
(1)写出元素名称:A_____ E____ ,写出D的原子符号____ (标出质子数和质量数)
(2)画出C的原子结构示意图_________ 。
(3)写出AB2与C2B2反应的化学方程式___________ 。
(4)比较B和E的气态氢化物的稳定性(用化学式回答):________ 。
(5)判断C元素和D元素的金属性强弱,简要地说明你的一个判断依据:________________ 。
试根据以上叙述回答:
(1)写出元素名称:A
(2)画出C的原子结构示意图
(3)写出AB2与C2B2反应的化学方程式
(4)比较B和E的气态氢化物的稳定性(用化学式回答):
(5)判断C元素和D元素的金属性强弱,简要地说明你的一个判断依据:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A~H 均为短周期元素、请回答下列问题:

(1)F元素在周期表中的位置为________ ,A 和D形成的既有极性键又有非极性键的化合物,其电子式为________ 。
(2)D、E、G、H 的简单离子半径由大到小的顺序为(写化学式)________ 。
(3)用电子式表示出E、H 两种元素组成的化合物的形成过程________ 。
(4)用乙图装置证明酸性:HCl>H2CO3>H2SiO3,则溶液b为________ ;溶液c中的离子方程式为________ 。下列事实可用于比较元素碳与Cl 非金属性相对强弱的是________ 。
a.最高正化合价Cl>C
b.C1的氢化物比C 的简单氢化物稳定
C.C1的氢化物比C 的简单氢化物沸点高
d.最高价氧化物的水化物的酸性:HClO4>H2CO3
(5)A和D形成为18电子分子与A和G形成的13电了分子按4 :1的个数比反应的离子方程式为________ 。

(1)F元素在周期表中的位置为
(2)D、E、G、H 的简单离子半径由大到小的顺序为(写化学式)
(3)用电子式表示出E、H 两种元素组成的化合物的形成过程
(4)用乙图装置证明酸性:HCl>H2CO3>H2SiO3,则溶液b为
a.最高正化合价Cl>C
b.C1的氢化物比C 的简单氢化物稳定
C.C1的氢化物比C 的简单氢化物沸点高
d.最高价氧化物的水化物的酸性:HClO4>H2CO3
(5)A和D形成为18电子分子与A和G形成的13电了分子按4 :1的个数比反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有部分元素的性质与原子(或分子)结构如下表:
(1)元素T在元素周期表中的位置是________ 。
(2)元素Y与元素Z相比,金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是______ (填序号)。
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
(3)上述四种元素中有2种元素能形成一种淡黄色的固体,该化合物的电子式是________ ,所含化学键的类型有________ 。
(4)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素形成的化合物W气态时的密度与氧气相等(同温同压),Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式________ 。
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
(2)元素Y与元素Z相比,金属性较强的是
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
(3)上述四种元素中有2种元素能形成一种淡黄色的固体,该化合物的电子式是
(4)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素形成的化合物W气态时的密度与氧气相等(同温同压),Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号:X__ 、Z__ 。
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的化学键属于__ 键;含有离子键和共价键的化合物的化学式为__ 。
(3)由X、Y、Z所形成的常见离子化合物是__ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为__ 。X与W形成的化合物与水反应时,水是__ (填“氧化剂”或“还原剂”)。
(4)用电子式表示W与Z形成W2Z化合物的过程:__ 。
(5)Q与Z同主族,位于第4周期,其原子序数为__ 。
(1)X、Z两种元素的元素符号:X
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的化学键属于
(3)由X、Y、Z所形成的常见离子化合物是
(4)用电子式表示W与Z形成W2Z化合物的过程:
(5)Q与Z同主族,位于第4周期,其原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可与A形成10电子分子,B、C位于同一周期,二者可以形成多种共价化合物,C、F位于同一主族元素,B元素原子最外电子层的P能级上的电子处于半满状态,C元素原子的最外层电子数是内层电子总数的3倍,E元素原子最外层电子数比最内层电子数多1。
请回答下列问题:
(1)E元素基态原子的电子排布式为___ 。
(2)F元素原子的价电子轨道表示式为___ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的化学式为___ 。
(4)离子半径:D+___ (填“<”“>”或“=”,下同)B3-,第一电离能:B___ C,电负性:C___ F。
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1:1,X的电子式为___ ,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:___ 。
请回答下列问题:
(1)E元素基态原子的电子排布式为
(2)F元素原子的价电子轨道表示式为
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的化学式为
(4)离子半径:D+
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1:1,X的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q为四种短周期元素,X的M电子层有1个电子,Y的最外层电子数为内层电子数的2倍,Z的最高化合价为最低化合价绝对值的3倍,Z与Q同周期,Q的原子半径小于Z。回答下列问题:
(1)Z在周期表中的位置为_______ ,Y与Z形成的化合物的电子式为_______ 。
(2)Q的核外电子排布式为_______ , 为含
为含_______ 键的_______ 分子。(填“极性”或“非极性”)
(3)实验室制备Q单质的化学方程式为_______ ;X的某种化合物可用于Q单质的尾气处理,该反应的离子方程式为_______ 。
(4)设计一个简单的实验方案,证明非金属性Q大于Z_______ 。
(1)Z在周期表中的位置为
(2)Q的核外电子排布式为
 为含
为含(3)实验室制备Q单质的化学方程式为
(4)设计一个简单的实验方案,证明非金属性Q大于Z
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_______ 。
(2)地壳中含量最多的金属元素是_______ ,写出元素⑥的简单气态氢化物的化学式_______ 。
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是_______ ,呈两性的氢氧化物是_______ 。
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是_______ 。
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如右图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:
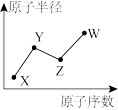
(1)写出四种元素的元素符号:X____ Y____ Z____ W____
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确___ ,说明理由__________________________________ 。
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为________ ;化合物乙是一种常见的强酸,会因保存不当而变成黄色液体,其原因是_______________________________ 。把红热的木炭投入黄色液体,剧烈反应,方程式为_____________________ ,将产生的气体通过澄清石灰水时气体变为无色,但未见有浑浊现象,原因是______________ 。(写出有关反应的化学方程式)

(1)写出四种元素的元素符号:X
(2)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确
(3)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有漂白消毒杀菌作用,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表。J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
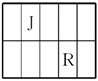
(1)M的离子结构示意图为________ ;元素T在周期表中位于第________ 族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为_____________________ 。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为________________________________________________________________________ 。
(4)L的最简单气态氢化物甲的水溶液显碱性。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____________________________ 。

(1)M的离子结构示意图为
(2)J和氢组成的化合物分子有6个原子,其结构简式为
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为
(4)L的最简单气态氢化物甲的水溶液显碱性。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近一年使用:0次



