已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号:X__ 、Z__ 。
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的化学键属于__ 键;含有离子键和共价键的化合物的化学式为__ 。
(3)由X、Y、Z所形成的常见离子化合物是__ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为__ 。X与W形成的化合物与水反应时,水是__ (填“氧化剂”或“还原剂”)。
(4)用电子式表示W与Z形成W2Z化合物的过程:__ 。
(5)Q与Z同主族,位于第4周期,其原子序数为__ 。
(1)X、Z两种元素的元素符号:X
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的化学键属于
(3)由X、Y、Z所形成的常见离子化合物是
(4)用电子式表示W与Z形成W2Z化合物的过程:
(5)Q与Z同主族,位于第4周期,其原子序数为
更新时间:2020-05-12 16:13:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。部分元素在周期表中的位置如图:
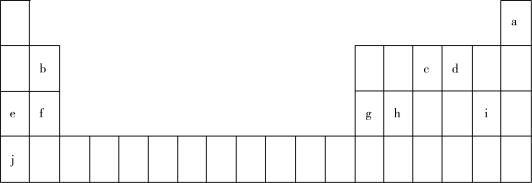
(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为_______ 。
②经分析,月壤中含有大量的元素d和h,原子半径d_______ h(填“>”、“<”或“=”),元素h在周期表中的位置为_______ 。
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为_______ ,用电子式表示f原子与i原子形成化合物的形成过程:_______ 。
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为_______ 。
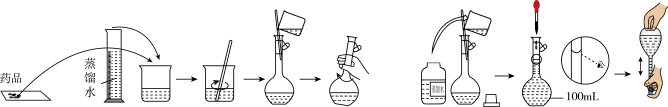
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为_______ 。实验室按照如图操作配制该溶液,所得溶液浓度_______ (填“偏大”或“偏小”)。
(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式_______ 。

(1)2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相,对月壤中化学元素的分析有助于认识月球表面环境。
①月壤中含有较丰富的质量数为3的a,它可以作为未来核聚变的重要原料之一,a的这种核素表示为
②经分析,月壤中含有大量的元素d和h,原子半径d
(2)e和f的单质都是化学家戴维通过电解的方法首次制得。e的单质与水反应的化学方程式为
(3)d和i两种元素的简单氢化物中,熔沸点较高的氢化物的电子式为
(4)《天工开物》记载,“凡火药,以硝石、硫磺为主,草木灰为辅”,由c、d、j三种元素组成的化合物是硝石的主要成分,化学式为

(5)元素b与g的性质相似,可以预测b与g的单质或化合物也可能具有相似的性质。请写出b的最高价氧化物对应水化物与e的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,表中的每个编号代表一种元素。请根据要求回答问题:
(1)元素①③④组成的化合物的化学式是_____________ ,其属于________________ (填“离子化合物”或“共价化合物”)。
(2)元素⑤的离子结构示意图是__________________ 。
(3)元素⑥、⑦的氢化物稳定性比较:__________________ (填化学式):元素②、③、④的原子半径比较:__________________ (填元素符号)。
(4)元素④、⑦组成的化合物的电子式为____________________ 。
(5)元素④的单质与水反应的化学方程式为__________________________ 。
| 周期族 | ⅠA | ⅡA | ⅢB~ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ||||||||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(2)元素⑤的离子结构示意图是
(3)元素⑥、⑦的氢化物稳定性比较:
(4)元素④、⑦组成的化合物的电子式为
(5)元素④的单质与水反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为八种短周期主族元素的部分性质(已知铍的原子半径为0.89×10-10m):
(1)元素M在元素周期表中的位置为_________________________ 。
(2)写出X、Y、J三种元素形成的化合物电子式_________ 。用电子式表示X元素与Z元素形成化合物的过程:_______________________ 。
(3)写出Y与Q两种元素形成的化合物与J的最高价氧化物的水化物反应的离子方程式_____ 。
(4)R与T相比,非金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是_______ (填字母)。
A.常温下T的单质呈固态,R的单质呈气态
B.R的氢化物比T的氢化物稳定
C.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
D.R与T形成的化合物中T呈正价
(5)J与Q相比,金属性较强的是____ (用元素符号表示),能证明这一结论的依据是______ 。
(6)根据表中数据推测,M的原子半径的最小范围是____________________ 。
| 元素代号 | X | Y | Z | M | R | J | Q | T |
| 原子半径/10-10m | 0.74 | 0.75 | 0.99 | 1.86 | 1.43 | 1.10 | ||
| 主要化合价 | -2 | +5、-3 | +4、-4 | +7、-1 | +1 | +3 | +5、-3 | |
| 其它 | 原子核内无中子 | 无机非金属材料主角 | 有两种氧化物 |
(2)写出X、Y、J三种元素形成的化合物电子式
(3)写出Y与Q两种元素形成的化合物与J的最高价氧化物的水化物反应的离子方程式
(4)R与T相比,非金属性较强的是
A.常温下T的单质呈固态,R的单质呈气态
B.R的氢化物比T的氢化物稳定
C.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
D.R与T形成的化合物中T呈正价
(5)J与Q相比,金属性较强的是
(6)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A元素原子的最外层电子数是次外层电子数的2倍,E的最高化合价和最低化合价的代数和为4,C与E同主族,D单质可用于焊接钢轨。请回答下列问题:
(1)C、D、E的原子半径由大到小的顺序为______ (填元素符号)。
(2)元素A在元素周期表中的位置是_______ 。
(3)C和E分别对应的氢化物的沸点较高的是_______ (填分子式)。
(4)元素E与元素F相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ (填选项序号)。
a.常温下E的单质和F的单质状态不同
b.F的氢化物比E的氢化物稳定
c.一定条件下E和F的单质都能与钠反应
d.E的最高价含氧酸酸性弱于F的最高价含氧酸
(5)E元素和F元素以原子个数比1:1 形成化合物G,G的结构式为________ 。已知G是一种黄色油状液体,常温下遇水易反应,产生的气体与E单质完全燃烧的产物相同,且溶液出现浑浊。请写G与水反应的化学方程式_______ 。
(1)C、D、E的原子半径由大到小的顺序为
(2)元素A在元素周期表中的位置是
(3)C和E分别对应的氢化物的沸点较高的是
(4)元素E与元素F相比,非金属性较强的是
a.常温下E的单质和F的单质状态不同
b.F的氢化物比E的氢化物稳定
c.一定条件下E和F的单质都能与钠反应
d.E的最高价含氧酸酸性弱于F的最高价含氧酸
(5)E元素和F元素以原子个数比1:1 形成化合物G,G的结构式为
您最近一年使用:0次
【推荐2】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)在元素周期表中M位于_____ 区,基态M原子的价层电子排布图为_____ ,第四能层s轨道上电了数目和M元素相同的元素还有_____ (填元素符号)。
(2)元素Y基态原子的核外电子排布式为_______ ,其同周期元素中,第一电离能最大的是____ (写元素符号)。元素Y的含氧酸中,酸性最强的是_____ (写化学式),该酸根离子的立体构型为_______ 。
(3)Z与元素Y同主族,在该族中原子序数最小,Z的气态氢化物的稳定性大于Y的气态氢化物的稳定性,原因是__________ ,Z的气态氢化物的沸点大于Y的气态氢化物的沸点,原因是_____ 。
(1)在元素周期表中M位于
(2)元素Y基态原子的核外电子排布式为
(3)Z与元素Y同主族,在该族中原子序数最小,Z的气态氢化物的稳定性大于Y的气态氢化物的稳定性,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)①B元素的原子结构示意图是____ 。
②D元素原子的最外层价电子排布式是____ 。
③A2B形成的分子中心原子的杂化轨道类型是:____ 。
④C元素原子的轨道表示式是____ 。
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示)____ 。
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式____ ;用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因____ 。
(1)①B元素的原子结构示意图是
②D元素原子的最外层价电子排布式是
③A2B形成的分子中心原子的杂化轨道类型是:
④C元素原子的轨道表示式是
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是(用化学式表示)
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________ ;五种元素的原子半径从大到小的顺序是____________________ (用元素符号表示)。
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___ ,B的分子式为____________ 。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______ ,其最高价氧化物对应的水化物化学式为_______ 。
回答下列问题:
(1)L的元素符号为
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有部分短周期元素的性质或原子结构如下:
(1)X的无中子原子的符号为____________ ,Y的原子结构示意图为_____________ ,Q在元素周期表中的位置为___________________ 。
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______________________ (用化学式表示),写出两者反应的离子方程式:__________________________________________ 。
(3)M、W两种元素中非金属性较强的是______________ (用元素符号表示),下列表述中能证明这一事实的____________________ (填序号),
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
| 元素 | 元素的性质或原子结构 |
| X | 该元素的一种原子无中子 |
| Y | 原子半径最大的短周期元素 |
| Z | 第三周期元素中简单离子半径最小 |
| M | 地壳中含量最多的元素 |
| Q | 其氧化物是光导纤维的基本原料 |
| W | 其核电荷数为M元素核电荷数的2倍 |
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)M、W两种元素中非金属性较强的是
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知有五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所有离子的电子数都相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)C、D两种元素的名称分别为_______ 、_______ 。
(2)A,B,C离子半径从大到小的顺序_______ (用具体离子符号表示)。
(3)写出D元素形成的单质的结构式:_______ 。
(4)比较B、D氢化物的稳定性:_______ (用化学式表示)。
(5)A、B两种元素组成的化合物A2B2属于_______ (填“离子”或“共价”)化合物,存在的化学键类型是_______ ;写出A2B2与水反应的化学方程式:_______ 。
(6)D元素的最高价氧化物对应水化物的稀溶液与Cu反应的离子方程式:_______ 。
(1)C、D两种元素的名称分别为
(2)A,B,C离子半径从大到小的顺序
(3)写出D元素形成的单质的结构式:
(4)比较B、D氢化物的稳定性:
(5)A、B两种元素组成的化合物A2B2属于
(6)D元素的最高价氧化物对应水化物的稀溶液与Cu反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、 F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
(1) B元素名称为____ ,A与C以原子个数比为1:1形成的化合物的电子式为___ ,用电子式表示C与E形成化合物的过程____ 。
(2)DG形成的化合物是由____ (极性或非极性)键形成的分子,电子式为_____ 。
(3) 非金属性D____ E(填大于或小于),请从原子结构的角度解释原因:_____ 。
| 元素 | 有关性质或结构信息 |
A | 宇宙中含量最多的元素 |
B | 金属B能与NaOH溶液反应,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(2)DG形成的化合物是由
(3) 非金属性D
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
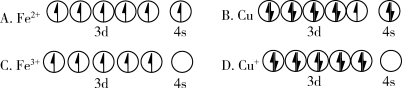
(2)CuFeS2中存在的化学键类型是________________ 。下列基态原子或离子的价层电子排布图正确的_____________ 。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是______ ,中心原子杂化类型为__________ ,属于_______ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是____________________ 。
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为_____ ,共价键的类型有_________ 。
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为__________ ,S2-的配位数为____________ 。
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是________ g•cm-3(列出计算式)。
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(2)CuFeS2中存在的化学键类型是

(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有三种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于___________ 。
(2)B的最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(3)元素D的非金属性比元素A的强,用原子结构解释原因___________ 。
(4)已知硒 与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是___________ 。
a. 的最低负化合价为-2价 b.
的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性
c. 的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
| 元素 | 相关信息 |
| A | -2价阴离子的电子层结构与 原子相同 原子相同 |
| B | 单质的焰色反应为黄色 |
| D | 单质是黄绿色气体,可用于自来水消毒 |
(1)A在周期表中位于
(2)B的最高价氧化物对应的水化物中含有的化学键类型为
(3)元素D的非金属性比元素A的强,用原子结构解释原因
(4)已知硒
 与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是a.
 的最低负化合价为-2价 b.
的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性c.
 的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
您最近一年使用:0次



