元素周期表的一部分如下表,根据该表回答下列问题:
(1)②③④分别与①形成含有10个电子的分子的化学式依次为___________ 、___________ 、___________ 。
(2)上述元素中,非金属性最强的元素是___________ (填元素符号),最高价氧化物对应水化物的酸性最强的是___________ (填酸的化学式)。
(3)⑤的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为___________ ,该反应中产生标准状况下22.4L的气体时,转移的电子的数目为___________ (用含NA的代数式表示)。
(4)在加热条件下,⑥的氢化物的浓溶液与MnO2反应可制得⑥的单质,该反应中,氧化剂与还原剂的物质的量之比为___________ ,将①的单质在⑥的单质中点燃,可观察到的现象为___________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ |
(2)上述元素中,非金属性最强的元素是
(3)⑤的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为
(4)在加热条件下,⑥的氢化物的浓溶液与MnO2反应可制得⑥的单质,该反应中,氧化剂与还原剂的物质的量之比为
更新时间:2022-01-01 21:19:40
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表为长式周期表的一部分,编号代表对应元素。
回答下列问题:
(1)基态原子⑨核外电子排布式为____ ,核外电子总共有___ 种运动状态,电子占据的能最量高轨道的形状为__ 。
(2)在标号的主族元素中,第一电离能最小的是__ (填元素符号,下同),电负性最大的是__ 。
(3)表中元素⑪三价离子的价电子轨道表示式为____ ,该元素属于____ 区元素。
(4)④、⑧元素的简单氢化物为NH3、PH3,请对比沸点:NH3______ PH3,水溶性:NH3_______ PH3(填“<”、“>”或“=”)。
(5)由元素①⑤⑨可组成化合物HClO,O原子的杂化轨道类型为______ 。
(6)元素①⑦能形成阴离子[AlH4]-,其空间构型为______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||||||||||||
| ⑪ |
(1)基态原子⑨核外电子排布式为
(2)在标号的主族元素中,第一电离能最小的是
(3)表中元素⑪三价离子的价电子轨道表示式为
(4)④、⑧元素的简单氢化物为NH3、PH3,请对比沸点:NH3
(5)由元素①⑤⑨可组成化合物HClO,O原子的杂化轨道类型为
(6)元素①⑦能形成阴离子[AlH4]-,其空间构型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】几种主族元素在周期表中的位置如下
根据上表回答下列问题:
(1)⑥元素的氢化物是_______ (填化学式)。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式),①与水反应的化学方程式为_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母,下同)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是_______ 。

族 周期 | I A | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ |
(1)⑥元素的氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与⑤元素形成的分子可能是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,其中每个数字编号代表一种短周期元素。
请按要求回答下列问题:
(1)元素①的元素符号 是___________ ;元素②的元素名称 是___________ 。
(2)元素⑤处于周期表中第___________ 周期第___________ 族。
(3)①~⑦七种元素中原子半径最大 的是___________ (填元素符号)。②③④三种元素的最简单氢化物中最稳定 的是___________ (填化学式)。
(4)元素③和元素⑦的氢化物均极易溶于水,且二者能反应产生大量白烟,写出该反应的化学方程式 ___________ 。
(5)元素⑥的最高价氧化物对应的水化物是一种两性氢氧化物,该物质与元素⑦的最高价氧化物对应水化物反应的离子方程式 为___________ 。
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ |
(1)元素①的
(2)元素⑤处于周期表中第
(3)①~⑦七种元素中原子半径
(4)元素③和元素⑦的氢化物均极易溶于水,且二者能反应产生大量白烟,写出该反应的
(5)元素⑥的最高价氧化物对应的水化物是一种两性氢氧化物,该物质与元素⑦的最高价氧化物对应水化物反应的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】按要求回答下列问题
(1) 空间构型呈:
空间构型呈:___________ (用文字描述);HClO的结构式:___________ 。
(2)写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:___________ 。
(3)用单线桥法标出下列反应电子转移的方向和数目:___________ 。
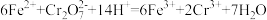
(4)用一个离子方程式说明Cl与S非金属性的相对强弱:___________ 。
(1)
 空间构型呈:
空间构型呈:(2)写出
 在水溶液中的电离方程式:
在水溶液中的电离方程式:(3)用单线桥法标出下列反应电子转移的方向和数目:
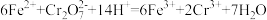
(4)用一个离子方程式说明Cl与S非金属性的相对强弱:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X原子的L层电子数为5,Z单质与 在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
(1)元素X为___________ (填名称),Y在元素周期表中的位置为___________ 。
(2)X、Z简单气态氢化物之间反应的化学方程式为___________ 。
(3)Y、W非金属性较强的是___________ (填元素符号);W简单气态氢化物的电子式为___________ 。
(4)Q的最高价氧化物对应水化物属于___________ (填“共价化合物”或“离子化合物”)。
 在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:
在暗处能剧烈化合并发生爆炸,W与Y同主族。回答下列问题:(1)元素X为
(2)X、Z简单气态氢化物之间反应的化学方程式为
(3)Y、W非金属性较强的是
(4)Q的最高价氧化物对应水化物属于
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语 回答下列问题。
(1)元素①的原子结构示意图为________ 。
(2)元素③和⑤可形成化合物,用电子式表示其形成过程______ 。
(3)元素②、③形成离子的半径_____ >______ 。
(4) 元素③、④形成的最高价氧化物水化物的碱性__ >____ 。
(5)元素⑥的单质与元素③⑨组成的化合物的水溶液反应的离子方程式为___ 。请从原子结构的角度解释该反应能发生的原因:____ 。
(6)某同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成①、⑦、⑧的非金属性强弱比较的实验研究;从以下所给物质中选出实验所需的物质:a.稀HNO3 b.稀盐酸 c.碳酸钙 d.Na2SiO3溶液 e.SiO2。

试剂A为________ ;(填字母,下同)试剂B为________ ;试剂C为________ 。
写出该过程中的化学方程式________ 、________ 。该装置存在一个缺陷是________ 。
族 周期 | IA | 0 | |||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
2 | ⑦ | ① | ② | ||||||
3 | ③ | ④ | ⑧ | ⑤ | ⑥ | ||||
4 | ⑨ | ||||||||
(2)元素③和⑤可形成化合物,用电子式表示其形成过程
(3)元素②、③形成离子的半径
(4) 元素③、④形成的最高价氧化物水化物的碱性
(5)元素⑥的单质与元素③⑨组成的化合物的水溶液反应的离子方程式为
(6)某同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成①、⑦、⑧的非金属性强弱比较的实验研究;从以下所给物质中选出实验所需的物质:a.稀HNO3 b.稀盐酸 c.碳酸钙 d.Na2SiO3溶液 e.SiO2。

试剂A为
写出该过程中的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分,请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为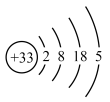 ,砷在周期表中的位置是
,砷在周期表中的位置是___________ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga___________ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途___________ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为___________ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是___________ 。
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
(6)小赵同学在研究元素周期表时发现,碳元素有“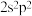 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是___________ 。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为
 ,砷在周期表中的位置是
,砷在周期表中的位置是(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
| A.“类钫”在化合物中显+1价 |
| B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 |
| D.“类钫”单质能与冷水剧烈反应 |
(6)小赵同学在研究元素周期表时发现,碳元素有“
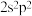 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E是五种短周期主族元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
回答下列问题:
(1)若元素E的某种核素中中子数比质子数多3,表示这种核素组成的符号为___________ 。
(2)把D的单质放到NaOH溶液中,反应的离子方程式为___________ 。
(3)甲的电子式为___________ ,丁的化学式为___________ 。
(4)有200 mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2 mol·L-1,c(Cl-)=1.3 mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1NaOH溶液体积是___________ mL。
(5)在密闭容器中充入BC2、BC和乙的混合气体共w g,若加入足量Na2O2,并不断用电火花点燃至反应完全,测得固体质量增重w g,则BC2与乙的质量比值为___________ 。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子个数比 | A和C 1∶1 | B和A 1∶4 | D和E 1∶3 | B和E 1∶4 |
(1)若元素E的某种核素中中子数比质子数多3,表示这种核素组成的符号为
(2)把D的单质放到NaOH溶液中,反应的离子方程式为
(3)甲的电子式为
(4)有200 mL MgCl2和丙的混合溶液,其中c(Mg2+)=0.2 mol·L-1,c(Cl-)=1.3 mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1NaOH溶液体积是
(5)在密闭容器中充入BC2、BC和乙的混合气体共w g,若加入足量Na2O2,并不断用电火花点燃至反应完全,测得固体质量增重w g,则BC2与乙的质量比值为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C为同一短周期的三种元素,它们的原子序数依次增大且和为40;A是该周期中(除稀有气体元素外)原子半径最大的元素,B元素的原子核外M层上的电子数比K层上的电子数多1。回答下列问题:
(1)A原子的结构示意图为__________ ;A元素在周期表中位置为______________ 。
(2)写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式______________ 。
(3)A和C形成的化合物的电子式为__________ ,该化合物的水溶液呈_________ 性(填“酸”或“碱”)。
(1)A原子的结构示意图为
(2)写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式
(3)A和C形成的化合物的电子式为
您最近一年使用:0次



