Q、W、X、Y、Z为短周期元素,Q是原子半径最小的元素,W是地壳中含量最高的元素,X原子的质子数等于Z与Y的质子数之和:Z与Y位于同一周期,Y原子核外最外层电子比次外层多3个电子,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y、Z的元素名称分别为_______ 、________ 。
(2)X在周期表中的位置是_______ ,其离子结构示意图为_______ 。
(3)W元素有多种核素,请写出中子数为10的W元素的一种核素符号________ 。
(4)X、Y、Z三种元素原子半径由大到小的顺序为_________ (填元素符号);
(5)Y和W两种元素形成的最简单的氢化物中,更稳定的是_______ (用电子式表示)
(1)Y、Z的元素名称分别为
(2)X在周期表中的位置是
(3)W元素有多种核素,请写出中子数为10的W元素的一种核素符号
(4)X、Y、Z三种元素原子半径由大到小的顺序为
(5)Y和W两种元素形成的最简单的氢化物中,更稳定的是
21-22高一上·黑龙江哈尔滨·期末 查看更多[2]
哈尔滨市第六中学校2021-2022学年高一上学期期末考试化学试题 (已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)
更新时间:2022-01-05 21:01:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)10种元素中,化学性质最不活泼的是__________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是__________ 。
(3)10种元素中最高价氧化物的水化物,酸性最强的是__________ 。
(4)元素⑦组成的含非极性键的分子的电子式:__________ 。
(5)区分①、②的碳酸正盐的简单实验方法__________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的离子方程式为__________ 。
(7)③的单质与⑥的最高价氧化物反应的方程式:__________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)10种元素中最高价氧化物的水化物,酸性最强的是
(4)元素⑦组成的含非极性键的分子的电子式:
(5)区分①、②的碳酸正盐的简单实验方法
(6)①和⑤最高价氧化物对应的水化物相互反应的离子方程式为
(7)③的单质与⑥的最高价氧化物反应的方程式:
您最近一年使用:0次
【推荐2】A、B、C、D、E、F、G是元素周期表前四周期常见的元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)A在元素周期表中的位置为___________ ,画出基态B原子的轨道表示式___________ 。
(2)F元素基态原子的最高能级具有的原子轨道数为___________ ,该原子轨道呈___________ 形。
(3)已知元素A、B形成的 链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为___________ 。
(4)C元素可形成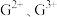 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(5)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ (填“离子”或“共价”)化合物。推测M的最高价氧化物对应的水化物___________ (填“能”或“不能”)与D的最高价氧化物对应水化物发生反应。
| A | 原子核外有6个电子 |
| B | 原子序数比A大1 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子价层电子排布式为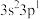 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属,其高价氯化物的盐溶液常用于刻蚀铜制印刷电路板 |
(2)F元素基态原子的最高能级具有的原子轨道数为
(3)已知元素A、B形成的
 链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为(4)C元素可形成
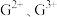 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(5)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)金属性最强的元素是_______ (填元素符号)
(2)④、⑤、⑧对应简单离子的半径最大的是_______ (填微粒符号)。
(3)元素⑧的气态氢化物比元素⑨的气态氢化物的稳定性_______ (填“强”或“弱”)。
(4)用电子式表示由⑤和⑨两种元素组成的化合物的形成过程_______ 。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑦的最高价氧化物对应的水化物能发生化学反应,其离子方程式为_______ 。
(6)由14个①的原子和6个②的原子构成的分子有_______ 种同分异构体。
(7)与元素③同主族且处于第5周期的元素原子序数为_______ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)金属性最强的元素是
(2)④、⑤、⑧对应简单离子的半径最大的是
(3)元素⑧的气态氢化物比元素⑨的气态氢化物的稳定性
(4)用电子式表示由⑤和⑨两种元素组成的化合物的形成过程
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑦的最高价氧化物对应的水化物能发生化学反应,其离子方程式为
(6)由14个①的原子和6个②的原子构成的分子有
(7)与元素③同主族且处于第5周期的元素原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
请回答:
(1)这九种元素分别是①_______ (填元素符号,下同)、②_______ 、③_______ 、④_______ 、⑤_______ 、⑥_______ 、⑦_______ 、⑧_______ 、⑨_______ ,其中化学性质最不活泼的是_______ 。
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是_______ (填化学式)。
(3)①、②、③三种元素按原子半径由大到小的顺序依次为_______ (填元素符号)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(1)这九种元素分别是①
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是
(3)①、②、③三种元素按原子半径由大到小的顺序依次为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下列中所列的是五种短期周期元素原子的半径及主要化合价:
(1)C元素在周期表中的位置___ ;E原子的电子填充在___ 个轨道上,这些电子有___ 种不同的能量。
(2)B、D、E所代表元素的离子半径从大到小的顺序为___ (填离子符号)
(3)C与E形成的化合物属于__ 晶体。
(4)已知X是与E同族的另一短周期元素,有人认为:H-E键的键能大于H-X键的键能,所以H2E的沸点高于H2X的沸点。你是否赞同这种观点___ (“赞同”或“不赞同”),理由:___ 。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.111 | 0.064 | 0.117 | 0.160 | 0.066 |
| 主要化合物 | +2 | -1 | +4,-4 | +2 | -2 |
(2)B、D、E所代表元素的离子半径从大到小的顺序为
(3)C与E形成的化合物属于
(4)已知X是与E同族的另一短周期元素,有人认为:H-E键的键能大于H-X键的键能,所以H2E的沸点高于H2X的沸点。你是否赞同这种观点
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】根据下表中几种短周期元素的原子半径及主要化合价,回答下列问题:
(1)元素D组成的常见单质有两种,分别是_______ 、_______ 。(填名称)
(2)E、I两种元素组成的化合物的化学式为_______ ,用电子式表示其形成过程:_______ 。
(3)A、H、J的离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)78 g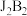 与足量的水反应生成
与足量的水反应生成_______ L(标准状况下)气体。
(5)元素E的单质与水反应的离子方程式为_______ 。
| 元素代号 | A | B | D | E |
| 化合价 | -1 | -2 | +4、-4 | -1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 |
| 元素代号 | G | H | I | J |
| 化合价 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.110 | 0.143 | 0.160 | 0.186 |
(2)E、I两种元素组成的化合物的化学式为
(3)A、H、J的离子半径由大到小的顺序是
(4)78 g
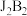 与足量的水反应生成
与足量的水反应生成(5)元素E的单质与水反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水,并将核废水主要辐射物质“氚 ”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。
”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。

(1)下列有关氚的说法正确的是_______。
| A.卡通形象中标“+”号的小球表示中子 | B.氚的核素符号为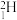 |
| C.氚和及其同位素性质完全相同 | D.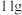 氚水 氚水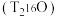 所含中子数为 所含中子数为 |
(2)有关
 和
和 的说法正确的是___________。
的说法正确的是___________。| A.互为同位素 | B.互为同素异形体 |
| C.电子数不同 | D.同温同压下密度之比为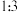 |
(3)在离子
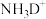 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为(4)
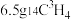 在标况下的体积约为
在标况下的体积约为(5)一个
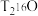 分子的质量是
分子的质量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、T、Z的原子序数依次增大,其族序数之和为15已知几种元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)元素X的一种同位素可用来测定文物所属年代,这种同位素的原子符号是___________ 。
(2)Y形成的一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是___________ ,书写Y的简单氢化物的电子式___________ 。
(3)画出T的原子结构示意图:___________ 。
(4)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的化学方程式为___________ 。
(5)Z元素在元素周期表中的位置是:___________ ,其组成的单质可以与Fe反应,该实验现象是:___________ ,5.6gFe参与该反应时,转移电子数是___________ 。
| 元素编号 | 元素性质或原子结构的相关叙述 |
| T | 失去一个电子后形成与Ne相同的核外电子排布 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其某种单质是空气的主要成分,具有氧化性 |
| Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(2)Y形成的一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)画出T的原子结构示意图:
(4)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的化学方程式为
(5)Z元素在元素周期表中的位置是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的短周期部分,①~⑦代表七种短周期元素。
已知:⑤的焰色试验火焰呈黄色。
请填写下列空白:
(1)②在元素周期表中的位置为___________ ;①的原子结构示意图为___________ 。
(2)③的一种核素的中子数为10,其原子符号为___________ (用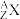 形式表示)。
形式表示)。
(3)④和⑦中非金属性较弱的是___________ (填元素符号)。
(4)①和⑤中原子半径较大的是___________ (填元素符号),与⑤同族的下一周期元素和③的最简单氢化物反应的离子方程式为___________ 。
(5)将⑥的氧化物加入⑤的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为___________ 。
| ① | ② | ③ | ④ | |||
| ⑤ | ⑥ | ⑦ |
请填写下列空白:
(1)②在元素周期表中的位置为
(2)③的一种核素的中子数为10,其原子符号为
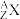 形式表示)。
形式表示)。(3)④和⑦中非金属性较弱的是
(4)①和⑤中原子半径较大的是
(5)将⑥的氧化物加入⑤的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为
您最近一年使用:0次



