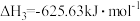已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) ΔΗ= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔΗ= -241.8kJ/mol
据此判断下列说法正确的是
①CO(g)+1/2O2(g)=CO2(g) ΔΗ= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔΗ= -241.8kJ/mol
据此判断下列说法正确的是
| A.H2(g)+1/2O2(g)=H2O(l) ΔΗ>-241.8kJ/mol |
| B.H2(g)的燃烧热ΔΗ =-241.8 kJ/mol |
| C.H2(g)转变成H2O(g)的化学反应一定放出能量 |
| D.CO(g)+ H2O(g)= CO2(g)+ H2(g)的ΔΗ =-41.2kJ/mol |
更新时间:2021-12-13 19:45:14
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知SO2和O2反应生成4mol SO3时放出的热量为Q kJ,那么2mol SO2和1mol O2在一有催化剂的密闭容器中发生反应时,放出的热量为
| A.大于Q kJ | B.等于Q kJ | C.小于0.5Q kJ | D.无法确定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知H-H键、Cl-Cl键和H-Cl键的键能分别为436kJ·mol-1、243kJ·mol-1和431kJ·mol-1,则由Cl2(g)和H2(g)反应生成1molHCl(g)时的能量变化是:
| A.放热183kJ | B.放热91.5kJ | C.吸热183kJ | D.吸热91.5kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列热化学方程式中ΔH能表示可燃物燃烧热的是 ( )
| A.H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802.3kJ·mol-1 |
| C.2H2(g)+O2(g)=2H₂O(g) ΔH=-571.6kJ·mol-1 |
D.CO(g)+ O2(g)=CO2(g) ΔH=-258 kJ-mol-1 O2(g)=CO2(g) ΔH=-258 kJ-mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】1 mol H2在O2中完全燃烧生成液态水放出285.8kJ的热量,下列热化学方程式正确的是
A.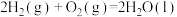 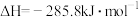 |
B.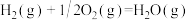 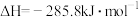 |
C.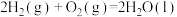 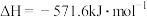 |
D. 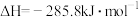 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知稳定性:反—2—丁烯>顺—2—丁烯>1—丁烯。下列说法正确的是
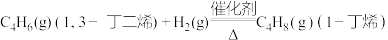

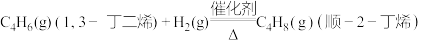



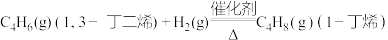

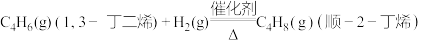



| A.相同条件下,1mol的1,3—丁二烯和1mol氢气总能量比1mol的1—丁烯能量低 |
B.其他条件不变,选择合适的催化剂可以降低活化能和焓变,其中 变化最大 变化最大 |
| C.相同条件下,1mol的1,3—丁二烯和1mol氢气反应达到平衡时产物中反—2—丁烯最少 |
| D.顺—2—丁烯转化为反—2—丁烯是放热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】可逆反应 ,某温度下的平衡常数为
,某温度下的平衡常数为 (
(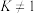 ),反应热为
),反应热为 。保持温度不变,将方程式的书写作如下改变,则
。保持温度不变,将方程式的书写作如下改变,则 和K的相应变化为
和K的相应变化为
 ,某温度下的平衡常数为
,某温度下的平衡常数为 (
(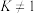 ),反应热为
),反应热为 。保持温度不变,将方程式的书写作如下改变,则
。保持温度不变,将方程式的书写作如下改变,则 和K的相应变化为
和K的相应变化为A.写成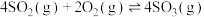 , , 、K均扩大了一倍 、K均扩大了一倍 |
B.写成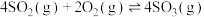 , , 扩大了一倍,K保持不变 扩大了一倍,K保持不变 |
C.写成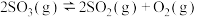 , , 、K变为原来的相反数 、K变为原来的相反数 |
D.写成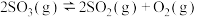 , , 变为原来的相反数,K变为原来的倒数 变为原来的相反数,K变为原来的倒数 |
您最近一年使用:0次

 的相对能量为0],下列说法错误的是
的相对能量为0],下列说法错误的是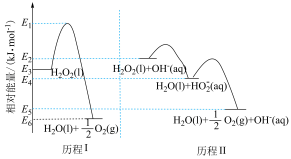

 (aq)
(aq) (E4-E2)
(E4-E2)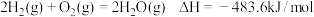 ,则氢气的燃烧热为
,则氢气的燃烧热为
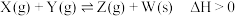 ,在恒温恒压的条件下,达到平衡后加入X,上述反应的
,在恒温恒压的条件下,达到平衡后加入X,上述反应的 增大;
增大; (条件高温)可用于纯硅的制备,用E表示键能,该反应
(条件高温)可用于纯硅的制备,用E表示键能,该反应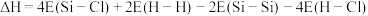
 时,放出的热量相等;
时,放出的热量相等; (s,石英砂)
(s,石英砂)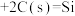 (s,粗硅)
(s,粗硅)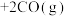
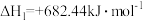
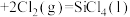
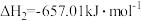
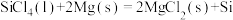 (s,纯硅)
(s,纯硅)