下列说法不正确的是
| A.在多电子原子中,电子的能量是不相同的,离核较近的区域内运动的电子能量较低 |
| B.已知第117号元素的原子最外层电子数是7,则该元素位于第七周期第ⅦA族 |
| C.在周期表中金属与非金属的分界处可以找到半导体材料 |
| D.碱金属元素的化学性质相似,都能在加热条件下与氧气反应生成过氧化物 |
更新时间:2022-01-15 17:51:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z是短周期的三种主族元素,在周期表中的位置如图,下列说法正确的是


| A.原子半径:X<Y<Z |
| B.X的气态氢化物热稳定性强于Z的气态氢化物 |
| C.若Z的最高正价为+m,则X的最高正价也一定为+m |
| D.Y和Z的最高价氧化物对应水化物可能均为强碱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.元素周期表里,主族元素所在的族序数等于原子核外电子数 |
| B.F是最活泼非金属,Li是最活泼金属. |
| C.X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
| D.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是
| A.SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强 |
| B.根据卤族元素的性质,推出铁与足量碘蒸气反应后铁元素显+3价 |
| C.由F、Cl、Br非金属性依次减弱,推出HF、HCl、HBr的还原性依次增强 |
| D.结构和组成相似的物质,沸点随相对分子质量的增大而升高,因此NH3沸点低于PH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】类推的思维方法在化学学习与研究中可能会产生错误的结论,因此类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论正确的是
| A.金刚石中C—C键的键长为154.45pm,C60中C—C键的键长为140~145pm,所以C60的熔点高于金刚石 |
| B.CO2晶体是分子晶体,SiO2晶体也是分子晶体 |
C.从CH4、NH 、SO 、SO 为正面体结构,可推测CC14、PH 为正面体结构,可推测CC14、PH 、PO 、PO 也为正四面体结构 也为正四面体结构 |
| D.C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】硒化物[如 CdSe (硒化镉)]可用于太阳能电池、光传感器,热电发电与制冷等。下列说法不正确的是
| A.S、Se 均位于元素周期表第ⅥA 族,它们的氢化物稳定性依次减弱 |
| B.Cd 为元素周期表中 48 号元素,则其位于元素周期表中第五周期第 IIB 族 |
| C.SeO2与 SO2在水中可以生成硫酸,说明 SeO2氧化性强于 SO2 |
| D.CdSe 在充足氧气中燃烧可以得到 SeO2和金属 Cd |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素 X、Y、Z、R、T原子序数依次增大。X原子的最外层电子数是其电子层数的2倍,Z元素原子在同周期原子中半径最小,Y与R能形成 R2Y、R2Y2型常见离子化合物,R与T形成的化合物 R2T 能促进水的电离。下列说法错误的是
| A.最高价氧化物对应水化物的酸性 X<T |
| B.Z的单质能与Y的简单氢化物反应 |
| C.原子半径和简单离子半径均满足R>T>Y |
| D.由X、Y、R三种元素组成的常见化合物的水溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】a、b、c、d是四种短周期元素,a、b、d同周期;c、d同主族a的原子结构示意图为 ,b与c形成的化合物的化学式为
,b与c形成的化合物的化学式为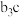 ,且b、c离子有相同的电子层结构。下列比较中,正确的是
,且b、c离子有相同的电子层结构。下列比较中,正确的是
| A.原子序数:a>b>c | B.氢化物稳定性:a>c>d |
| C.原子半径:c>a>d | D.最高价氧化物水化物的酸性:c>a>d |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】a、b、c、d、e五种短周期元素的原子半径和最外层电子数之间的关系如图所示。下列说法正确的是


| A.离子半径:b>d |
| B.最低价氢化物的沸点:d>e |
| C.最高价氧化物的水化物的酸性:c>e |
| D.a与b、c、d、e均可形成共价化合物 |
您最近一年使用:0次



