元素周期律的发现是近代化学史上的一座里程碑。下列事实不能 用元素周期律解释的是
| A.气态氢化物的稳定性:H2O>H2S |
| B.常温下,形状和大小相同的Mg、Al与同浓度盐酸反应,Mg条更剧烈 |
| C.Br2从NaI溶液中置换出I2 |
| D.酸性:H2SO4>H2SO3 |
更新时间:2021-12-21 11:34:13
|
【知识点】 元素周期律的应用
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】Q、X、Y、Z、W为原子序数依次增大的五种前20号元素。其中化合物Y2Q4的电子总数为18个,Z元素的最外层电子数比次外层电子数少2,由四种元素组成的化合物结构为W+[Z—X≡Y]-,下列说法错误的是
| A.Z元素的单质存在于火山喷口附近或地壳的岩层里 |
| B.简单离子半径:Z>W>Y |
| C.简单气态氢化物的热稳定性:Y>Z |
| D.图示化合物遇含Fe3+的溶液可生成血红色沉淀 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素,可以构成某复合型高分子聚合物 ,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
 ,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是
,M分子结构庞大,吸附能力强。X形成的单质是相同条件下密度最小的气体,Y与W同主族,Y的L层电子数为K层电子数的三倍,Z是地壳中含量最多的金属元素。下列说法正确的是A.简单离子半径大小关系: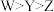 |
| B.M在水中能形成胶体,具有净水、杀菌、消毒的功能 |
| C.Z的最高价氧化物对应的水化物为强碱 |
D.M化学式中存在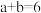 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时0.01mol·L-1X和W形成化合物的水溶液pH为2。下列说法正确的是
| A.由于非金属性Y>R,则X、Y组成化合物的沸点高于X、R组成的化合物 |
| B.在Z、Y形成的两种离子化合物中阴阳离子的个数比分别为1:2和1:1 |
| C.原子半径由大到小排列的是:Z>R>W>Y>X |
| D.Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
您最近半年使用:0次



