某生产企业的工业废水中含有大量的FeSO4和较多的CuSO4。为了变废为宝,技术人员计划从该废水中回收FeSO4和金属Cu,工艺流程如图所示。回答下列问题:
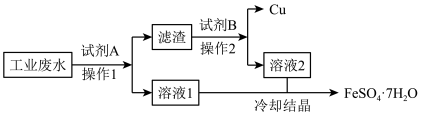
(1)“操作1”与“操作2”的名称为_______ ,在实验室中进行该操作时,所需要的玻璃仪器除烧杯外,还有_______ 。
(2)加入试剂A的目的是将 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为______ 。
(3)“滤渣”的成分为________ ,加入的试剂B为________ (填化学式)。
(4)要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是___________ 。

(1)“操作1”与“操作2”的名称为
(2)加入试剂A的目的是将
 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为(3)“滤渣”的成分为
(4)要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是
更新时间:2022-01-20 20:03:11
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】粗盐精制,除去粗盐中的 Ca2+、Mg2+、 杂质时,粗盐溶解后加入沉淀剂: a.过量的 Na2CO3溶液 b. 过量的 BaCl2 溶液 c. 过量的 NaOH 溶液,过滤除去沉淀, 再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂: a.过量的 Na2CO3溶液 b. 过量的 BaCl2 溶液 c. 过量的 NaOH 溶液,过滤除去沉淀, 再加入适量的盐酸。
(1)加入沉淀剂的顺序正确的是_______ (填序号)。
A.abc B.bac C.cba
(2)分别写出加入氯化钡及氢氧化钠时发生反应的离子方程式_________ 。
(3)加入碳酸钠的目的_______ ,加入稀盐酸的目的_____ 。并写出加稀盐酸时反应的离子方程式________ 。除去稀盐酸的方法_______ 。
 杂质时,粗盐溶解后加入沉淀剂: a.过量的 Na2CO3溶液 b. 过量的 BaCl2 溶液 c. 过量的 NaOH 溶液,过滤除去沉淀, 再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂: a.过量的 Na2CO3溶液 b. 过量的 BaCl2 溶液 c. 过量的 NaOH 溶液,过滤除去沉淀, 再加入适量的盐酸。(1)加入沉淀剂的顺序正确的是
A.abc B.bac C.cba
(2)分别写出加入氯化钡及氢氧化钠时发生反应的离子方程式
(3)加入碳酸钠的目的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。

(1)沉淀A的主要成分是_________ (填化学式)。
(2)②中反应的离子方程式是_________ 。
(3)③加入过量的Na2CO3溶液的目的是________ 。
(4)溶液3中肯定含有的杂质是_______ ,为除去杂质可向溶液3中加入过量的_______ 。

(1)沉淀A的主要成分是
(2)②中反应的离子方程式是
(3)③加入过量的Na2CO3溶液的目的是
(4)溶液3中肯定含有的杂质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】粗盐含有泥沙以及Ca2+、Mg2+、SO42﹣等杂质,其提纯过程一般经过以下流程:

某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(1)操作①粗盐样品加水之前,需要将大颗粒粗盐变为细小颗粒或粉末,此时在实验室中需要用到的仪器为__________ 。
(2)操作②、④过滤后的滤液仍有浑浊,需要进行的操作是___________________ 。
(3)操作③按abc顺序依次加入过量的试剂。若a为NaOH溶液,则c为________ 。加入c发生反应的离子方程式为_________________________________________________ 。
(4)加盐酸调溶液pH的目的是________________________________ 。
(5)步骤⑥操作名称是______________ 。

某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(1)操作①粗盐样品加水之前,需要将大颗粒粗盐变为细小颗粒或粉末,此时在实验室中需要用到的仪器为
(2)操作②、④过滤后的滤液仍有浑浊,需要进行的操作是
(3)操作③按abc顺序依次加入过量的试剂。若a为NaOH溶液,则c为
(4)加盐酸调溶液pH的目的是
(5)步骤⑥操作名称是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。

试回答下列问题:
⑴ A的化学式是____________ ;
⑵ 反应F→D的化学方程式是______________________________________ 。
⑶ 检验F中金属阳离子的常用方法是___________________________________ 。
⑷ 物质B与盐酸反应的离子方程式是_________________________________ 。

试回答下列问题:
⑴ A的化学式是
⑵ 反应F→D的化学方程式是
⑶ 检验F中金属阳离子的常用方法是
⑷ 物质B与盐酸反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水回收硫酸亚铁和金属铜。请根据流程图(所加试剂均过量),回答下列问题:
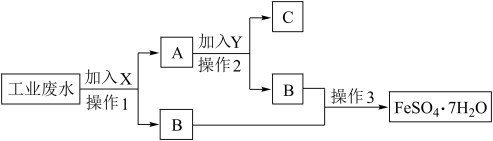
(1)物质X的化学式为:___ ,操作2的名称:___ 。
(2)已知Y为稀硫酸,写出C中成分的化学式:___ ,在A中加入Y的化学方程式为:___ 。
(3)工业废水中加入X所发生的离子方程式为:___ ;该反应是否为氧化还原反应___ (填“是”或“否”),如果是氧化还原反应,发生还原反应的离子是:___ 。
(4)流程中的操作3是:蒸发浓缩、___ 、过滤、洗涤、烘干。

(1)物质X的化学式为:
(2)已知Y为稀硫酸,写出C中成分的化学式:
(3)工业废水中加入X所发生的离子方程式为:
(4)流程中的操作3是:蒸发浓缩、
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~I是目前我们已学的常见物质,它们的相互转化关系如图所示(有反应条件、反应物和生成物未给出).已知A、D是组成元素相同的无色气体;G、F组成元素也相同,在常温下都是液体,E是最理想能源物质;C是世界上产量最高的金属。

 写出
写出 、
、 的化学式:
的化学式:
________ 、
________ .
 反应①的化学方程式可能为
反应①的化学方程式可能为________ ,此反应在生产中的应用是________ .
 若
若 由两种元素组成,反应⑤的化学方程式为
由两种元素组成,反应⑤的化学方程式为________ .
 反应②的化学反应基本类型是
反应②的化学反应基本类型是________ .
 物质的一种用途是
物质的一种用途是________ .

 写出
写出 、
、 的化学式:
的化学式:

 反应①的化学方程式可能为
反应①的化学方程式可能为 若
若 由两种元素组成,反应⑤的化学方程式为
由两种元素组成,反应⑤的化学方程式为 反应②的化学反应基本类型是
反应②的化学反应基本类型是 物质的一种用途是
物质的一种用途是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1)写出该反应的化学方程式________________________________________________ 。
(2)印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。

Ⅰ.步骤②需加入的试剂A是_____________________ (填化学式);
Ⅱ.步骤③通入的气体B是_____________ (填化学式),写出该反应的离子方程式:___________________
(1)写出该反应的化学方程式
(2)印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。

Ⅰ.步骤②需加入的试剂A是
Ⅱ.步骤③通入的气体B是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】I.现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而得到较为纯净的NaNO3。实验流程可用如图表示:
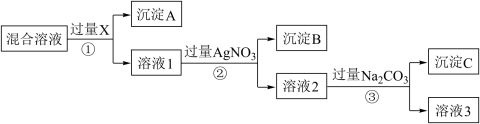
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:_______________ ,沉淀B:_______________ 。
(2)实验流程中加入过量的Na2CO3的目的是______________________________________ 。
(3)实验方案得到的溶液3中肯定含有__________ (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的______________ 。
Ⅱ.某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
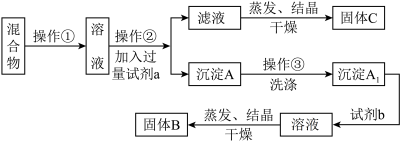
供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(4)操作②的名称是_______________ 。
(5)试剂a是_______ (填化学式,下同),试剂b是_________ 。
(6)加入试剂a所发生反应的化学方程式为________________________________ 。加入试剂b所发生反应的化学方程式为__________________________________ 。
(7)简述操作③的具体方法:______________________________________________________ 。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:
(2)实验流程中加入过量的Na2CO3的目的是
(3)实验方案得到的溶液3中肯定含有
Ⅱ.某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(4)操作②的名称是
(5)试剂a是
(6)加入试剂a所发生反应的化学方程式为
(7)简述操作③的具体方法:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】实验室以废铁屑(含有少量碳、Fe2O3杂质,表面附着少量油污)为原料制备无水FeCl3(s)。设计的流程如下:
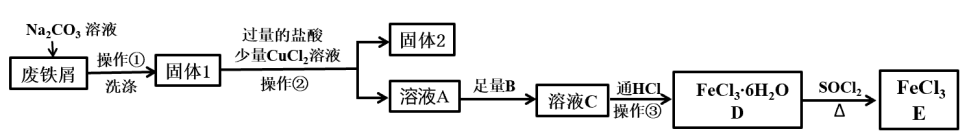
已知:SOCl2熔点-101℃,沸点76℃,易水解。
(1)Na2CO3溶液的作用为___________ ;操作①为___________ 。
(2)“操作②”前加入少量CuCl2溶液的目的为___________ 。
(3)“固体2”的成分为___________ 。
(4)为避免引入新的杂质,试剂B可以选用___________ (填字母)
a.KMnO4溶液 b.通氯气 c.H2O2溶液 d.稀硝酸
(5)操作③是蒸发结晶,加热的同时通入HCl(g)目的是___________ (用平衡移动原理解释)。
(6)D转化为E的化学方程式为___________ 。

已知:SOCl2熔点-101℃,沸点76℃,易水解。
(1)Na2CO3溶液的作用为
(2)“操作②”前加入少量CuCl2溶液的目的为
(3)“固体2”的成分为
(4)为避免引入新的杂质,试剂B可以选用
a.KMnO4溶液 b.通氯气 c.H2O2溶液 d.稀硝酸
(5)操作③是蒸发结晶,加热的同时通入HCl(g)目的是
(6)D转化为E的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】磷酸亚铁锂(LiFePO4)是新型锂离子电池的电极材料,其制备流程如下:

不同温度下碳酸锂的溶解度如下表所示:
(1)已知,锂与镁在元素周期表中位于对角线位置,写出碳酸锂高温煅烧分解的化学方程式___________ 。
(2)①操作1需要使用过滤装置,下图是过滤操作示意图,其操作不规范的是___________ (填标号)。
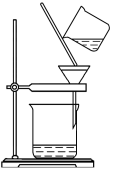
a.漏斗末端颈尖未紧靠烧杯内壁
b.过滤时利用玻璃棒引流
c.将滤纸湿润,使其紧贴漏斗壁
d.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
②煅烧时,需要使用下列仪器中的___________ (填仪器名称)。
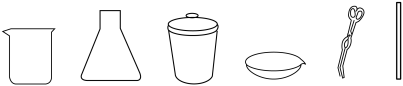
(3)研磨的目的是___________ (任答一点)。
(4)“沉锂”需要在95℃以上进行,主要原因是___________ 。过滤碳酸锂所得母液中主要含有硫酸钠,可能还含有___________ 和___________ 。
(5)制备磷酸亚铁锂的过程必须在惰性气体氛围中进行,原因是___________ 。
(6)在“煅烧”操作中,除了生成磷酸亚铁锂和乙酸外,还有其他气体产物逸出,写出该反应的化学方程式___________ 。

不同温度下碳酸锂的溶解度如下表所示:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/ (g·L-1) | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(2)①操作1需要使用过滤装置,下图是过滤操作示意图,其操作不规范的是

a.漏斗末端颈尖未紧靠烧杯内壁
b.过滤时利用玻璃棒引流
c.将滤纸湿润,使其紧贴漏斗壁
d.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
②煅烧时,需要使用下列仪器中的

(3)研磨的目的是
(4)“沉锂”需要在95℃以上进行,主要原因是
(5)制备磷酸亚铁锂的过程必须在惰性气体氛围中进行,原因是
(6)在“煅烧”操作中,除了生成磷酸亚铁锂和乙酸外,还有其他气体产物逸出,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某学习小组模拟“侯氏制碱法”开展如下项目化学习:
项目一、粗盐(含Ca2+、Mg2+、 等杂质)提纯氯化钠
等杂质)提纯氯化钠
粗盐提纯的流程如下:

(1)试剂X为___________ 。
(2)“操作1”所需玻璃仪器为烧杯、___________ 。
(3)“沉淀”的成分为CaCO3、Mg(OH)2、___________ 。
(4)“滤液”中加入稀盐酸生成气泡的离子方程式为___________ 。
项目二、模拟“侯氏制碱法”制备纯碱

(5)气体A为___________ 。
(6)“悬浊液”过滤所得滤液中含有的主要离子有___________ 。
(7)写出晶体转化为纯碱的化学方程式___________ 。
项目一、粗盐(含Ca2+、Mg2+、
 等杂质)提纯氯化钠
等杂质)提纯氯化钠粗盐提纯的流程如下:

(1)试剂X为
(2)“操作1”所需玻璃仪器为烧杯、
(3)“沉淀”的成分为CaCO3、Mg(OH)2、
(4)“滤液”中加入稀盐酸生成气泡的离子方程式为
项目二、模拟“侯氏制碱法”制备纯碱

(5)气体A为
(6)“悬浊液”过滤所得滤液中含有的主要离子有
(7)写出晶体转化为纯碱的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】四水合磷酸锌 [Zn3(PO4)2·4H2O,摩尔质量为457 g·mol-1,难溶于水] 是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备Zn3(PO4)2·4H2O的流程如图,回答下列问题:
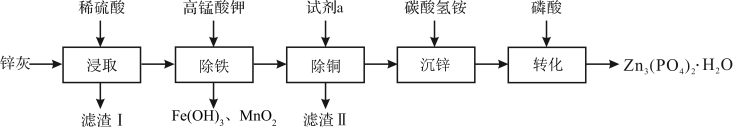
已知:①6NH4HCO3 + 3ZnSO4 ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
②ZnCO3·2Zn(OH)2·H2O + 2H3PO4 Zn3(PO4)2·4H2O + 2H2O + CO2↑
Zn3(PO4)2·4H2O + 2H2O + CO2↑
③常温下,Fe3+、Fe2+、Cu2+、Zn2+生成氢氧化物沉淀时的pH:
(1)滤渣Ⅰ的主要成分为_______ ;试剂a为_______ ;
(2)“除铁”操作时,需先将溶液调至接近中性,然后再滴加KMnO4溶液,使溶液中的铁元素转化为Fe(OH)3,该反应的离子方程式为_______ ;
(3)“转化”结束后,从混合液中分离得到Zn3(PO4)2·4H2O的操作包括_______ 和干燥。
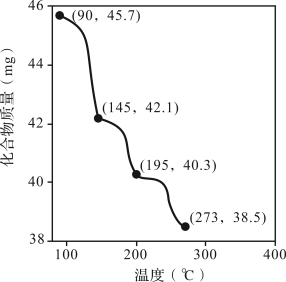
(4)称取45.7 mg Zn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为_______。
(5)为测定产品中Zn3(PO4)2·4H2O的含量,进行如下实验:(已知:Zn2+与H2Y2−按1:1反应;杂质不反应。)
步骤Ⅰ:准确称取0.4570g产品于烧杯中,加入适量盐酸使其溶解,将溶液转移至100 mL容量瓶,定容。
步骤Ⅱ:移取20.00 mL上述溶液于锥形瓶中,加入指示剂,在pH = 5~6的缓冲溶液中用0.02000mol·L-1 Na2H2Y标准溶液滴定至终点,测得Na2H2Y标准溶液的用量为27.60 mL。
步骤Ⅱ中移取溶液时所使用的玻璃仪器为_______ ;产品中Zn3(PO4)2·4H2O的质量分数为_______ 。下列操作中,导致产品中Zn3(PO4)2·4H2O含量测定值偏低的是_______ 。
a.步骤I中定容时俯视刻度线
b.步骤I中转移溶液时未洗涤烧杯
c.步骤II中滴定管未用Na2H2Y标准溶液润洗
d.步骤II中滴定前滴定管内无气泡,滴定结束后有气泡

已知:①6NH4HCO3 + 3ZnSO4
 ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑②ZnCO3·2Zn(OH)2·H2O + 2H3PO4
 Zn3(PO4)2·4H2O + 2H2O + CO2↑
Zn3(PO4)2·4H2O + 2H2O + CO2↑③常温下,Fe3+、Fe2+、Cu2+、Zn2+生成氢氧化物沉淀时的pH:
| Fe3+ | Fe2+ | Cu2+ | Zn2+ | |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 | 5.7 |
| 完全沉淀时的pH | 3.7 | 9.0 | 6.7 | 8.1 |
(2)“除铁”操作时,需先将溶液调至接近中性,然后再滴加KMnO4溶液,使溶液中的铁元素转化为Fe(OH)3,该反应的离子方程式为
(3)“转化”结束后,从混合液中分离得到Zn3(PO4)2·4H2O的操作包括
(4)称取45.7 mg Zn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为_______。

| A.90~145℃ | B.145~195℃ | C.195~273℃ | D.>273℃ |
步骤Ⅰ:准确称取0.4570g产品于烧杯中,加入适量盐酸使其溶解,将溶液转移至100 mL容量瓶,定容。
步骤Ⅱ:移取20.00 mL上述溶液于锥形瓶中,加入指示剂,在pH = 5~6的缓冲溶液中用0.02000mol·L-1 Na2H2Y标准溶液滴定至终点,测得Na2H2Y标准溶液的用量为27.60 mL。
步骤Ⅱ中移取溶液时所使用的玻璃仪器为
a.步骤I中定容时俯视刻度线
b.步骤I中转移溶液时未洗涤烧杯
c.步骤II中滴定管未用Na2H2Y标准溶液润洗
d.步骤II中滴定前滴定管内无气泡,滴定结束后有气泡
您最近一年使用:0次



