已知氢碘酸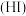 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:
(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_________ (填标号).
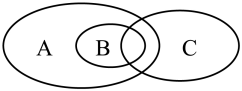
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为_________________ .
(3)常温下 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
______  (填“>”、“<”或“=).
(填“>”、“<”或“=).
(4)在反应 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为________ .
(5)下列三种氧化剂均可以将 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:
请判断等物质的量的三种氧化剂分别与足量HI作用,得到I2质量最多的是________ (填选项标号).
(6)向 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
①红褐色沉淀溶解,反应的离子方程式为___________________________ .
②最后溶液颜色加深,反应的离子方程式为______________________________ .
 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)常温下
 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
 (填“>”、“<”或“=).
(填“>”、“<”或“=).(4)在反应
 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为(5)下列三种氧化剂均可以将
 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:选项 | A | B | C |
氧化剂 |
|
|
|
还原产物 |
|
|
|
(6)向
 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.①红褐色沉淀溶解,反应的离子方程式为
②最后溶液颜色加深,反应的离子方程式为
更新时间:2022/01/18 16:14:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】从下列选项中选择正确的答案,将其字母填到横线上。
a.丁达尔现象 b.聚沉 c.电泳 d.渗析
(1)一束可见光照射鸡蛋清蛋白溶液,可从入射光侧面看到光亮的“通路”,这种现象称为____ 。
(2)做实验时,手指不慎被玻璃划破,可从急救箱中取出氯化铁溶液应急止血,其原理是_____ 。
(3)肾衰竭等疾病引起的血液中毒,可用血液透析进行治疗的原理是_____ 。
(4)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量的问题。解决方法:把这些陶土和水一起搅拌,使其分散质微粒直径介于1~100nm,然后插入两个电极,接通直流电源,这时与直流电源正极相连的一极聚集陶土,阴极聚集氧化铁,其原理是_____ 。
a.丁达尔现象 b.聚沉 c.电泳 d.渗析
(1)一束可见光照射鸡蛋清蛋白溶液,可从入射光侧面看到光亮的“通路”,这种现象称为
(2)做实验时,手指不慎被玻璃划破,可从急救箱中取出氯化铁溶液应急止血,其原理是
(3)肾衰竭等疾病引起的血液中毒,可用血液透析进行治疗的原理是
(4)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量的问题。解决方法:把这些陶土和水一起搅拌,使其分散质微粒直径介于1~100nm,然后插入两个电极,接通直流电源,这时与直流电源正极相连的一极聚集陶土,阴极聚集氧化铁,其原理是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】胶体是日常生活中的一种混合物。
(1)在水泥和冶金工业常用高压电对气溶胶作用除去大量烟尘,以减少对空气的污染,这种做法应用的原理是___________ 。
(2)某课外活动小组进行 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。
①实验室制备 胶体的方法是:
胶体的方法是:___________ ,当溶液变为红褐色时立即停止加热。
②写出制备 胶体的化学反应方程式:
胶体的化学反应方程式:___________ 。
③取少量制得的胶体加入试管中,再加入少量饱和氯化钠溶液,观察到的现象是___________ ,这种现象称为胶体的___________ 。
(3)有关制备 胶体实验方案评价。某同学在制备
胶体实验方案评价。某同学在制备 胶体时将蒸馏水改为自来水煮沸后进行实验,该同学是否能得到胶体?
胶体时将蒸馏水改为自来水煮沸后进行实验,该同学是否能得到胶体?___________ (填“能”或“不能”),理由是___________ 。
(1)在水泥和冶金工业常用高压电对气溶胶作用除去大量烟尘,以减少对空气的污染,这种做法应用的原理是
(2)某课外活动小组进行
 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。①实验室制备
 胶体的方法是:
胶体的方法是:②写出制备
 胶体的化学反应方程式:
胶体的化学反应方程式:③取少量制得的胶体加入试管中,再加入少量饱和氯化钠溶液,观察到的现象是
(3)有关制备
 胶体实验方案评价。某同学在制备
胶体实验方案评价。某同学在制备 胶体时将蒸馏水改为自来水煮沸后进行实验,该同学是否能得到胶体?
胶体时将蒸馏水改为自来水煮沸后进行实验,该同学是否能得到胶体?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】胶体是一种特殊的分散系,有很多特殊的性质。现有下列试剂供选择来制备各种胶体:①饱和FeCl3溶液;②Na2SiO3溶液;③稀盐酸;④蒸馏水;⑤NaOH溶液。
(1)证明有Fe(OH)3胶体生成的实验操作和现象是
(2)制备硅酸胶体所需的试剂为
(3)将上述两种胶体混合,出现的现象是
(4)向Fe(OH)3胶体中逐滴加入HI溶液,出现的现象是先产生沉淀,后沉淀逐渐溶解,写出沉淀溶解的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学反应方程式为_______ 。
(3)③与⑨发生反应的离子方程式为_______ 。
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是_______ (填化学式)。
(1)按物质的树状分类法填写表格的空白处:
| 分类标准 | 氧化物 | 电解质 | |||
| 属于该类的物质 | ② | ⑧⑨ | ⑦ |
(3)③与⑨发生反应的离子方程式为
(4)②与⑨发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,该反应的还原产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)以下为中学化学中常见的几种物质:①碳棒;②熔融KCl;③NaHSO4固体;④铜;⑤硫酸;⑥澄清石灰水,其中能导电的有________ (填序号。下同),属于电解质的有_________ 。
(2)要求写出方程式:
①碳酸钠和氯化钡溶液反应(离子方程式):______________________ ;
②碳酸氢钙溶液与过量氢氧化钠溶液:______________________ ;
③向NaHSO4溶液中滴加Ba(OH)2溶液至刚好沉淀完全:______________________ ;
(2)要求写出方程式:
①碳酸钠和氯化钡溶液反应(离子方程式):
②碳酸氢钙溶液与过量氢氧化钠溶液:
③向NaHSO4溶液中滴加Ba(OH)2溶液至刚好沉淀完全:
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛.
(1)碳与短周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子.碳元素在周期表中的位置是_____________ ,Q是_____________ ,R的电子式为_____________ .
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为_____________ ,除去粗产品中少量钠的试剂为_____________ .
(3)碳还原SiO2制SiC,其粗产品中杂质为Si和SiO2.现将20.0g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L.生成氢气的离子方程式为_____________ ,硅酸盐的物质的量浓度为_____________ .
(4)下列叙述正确的有_____________ (填序号).
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2.
(1)碳与短周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子.碳元素在周期表中的位置是
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为
(3)碳还原SiO2制SiC,其粗产品中杂质为Si和SiO2.现将20.0g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L.生成氢气的离子方程式为
(4)下列叙述正确的有
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2.
您最近一年使用:0次
【推荐1】已知:Fe2O3+3CO 2Fe+3CO2。
2Fe+3CO2。
(1)标出该反应中电子转移的方向和数目。___________ 。
(2)指出该反应中,氧化剂是___________ ,还原剂是___________ 。
(3)在该反应中,若有2 mol电子发生转移,在标准状况下,可生成CO2的体积为___________ 。
 2Fe+3CO2。
2Fe+3CO2。(1)标出该反应中电子转移的方向和数目。
(2)指出该反应中,氧化剂是
(3)在该反应中,若有2 mol电子发生转移,在标准状况下,可生成CO2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。
(1)用双线桥标出电子转移的方向和数目___ 。
(2)该反应中,氧化剂是___ ,还原剂是____ 。
Ⅱ.铜绿即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
(1)用单线桥标出电子转移的方向和数目____ 。
(2)该反应中的还原剂是____ 、氧化剂是____ 。
Ⅲ.氮化铝具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可以通过如下方式合成:Al2O3+N2+3C=2AlN+3CO
(1)用单线桥标出该反应中电子转移的方向和数目___ 。
(2)该反应中的还原剂是___ 、氧化剂是____ 。
(1)用双线桥标出电子转移的方向和数目
(2)该反应中,氧化剂是
Ⅱ.铜绿即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
(1)用单线桥标出电子转移的方向和数目
(2)该反应中的还原剂是
Ⅲ.氮化铝具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可以通过如下方式合成:Al2O3+N2+3C=2AlN+3CO
(1)用单线桥标出该反应中电子转移的方向和数目
(2)该反应中的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上处理污水中NO 常采用还原法。
常采用还原法。
I.不同密度的HNO3与Fe反应(相同温度)时还原产物成分分布情况如图示。____ 。
(2)已知:硝酸的密度小于1.1g·cm-3时,Fe元素转化生成Fe2+。写出硝酸密度小于1.1g·cm-3时发生的主要反应的离子方程式____ 。
II.工业上利用铝粉(掺少量炭粉)处理酸性污水中的硝酸盐,脱硝率可达94%,其反应过程原理如图所示。____ 。
(4)酸性过强,不利于脱硝的原因是____ 。
 常采用还原法。
常采用还原法。I.不同密度的HNO3与Fe反应(相同温度)时还原产物成分分布情况如图示。
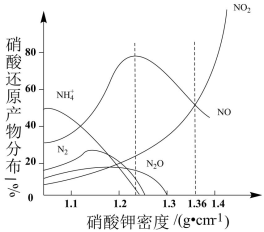
(2)已知:硝酸的密度小于1.1g·cm-3时,Fe元素转化生成Fe2+。写出硝酸密度小于1.1g·cm-3时发生的主要反应的离子方程式
II.工业上利用铝粉(掺少量炭粉)处理酸性污水中的硝酸盐,脱硝率可达94%,其反应过程原理如图所示。
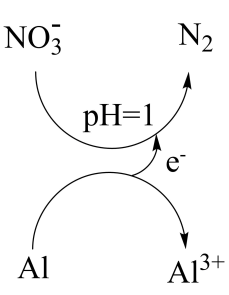
(4)酸性过强,不利于脱硝的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】部分含氯物质的分类与相应化合价关系如图所示。
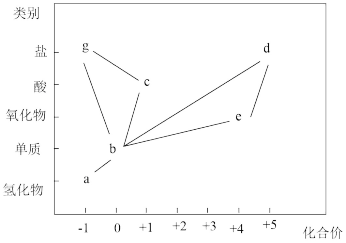
(1) 和浓盐酸在一定温度下反应会生成易爆物e,配平下列方程式:
和浓盐酸在一定温度下反应会生成易爆物e,配平下列方程式:_______
_______ _______HCl(浓)=_______KCl+_______□+_______
_______HCl(浓)=_______KCl+_______□+_______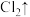 +_______+
+_______+
(2)c物质具有很强的漂白性,但由于其见光易分解,不方便运输和保存,写出c物质见光分解的方程式_______ ,其中还原剂是_______ ,氧化产物是_______ 。
(3)a~g六种物质中属于强电解质的是_______ (填序号,下同),属于弱电解质的是_______ ,属于非电解质的是_______ ,熔融状态下能导电的是_______ 。

(1)
 和浓盐酸在一定温度下反应会生成易爆物e,配平下列方程式:
和浓盐酸在一定温度下反应会生成易爆物e,配平下列方程式:_______
 _______HCl(浓)=_______KCl+_______□+_______
_______HCl(浓)=_______KCl+_______□+_______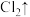 +_______+
+_______+
(2)c物质具有很强的漂白性,但由于其见光易分解,不方便运输和保存,写出c物质见光分解的方程式
(3)a~g六种物质中属于强电解质的是
您最近一年使用:0次



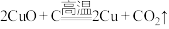 ②
② 完成以下问题:
完成以下问题: 失氧发生
失氧发生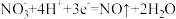 ,已知
,已知 、
、 、
、 四种物质中的—种能使上述还原过程发生。
四种物质中的—种能使上述还原过程发生。

