现有一混合物的水溶液,只可能含有以下离子中的若干种:K+、 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 。现取3份100 mL该溶液分别进行如下实验:
。现取3份100 mL该溶液分别进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝;
第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到白色沉淀,再将沉淀经足量盐酸洗涤,发现沉淀部分溶解。
根据上述实验,试回答下列问题:
(1)由第一份进行的实验对Cl-是否存在的判断是_______ (填“一定存在”“一定不存在”或“不能确定”)。
(2)可以判断该待测液中一定含有的阴离子是_______ ,一定没有的阳离子是_______ 。还有一种阳离子没有检验,检验这种离子的实验方法是_______ ,确定该离子存在的现象是_______ 。
 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 。现取3份100 mL该溶液分别进行如下实验:
。现取3份100 mL该溶液分别进行如下实验:第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝;
第三份加入足量BaCl2溶液后,经过滤、洗涤、干燥,得到白色沉淀,再将沉淀经足量盐酸洗涤,发现沉淀部分溶解。
根据上述实验,试回答下列问题:
(1)由第一份进行的实验对Cl-是否存在的判断是
(2)可以判断该待测液中一定含有的阴离子是
更新时间:2021-12-29 22:05:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种可溶性盐,阳离子分别可能是Ba2+、Na+、Ag+、Cu2+中的某一种,阴离子分别可能是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 中的某一种。把四种盐分别溶于盛有蒸馏水的试管中,只有C盐的溶液呈蓝色。
中的某一种。把四种盐分别溶于盛有蒸馏水的试管中,只有C盐的溶液呈蓝色。
(1)向这四种盐溶液中分别加盐酸,B盐有沉淀产生,D盐有无色无味气体逸出。则它们的化学式应为:
A_______ ,B_______ ,C_______ ,D_______ 。
(2)写出下列反应的离子方程式:
①A+C:_______ 。
②D+盐酸:_______ 。
③A+B:_______ 。
 、SO
、SO 、Cl-、CO
、Cl-、CO 中的某一种。把四种盐分别溶于盛有蒸馏水的试管中,只有C盐的溶液呈蓝色。
中的某一种。把四种盐分别溶于盛有蒸馏水的试管中,只有C盐的溶液呈蓝色。(1)向这四种盐溶液中分别加盐酸,B盐有沉淀产生,D盐有无色无味气体逸出。则它们的化学式应为:
A
(2)写出下列反应的离子方程式:
①A+C:
②D+盐酸:
③A+B:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫化钠,俗称臭碱,是重要的化工原料,工业上可用氢氧化钠吸收硫化氢气体制备。
(1)实验室常用块状硫化亚铁(FeS)固体和稀硫酸布常温下反应制取硫化氢,写出该反应的离子反应方程式:_______ 。利用上述药品,在以下的装置中选择一个合适装置制备硫化氢气体并对该装置进行气密性检查:_______ 。
a. b.
b. c.
c. d.
d. e.
e.
(2)已知:





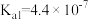
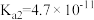

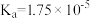
若用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂为_______ 。
a.硝酸 b.碳酸氢钠 c.硼酸 d.醋酸
(3)查阅文献可知,久置硫化钠固体中可能含有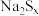 、
、 、S、
、S、 ,为检验
,为检验 变质情况,设计实验如下:
变质情况,设计实验如下:
已知:① (黄色),
(黄色),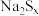 与酸反应生成S和H2S;
与酸反应生成S和H2S;
② 、
、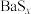 均易溶于水,
均易溶于水, 微溶于水;
微溶于水;
③白色的 难溶于水,且易转化为黑色
难溶于水,且易转化为黑色 。
。
限选试剂:盐酸、稀硫酸、稀硝酸、 溶液、
溶液、 溶液、
溶液、 溶液
溶液
(4)某小组同学为检验 变质的产物中是否含有
变质的产物中是否含有 ,设计实验:取久置潮解的
,设计实验:取久置潮解的 固体溶于水,静置,取少量上层清液于试管中,向其中滴加
固体溶于水,静置,取少量上层清液于试管中,向其中滴加 溶液,产生黑色沉淀。由此得出结论:
溶液,产生黑色沉淀。由此得出结论: 变质的产物中含
变质的产物中含 。该实验是否合理
。该实验是否合理_______ (填“是”或“否”),请分析原因_______ 。
(1)实验室常用块状硫化亚铁(FeS)固体和稀硫酸布常温下反应制取硫化氢,写出该反应的离子反应方程式:
a.
 b.
b. c.
c. d.
d. e.
e.
(2)已知:






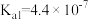
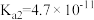

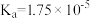
若用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂为
a.硝酸 b.碳酸氢钠 c.硼酸 d.醋酸
(3)查阅文献可知,久置硫化钠固体中可能含有
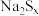 、
、 、S、
、S、 ,为检验
,为检验 变质情况,设计实验如下:
变质情况,设计实验如下:| 实验序号 | 实验操作 | 实验现象 | 结论 |
| 实验I | 取0.5g久置的 固体于试管中。加入 固体于试管中。加入 ,搅拌,静置、过滤 ,搅拌,静置、过滤 | 静置后固体量减少 | 证明变质固体中含有 |
| 实验II | 将实验I过滤得到的固体溶于水,静置后滴加稀硫酸 | 溶解静置,上层清液呈黄色,加酸产生淡黄色沉淀 | 证明变质固体中一定含有 |
| 实验III | 取久置潮解的Na2S固体溶于水,再加足量 | 证明杂质中含有Na2SO4 |
 (黄色),
(黄色),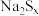 与酸反应生成S和H2S;
与酸反应生成S和H2S;②
 、
、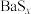 均易溶于水,
均易溶于水, 微溶于水;
微溶于水;③白色的
 难溶于水,且易转化为黑色
难溶于水,且易转化为黑色 。
。限选试剂:盐酸、稀硫酸、稀硝酸、
 溶液、
溶液、 溶液、
溶液、 溶液
溶液(4)某小组同学为检验
 变质的产物中是否含有
变质的产物中是否含有 ,设计实验:取久置潮解的
,设计实验:取久置潮解的 固体溶于水,静置,取少量上层清液于试管中,向其中滴加
固体溶于水,静置,取少量上层清液于试管中,向其中滴加 溶液,产生黑色沉淀。由此得出结论:
溶液,产生黑色沉淀。由此得出结论: 变质的产物中含
变质的产物中含 。该实验是否合理
。该实验是否合理
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】甲、乙、丙、丁四种易溶于水的物质分别由NH 、Ba2+、Mg2+、H+、OH-、Cl-、HCO
、Ba2+、Mg2+、H+、OH-、Cl-、HCO 、SO
、SO 中的不同阳离子和阴离子各一种组成。
中的不同阳离子和阴离子各一种组成。
已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)由②可知乙溶液中含有的阴离子是___ 。
(2)写出下列物质化学式:甲___ ;丁___ 。
(3)写出甲与乙反应的离子方程式:___ 。
(4)写出足量的甲与丁反应的离子方程式:___ 。
 、Ba2+、Mg2+、H+、OH-、Cl-、HCO
、Ba2+、Mg2+、H+、OH-、Cl-、HCO 、SO
、SO 中的不同阳离子和阴离子各一种组成。
中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)由②可知乙溶液中含有的阴离子是
(2)写出下列物质化学式:甲
(3)写出甲与乙反应的离子方程式:
(4)写出足量的甲与丁反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】中学化学中几种常见物质的转化关系如下:

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出A、B、H的化学式:A___________ 、B___________ 、H___________ 。
(2)写出C的酸性溶液与双氧水反应的离子方程式:___________ 。
(3)写出鉴定E中阳离子的实验方法和现象:___________ 。
(4)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:___________ 。

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出A、B、H的化学式:A
(2)写出C的酸性溶液与双氧水反应的离子方程式:
(3)写出鉴定E中阳离子的实验方法和现象:
(4)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
您最近一年使用:0次
【推荐2】现有NH4Cl、(NH4)2SO4、NaCl、Na2SO4四种溶液,某化学兴趣小组设计如下实验可将其鉴别出来。实验步骤如下:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的NaOH溶液、加热、将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量BaCl2溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
根据所学知识,按要求回答下列问题:
(1)溶液A、D中的溶质依次为_______ 、_______ 。 (填化学式)
(2)溶液B与NaOH溶液共热时发生反应的离子方程式为_______ 。
(3)步骤②试管中产生的白色沉淀的化学式为_______ 。
(4)检验溶液D中溶质的阴离子的具体实验操作为_______ , 发生反应的化学方程式为_______ 。
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的NaOH溶液、加热、将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量BaCl2溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
根据所学知识,按要求回答下列问题:
(1)溶液A、D中的溶质依次为
(2)溶液B与NaOH溶液共热时发生反应的离子方程式为
(3)步骤②试管中产生的白色沉淀的化学式为
(4)检验溶液D中溶质的阴离子的具体实验操作为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学要对某溶液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
(1)
(2)根据以上的实验报告,关于滤液的成分,他的结论是:滤液中含有氯化铵和氯化锌。
若想从滤液中得到溶质固体,还应进行的操作是加热蒸发(加热浓缩),_______ , 过滤。
若要将所得的溶质固体中的物质加以分离,可用_____________ 法。
(1)
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中, | 含有Cl- | |
| 2.检验NH4+ | 取少许滤液于试管中, | 含有NH4+ | |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
(2)根据以上的实验报告,关于滤液的成分,他的结论是:滤液中含有氯化铵和氯化锌。
若想从滤液中得到溶质固体,还应进行的操作是加热蒸发(加热浓缩),
若要将所得的溶质固体中的物质加以分离,可用
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO )=
)=___________ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度是___________ ;
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:___________ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式为___________ 。
 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO
 )=
)=(2)某同学认为该溶液中一定存在K+,浓度是
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:
(4)写出③中固体加入足量盐酸洗涤的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:

(1)操作Ⅰ的名称是__ 。
(2)用H2SO4“酸浸”时的离子方程式为__ (任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__ 。
(4)“煅烧”时的化学方程式为__ 。
(5)沉淀A与氢氟酸反应的化学方程式为__ 。

(1)操作Ⅰ的名称是
(2)用H2SO4“酸浸”时的离子方程式为
(3)简述如何检验酸浸后溶液中是否有Fe3+
(4)“煅烧”时的化学方程式为
(5)沉淀A与氢氟酸反应的化学方程式为
您最近一年使用:0次
【推荐3】某学习小组欲从含有[Cu(NH3)4]SO4、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵[CuSO4·(NH4)2SO4]固体,完成了如下实验:
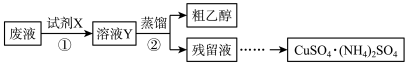
已知:[Cu(NH3)4]2++4H+==Cu2++4NH4+
请回答:
(1)步骤①中,试剂X应采用_____________________________________________ 。
(2)甲、乙两同学取相同量的溶液Y分别进行蒸馏,收集到的馏出液体积相近,经检测,甲同学的馏出液中乙醇含量明显偏低,可能的原因是_______________________________________________ 。
(3)设计实验方案验证硫酸铜铵固体中的NH4+___________________________________________

已知:[Cu(NH3)4]2++4H+==Cu2++4NH4+
请回答:
(1)步骤①中,试剂X应采用
(2)甲、乙两同学取相同量的溶液Y分别进行蒸馏,收集到的馏出液体积相近,经检测,甲同学的馏出液中乙醇含量明显偏低,可能的原因是
(3)设计实验方案验证硫酸铜铵固体中的NH4+
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】现有1 L未知成分的混合溶液,其中除了含有0.2 mol的Na⁺外,还可能含有下列离子中的一种或几种:
现进行如下实验操作(每次实验所加试剂均过量):
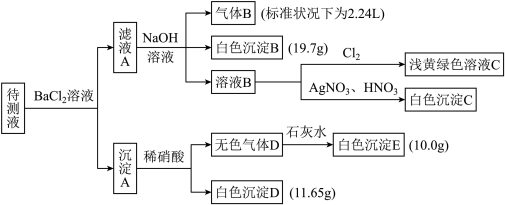
已知:① +OH-
+OH- NH3+H2O;
NH3+H2O;
②Cl2+2Br-=Br2+2Cl-;
③Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
(1)由气体B可确定待测液中含有的离子是_____ 。
(2)由沉淀D和沉淀E可以判断待测液中一定含有_____ 离子,据此可以排除的离子是_____ 。
(3)由白色沉淀B可确定待测液中含有的离子是_____ ,写出产生沉淀B的离子方程式_____ 。
(4)某同学读图后,认为待测液中一定不含Br-,他的判断依据是_____ 。
(5)综合分析,此1 L待测液中K+的物质的量的取值范围为_____ 。
| 阳离子 | K⁺、 、Mg2+、Ba2+、Fe3+ 、Mg2+、Ba2+、Fe3+ |
| 阴离子 | Cl⁻、Br⁻、 、 、 、 、 |

已知:①
 +OH-
+OH- NH3+H2O;
NH3+H2O;②Cl2+2Br-=Br2+2Cl-;
③Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
(1)由气体B可确定待测液中含有的离子是
(2)由沉淀D和沉淀E可以判断待测液中一定含有
(3)由白色沉淀B可确定待测液中含有的离子是
(4)某同学读图后,认为待测液中一定不含Br-,他的判断依据是
(5)综合分析,此1 L待测液中K+的物质的量的取值范围为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某强酸性无色溶液中可能含下表离子中的若干种。
实验Ⅰ:取少量该强酸性溶液A进行如图1实验。
实验Ⅱ:为了进一步确定该溶液的组成,取100mL原溶液A,向该溶液中滴加 的
的 溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图2所示。
溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图2所示。


回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有_______ 。
(2)该溶液中一定存在的离子是有_______ 。
(3)检验气体X的方法是有_______ 。
(4)写出图2中BC段对应的离子方程式有_______ 。
(5)通过上述信息可知,该溶液中阴离子的浓度为有_______  。
。
| 阳离子 |  、 、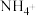 、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 、 、 |
实验Ⅱ:为了进一步确定该溶液的组成,取100mL原溶液A,向该溶液中滴加
 的
的 溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图2所示。
溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图2所示。

回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有
(2)该溶液中一定存在的离子是有
(3)检验气体X的方法是有
(4)写出图2中BC段对应的离子方程式有
(5)通过上述信息可知,该溶液中阴离子的浓度为有
 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32-中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。

试推断并完成作答:
(1)溶液中一定含有的离子是___________ ;
(2)溶液中肯定不含有的离子是_________ ;
(3)检验可能含有的离子的方法是____________ 。
(4)图示中a点沉淀的成分是______________ 。
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。

试推断并完成作答:
(1)溶液中一定含有的离子是
(2)溶液中肯定不含有的离子是
(3)检验可能含有的离子的方法是
(4)图示中a点沉淀的成分是
您最近一年使用:0次



