X、Y、Z、W、R为原子序数依次增大的五种短周期元素。同温同压下,相同物质的量的X和Y的单质分别与足量稀盐酸反应,生成H2的体积之比为1∶3;R的单质具有较强的氧化性;W元素的核电荷数等于Z、R元素的原子序数之和的一半。请回答下列问题:
(1)X的元素符号为___________ ;W元素在周期表中的位置为___________ 。
(2)R元素的最高价氧化物对应的水化物的化学式为___________ 。
(3)Y、Z、W、R四种元素的非金属性由强到弱的顺序是___________ (用元素符号表示),从原子结构角度解释其原因:___________ 。
(4)硒(Se)与W为同族元素,镓(Ga)和铟(In)与Y为同族元素,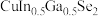 中Cu的化合价为
中Cu的化合价为___________ 。
(5)W与R形成的化合物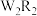 中所有原子最外层都满足8电子结构,其结构式为
中所有原子最外层都满足8电子结构,其结构式为___________ ,用电子式表示其形成过程:___________ 。
(1)X的元素符号为
(2)R元素的最高价氧化物对应的水化物的化学式为
(3)Y、Z、W、R四种元素的非金属性由强到弱的顺序是
(4)硒(Se)与W为同族元素,镓(Ga)和铟(In)与Y为同族元素,
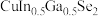 中Cu的化合价为
中Cu的化合价为(5)W与R形成的化合物
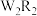 中所有原子最外层都满足8电子结构,其结构式为
中所有原子最外层都满足8电子结构,其结构式为
更新时间:2022-02-25 21:59:53
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、R五种前四周期元素,原子序数依次增大,其中X原基态时最外层电子数是其内层电子总数的2倍,Z原子基态时s电子数与p电子数相等,Z2-和W+有相同的核外电子排布;R的原子序数为29。回答下列问题:
(1)Y、Z、W三种元素的第一电离能由小到大的顺序为______ (用元素符号表示)。
(2)若M分子是Y2Z的等电子体,M的结构式为______ , M分子的中心原子的轨道杂化类型为________ , 1molM中含有_____ molσ键。
(3)Y的简单氢化物极易溶于Z的简单氢化物中,其主要原因是_____________ 。
(4)基态R+离子的核外电子排布式是__________ ,R的高价离子与Y的最常见氢化物形成的配离子的化学式为________________ 。
(5)Z与W形成的化合物W2Z的晶胞如图。其中Z离子的配位数为________ ,与一个Z离子距离最近的所有W离子为顶点构成的几何体为________ 结构。若W2Z的晶胞边长为a pm,则该化合物的密度为_______ g·cm-3(列出计算式即可,阿伏伽德罗常数用NA表示)。
(1)Y、Z、W三种元素的第一电离能由小到大的顺序为
(2)若M分子是Y2Z的等电子体,M的结构式为
(3)Y的简单氢化物极易溶于Z的简单氢化物中,其主要原因是
(4)基态R+离子的核外电子排布式是
(5)Z与W形成的化合物W2Z的晶胞如图。其中Z离子的配位数为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素A、B、C、D、E、F的原子序数逐渐增大,A和B同周期,A和F同族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的简单阴离子与C、D、E的简单阳离子电子层结构相同。请回答下列有关问题:
(1)F在元素周期表中的位置是_____________ 。
(2)C2B2的电子式是_________ ;AB2的结构式是_______ 。
(3)B、C、D、E离子半径由大到小的顺序为______ (用离子符号回答); C、D、E最高价氧化物对应水化物的碱性由强到弱的顺序为____________ (用化学式表示,且用“>”符号连接回答)。
(4) C、E最高价氧化物对应水化物能够相互反应,则反应的离子方程式为___________ 。
(1)F在元素周期表中的位置是
(2)C2B2的电子式是
(3)B、C、D、E离子半径由大到小的顺序为
(4) C、E最高价氧化物对应水化物能够相互反应,则反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As(Ⅲ)亚砷酸盐和As(Ⅴ)砷酸盐形式存在。
(1)砷与磷为同一主族元素,砷的原子序数为________________ 。
(2)根据元素周期律,下列说法正确的是__________________ 。
a.酸性: H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______ 。
Ⅱ.(4)A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图:

若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素为________ (写元素名称),它在周期表中的位置为______ 。
②该金属元素的单质与某氧化物在高温下反应,常用于焊接铁轨及定向爆破,该反应的化学方程式为________ 。
Ⅲ.铁及其化合物在生活中有广泛应用。
(5)Fe3+基态核外电子排布式为______ 。
(6)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为______ 。

(7)某铁的化合物结构简式如图所示:

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为______ (用元素符号表示)。
②上述化合物中氮原子的杂化方式为______ 。
(1)砷与磷为同一主族元素,砷的原子序数为
(2)根据元素周期律,下列说法正确的是
a.酸性: H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为
Ⅱ.(4)A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图:

若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素为
②该金属元素的单质与某氧化物在高温下反应,常用于焊接铁轨及定向爆破,该反应的化学方程式为
Ⅲ.铁及其化合物在生活中有广泛应用。
(5)Fe3+基态核外电子排布式为
(6)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为

(7)某铁的化合物结构简式如图所示:

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为
②上述化合物中氮原子的杂化方式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X﹣的半径,Y2是空气主要成分之一,请回答:
(1)Q元素在周期表中的位置___________ ;
(2)这五种元素原子半径从大到小的顺序为___________ (填元素符号)。
(3)元素的非金属性Z___________ Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有___________ (填序号)。
A.Q的氢化物的水溶液放置在空气中会变浑浊 B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态 D.Z和Q在周期表中的位置
(4)Q的氢化物与它的低价氧化物反应的化学方程式为___________
(5)X与Y可形成分子A,也可形成阳离子B,写出A的化学式___________ ;实验室制备气体A的化学方程式___________ 。
(1)Q元素在周期表中的位置
(2)这五种元素原子半径从大到小的顺序为
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊 B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态 D.Z和Q在周期表中的位置
(4)Q的氢化物与它的低价氧化物反应的化学方程式为
(5)X与Y可形成分子A,也可形成阳离子B,写出A的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】原子序数依次递增的A、B、C、D、E、F五种元素,其中A、B、C属于同一周期,A原子最外层p能级中的电子数等于次外层的电子总数,C原子最外层中有2个不成对的电子;元素D的焰色试验呈紫色;E原子的最高能层为N层,且在同周期元素的基态原子中不成对电子数最多;F的原子序数为26。请回答下列问题:
(1)A、B、C三种元素的第一电离能由大到小的顺序为_______ 。
(2)说明元素D具有焰色试验的原因:_______ 。
(3)E的基态原子的外围电子排布式为_______ 。
(4)F在元素周期表中的位置是_______ 。
(1)A、B、C三种元素的第一电离能由大到小的顺序为
(2)说明元素D具有焰色试验的原因:
(3)E的基态原子的外围电子排布式为
(4)F在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种短周期元素,原子半径大小顺序为:D>A>B>C。已知:C原子的最外层电子数是次外层的3倍,D原子的核外电子数比C原子的核外电子数多4,B、C两元素在周期表的位置相邻,且B和C所构成的阴离子电子总数为32 ,A元素最高价氧化物对应水化物的分子式为HXAOY,其分子中A的原子核外电子数比氢、氧原子的核外电子总数之和少16。HXAOY的相对分子质量比A的气态氢化物的相对分子质量多64。试回答下列问题:
(1)写出元素符号:A_______ ,B_______ ,C_______ 。
(2)A和D两元素组成的化合物的晶体类型是_______ ,其电子式为_______ 。
(1)写出元素符号:A
(2)A和D两元素组成的化合物的晶体类型是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】原子序数依次增大的四种常见元素W、X、Y、Z,均可形成一种或多种氧化物。其中W、Y的氧化物是导致酸雨的主要物质,X的氧化物既可以和强酸、亦可以和强碱反应,Z则具有砖红色和黑色的两种氧化物。
(1)W元素在元素周期表的位置为____________ ,用电子式表示其气态氢化物________ 。
(2)含有X的某种物质常用作净水剂,用离子方程式表示其净水的原理是_____________ 。
(3)Y的一种氧化物,属于酸性氧化物,它既具有氧化性,也具有还原性,还具有漂白性。设计实验,验证该氧化物具有还原性,其操作方法是______________ 。
(4)一定物质的量的稀硝酸恰能将Z的砖红色的氧化物氧化,自身被还原成NO。则反应中氧化剂与还原剂的物质的量的比为____________ 。
(1)W元素在元素周期表的位置为
(2)含有X的某种物质常用作净水剂,用离子方程式表示其净水的原理是
(3)Y的一种氧化物,属于酸性氧化物,它既具有氧化性,也具有还原性,还具有漂白性。设计实验,验证该氧化物具有还原性,其操作方法是
(4)一定物质的量的稀硝酸恰能将Z的砖红色的氧化物氧化,自身被还原成NO。则反应中氧化剂与还原剂的物质的量的比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知X、Y分别由原子序数依次增大的A、B、C、D四种短周期元素中的两种组成,A、B、C同周期,且C原子能形成双原子阴离子。已知化合物X是离子化合物,其阴、阳离子具有相同的电子层结构,气体甲是天然气的主要成分。
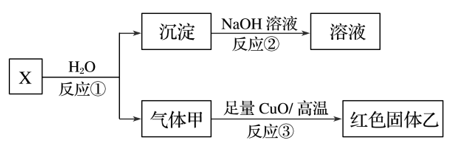
(1)气体甲的电子式:______________ ,写出反应①的化学方程式:_________________________ 。
(2)若红色固体乙是一种单质,写出反应③的化学方程式:_________________________________________ 。
(3)有人认为,乙中还含有Cu2O,请设计实验证明:_____________________________________ 。
(已知Cu2O+2H+===Cu+Cu2++H2O)

(1)气体甲的电子式:
(2)若红色固体乙是一种单质,写出反应③的化学方程式:
(3)有人认为,乙中还含有Cu2O,请设计实验证明:
(已知Cu2O+2H+===Cu+Cu2++H2O)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表列出了10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的是_______ ,电负性最小的金属元素是_______ 。
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是_______ 。
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是_______ 。
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为_______ 、_______ 。
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:_______ 。
(7)⑨元素原子的价电子的轨道表示式为_______ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑤ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑥ | ⑧ | ⑩ | |||
| 第4周期 | ② | ④ | ⑨ |
(2)①③⑥三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的简单离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应的水化物的化学式分别为
(5)①和⑥的最高价氧化物对应的水化物相互反应的离子方程式为
(6)用电子式表示第三周期主族元素中电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素原子的价电子的轨道表示式为
您最近一年使用:0次



