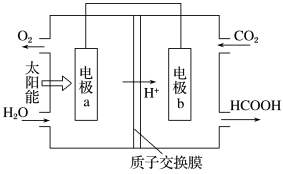
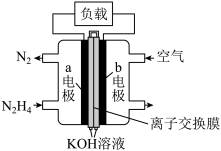
原电池正负极材料和离子导体的选择
负极材料选择 :_______
正极材料选择 :_______
离子导体选择:_______
负极材料选择 :
正极材料选择 :
离子导体选择:
更新时间:2022/03/02 19:45:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据有关知识,填写下列空白:
(1)拆开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3_____ 热量(填“吸收”或“放出”)_____ kJ;事实上,反应的热量总小于理论值,理由是_____ 。
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
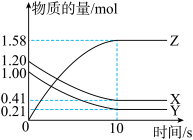
①写出该反应的化学方程式_____ 。
②从开始到10s用Z表示该反应的速率为______ 。
③为加快该反应的反应速率,可采取的措施是_____ 。
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。
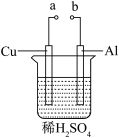
a和b用导线连接,Cu极为原电池______ 极填(“正”或“负”)。Al极发生_____ 填(“氧化”或“还原”)反应。溶液中SO 移向
移向_____ (填“Cu”或“Al”极)。溶液pH_____ (填增大或减小)。
(1)拆开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ。则理论上1molN2生成NH3
(2)一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

①写出该反应的化学方程式
②从开始到10s用Z表示该反应的速率为
③为加快该反应的反应速率,可采取的措施是
A.适当升高温度 B.恒容时充入Ne使压强增大
C.增大容器的体积 D.选择高效催化剂
(3)某兴趣小组为研究原电池原理,设计如图装置。

a和b用导线连接,Cu极为原电池
 移向
移向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质发生化学反应时,常常伴随有能量变化。某学习小组用如图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
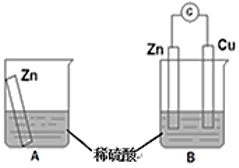
(1)A烧杯中反应的离子方程式为___________ 。
(2)B中Zn板是___________ 极,发生反应的电极反应式是___________ 。
(3)从能量转化的角度来看,A、B中反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为___________ ,B中是将化学能转变为___________ 。
(4)该小组同学反思原电池的原理,其中观点正确的是___________(填字母序号)。

(1)A烧杯中反应的离子方程式为
(2)B中Zn板是
(3)从能量转化的角度来看,A、B中反应物的总能量
(4)该小组同学反思原电池的原理,其中观点正确的是___________(填字母序号)。
| A.原电池反应的过程中一定有电子转移 |
| B.原电池装置需要2个电极 |
| C.电极一定都参加反应 |
| D.氧化反应和还原反应可以拆开在两极发生 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有反应:
A.2H2O2 H2O+O2↑
H2O+O2↑
B.Fe+H2SO4=FeSO4+H2↑
C.Na2CO3·10H2O与NH4NO3反应制作冷敷袋
D.2KOH+H2SO4=K2SO4+2H2O
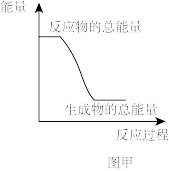
(1)上述四个反应过程中能量变化符合如图甲的是_______ (填序号)。
(2)上述四个反应中可用于设计成如图乙的原电池的反应是_______ (填反应序号)。根据该原电池回答下列问题:
①负极反应式为_______ ;正极发生_______ (填“氧化”或“还原”)反应。
②当导线中有2mol电子通过时,理论上发生的变化是_______ (填序号)。
a.溶液增重56g b.溶液增重54g c.析出1g H2 d.析出11.2L H2(标准状况)

(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2),请将此反应设计成原电池,请根据图乙画出该原电池的装置图,注明电极材料,电解质溶液,电子流向。_______
A.2H2O2
 H2O+O2↑
H2O+O2↑ B.Fe+H2SO4=FeSO4+H2↑
C.Na2CO3·10H2O与NH4NO3反应制作冷敷袋
D.2KOH+H2SO4=K2SO4+2H2O
(1)上述四个反应过程中能量变化符合如图甲的是

(2)上述四个反应中可用于设计成如图乙的原电池的反应是
①负极反应式为
②当导线中有2mol电子通过时,理论上发生的变化是
a.溶液增重56g b.溶液增重54g c.析出1g H2 d.析出11.2L H2(标准状况)

(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2),请将此反应设计成原电池,请根据图乙画出该原电池的装置图,注明电极材料,电解质溶液,电子流向。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应与能量变化对人类生产、生活有重要的意义。回答下列问题:
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
①装置甲中负极为___________ (填“A”或“B”)。
②装置乙中正极的电极反应式为___________ 。
③装置丙中溶液的pH___________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是___________ 。
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:___________ 。
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:
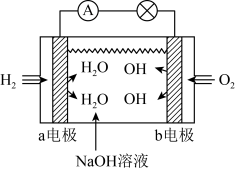
a电极是___________ 极,此时b电极发生反应的电极反应式是___________ , 向
向___________ (填“a”或“b”)电极移动。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 | 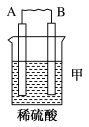 | 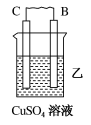 | 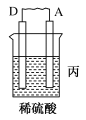 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是
 向
向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电池的发展是化学对人类的一项重大贡献。用图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流计。请回答下列问题:

(1)以下叙述中,正确的是_______ (填选项字母)。
a.甲中锌片是负极,乙中铜片是正极 b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的 均减小 d.乙中电流从铜片经导线流向锌片
均减小 d.乙中电流从铜片经导线流向锌片
e.乙烧杯中 向铜片方向移动
向铜片方向移动
(2)乙装置中负极的电极反应式为:_______ ;当乙中产生1.12L(标准状况)气体时,通过导线的电子数为_______  ;若电路导线上通过电子1mol,则理论上两极的变化是
;若电路导线上通过电子1mol,则理论上两极的变化是_______ (填选项字母)。
a.锌片质量减少32.5g b.锌片增重32.5g
c.铜片上析出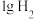 d.铜片上析出
d.铜片上析出
(3)将 与
与 的燃烧反应设计成燃料电池,装置如图所示(A、B为多孔碳棒)。实验测得
的燃烧反应设计成燃料电池,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则A电极入口通
定向移向A电极,则A电极入口通_______ 气体(填“ ”或“
”或“ ”)。该装置中实现的能量转化关系为
”)。该装置中实现的能量转化关系为_______ 。


(1)以下叙述中,正确的是
a.甲中锌片是负极,乙中铜片是正极 b.两烧杯中铜片表面均有气泡产生
c.两烧杯中溶液的
 均减小 d.乙中电流从铜片经导线流向锌片
均减小 d.乙中电流从铜片经导线流向锌片e.乙烧杯中
 向铜片方向移动
向铜片方向移动(2)乙装置中负极的电极反应式为:
 ;若电路导线上通过电子1mol,则理论上两极的变化是
;若电路导线上通过电子1mol,则理论上两极的变化是a.锌片质量减少32.5g b.锌片增重32.5g
c.铜片上析出
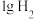 d.铜片上析出
d.铜片上析出
(3)将
 与
与 的燃烧反应设计成燃料电池,装置如图所示(A、B为多孔碳棒)。实验测得
的燃烧反应设计成燃料电池,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则A电极入口通
定向移向A电极,则A电极入口通 ”或“
”或“ ”)。该装置中实现的能量转化关系为
”)。该装置中实现的能量转化关系为
您最近一年使用:0次