下表为元素周期表中的一部分,列出10种元素在周期表中的位置,用化学符号回答下列各题。
(1)10种元素中,化学性质最不活泼的是___________ 。
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物的化学式为___________ 。
(5)①和⑨两元素形成化合物的电子式为___________ :该化合物焰色试验为___________ 色。
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为___________ 。
| 主族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨两元素形成化合物的电子式为
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为
更新时间:2022-03-08 17:52:25
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
(1)①~⑩中,最活泼的金属元素是________ (写元素符号,下同),最不活泼的元素是________ 。
(2)①⑧的简单离子,其半径更大的是________ (写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是____________ (填化学式)。
(4)元素的非金属性:⑥________ ⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是____________ (填化学式);碱性最强的是__________ (填化学式),该碱与⑤的最高价氧化物的水化物反应的离子方程式为__________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ② | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①⑧的简单离子,其半径更大的是
(3)⑧⑨的气态氢化物,更稳定的是
(4)元素的非金属性:⑥
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请回答下列问题:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):____ ,理由是____ 。
(2)Y是_____ W是____ (填元素符号)。
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式_____ 。
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请回答下列问题:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):
(2)Y是
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,请回答有关问题:
(1)⑧的元素符号是_____________ ;⑤号元素最高价氧化物对应的水化物为_____________ (写出化学式);
(2)表中原子半径最大的元素是_____________ ;非金属性最强的元素是_____________ ;(填元素符号)
(3)表中能形成两性氢氧化物的元素是_____________ (填写元素符号);写出该氢氧化物与⑥的最高价氧化物对应水化物反应的化学方程式:________________________________________ ;
(4)⑥、⑦、⑨三种元素的简单离子的半径大小顺序为_____________ (用“>”连接离子符号);
(5)工业上从海水大规模提取元素⑩的单质X的常用方法,流程如下:

分别写出流程a和c中发生的离子方程式:_____________________ 、_____________________ .
(6)用 从水溶液中提取⑩的单质X所使用的操作是
从水溶液中提取⑩的单质X所使用的操作是_____________ .
|
|
|
|
|
|
| 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)⑧的元素符号是
(2)表中原子半径最大的元素是
(3)表中能形成两性氢氧化物的元素是
(4)⑥、⑦、⑨三种元素的简单离子的半径大小顺序为
(5)工业上从海水大规模提取元素⑩的单质X的常用方法,流程如下:

分别写出流程a和c中发生的离子方程式:
(6)用
 从水溶液中提取⑩的单质X所使用的操作是
从水溶液中提取⑩的单质X所使用的操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮、磷、砷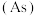 、锑
、锑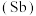 、铋
、铋 、镆
、镆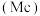 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)氮和磷氢化物性质的比较:热稳定性:
___________  (填“>”“<”)。 沸点:
(填“>”“<”)。 沸点:
___________ 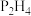 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是___________ 。
(2) 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是___________ (填序号)。
a.不能与 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应
(3) 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式 ___________ ,因此,配制 溶液应注意
溶液应注意___________ 。
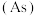 、锑
、锑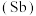 、铋
、铋 、镆
、镆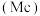 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:(1)氮和磷氢化物性质的比较:热稳定性:

 (填“>”“<”)。 沸点:
(填“>”“<”)。 沸点:
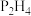 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(2)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是a.不能与
 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应(3)
 能发生较强烈的水解,生成难溶的
能发生较强烈的水解,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式  溶液应注意
溶液应注意
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
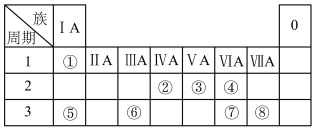
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ,元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键”或“离子键和共价键”),将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 和
和 的分子的电子式分别是
的分子的电子式分别是_______ 、_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 和
和 的分子的电子式分别是
的分子的电子式分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
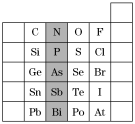
(1)阴影部分元素在元素周期表中的位置为___ 族。
(2)根据元素周期律预测:H3AsO4属于____ (填“强酸”或“弱酸”)。
(3)C和Si元素的氢化物都可以燃烧,但Si元素的氢化物在空气中可以自燃,试写出其完全燃烧的化学方程式:____ 。
(4)试比较S、O、F三种元素的原子半径大小:____ (填元素符号)。

(1)阴影部分元素在元素周期表中的位置为
(2)根据元素周期律预测:H3AsO4属于
(3)C和Si元素的氢化物都可以燃烧,但Si元素的氢化物在空气中可以自燃,试写出其完全燃烧的化学方程式:
(4)试比较S、O、F三种元素的原子半径大小:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)在此元素周期表的一部分中,金属性最强的元素是_______ (填元素符号)。
(2)⑤、⑥的原子半径由大到小的顺序为_______ (填元素符号)。
(3)⑦、⑧两种元素的氢化物稳定性较强的是_______ (用化学式表示)。
(4)⑤、⑧的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。

(1)在此元素周期表的一部分中,金属性最强的元素是
(2)⑤、⑥的原子半径由大到小的顺序为
(3)⑦、⑧两种元素的氢化物稳定性较强的是
(4)⑤、⑧的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知: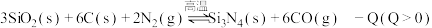 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子占有_______ 种能量不同的轨道。 属于
属于_______ 晶体。
(5)非金属性:S小于O。试用一个实验事实说明_______ 。
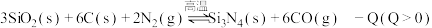 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子占有
 属于
属于(5)非金属性:S小于O。试用一个实验事实说明
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
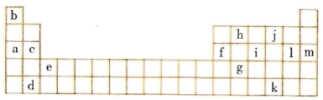
【推荐1】下表是现行中学化学教科书中元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题。

(1)② 表示的元素是______ (填元素符号);
(2)①、⑤两种元素的原子半径大小为①______ ⑤(填“< ”或“>”);
(3)③、④两种元素的金属性强弱顺序为:③______ ④(填“< ”或“>”);
(4)写出③与⑥两种元素所形成化合物的化学式_________ 。

(1)② 表示的元素是
(2)①、⑤两种元素的原子半径大小为①
(3)③、④两种元素的金属性强弱顺序为:③
(4)写出③与⑥两种元素所形成化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素单质及其化合物有广泛用途,请根据周期表中第3周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___________ 。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___________ ,氧化性最弱的简单阳离子是___________ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是___________ 。
a.NH3 b.HI c.SO2 d.CO2
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某粒子的结构示意图为:

试回答:
(1)当x-y=10时,该粒子为________ (填“原子”或“阳离子”“阴离子”)。
(2)当y=8时,该粒子可能是(写4种,写化学式):_______ 、________ 、_______ 、_______ 。
(3)比较当y=4时的元素氢化物与甲烷的稳定性______________ (填氢化物的化学式)。
(4)比较y=5、y=6、y=7的元素最高价氧化物对应水化物酸性强弱(写对应酸的化学式)________________________________ 。

试回答:
(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(写4种,写化学式):
(3)比较当y=4时的元素氢化物与甲烷的稳定性
(4)比较y=5、y=6、y=7的元素最高价氧化物对应水化物酸性强弱(写对应酸的化学式)
您最近一年使用:0次

 )最大的是
)最大的是