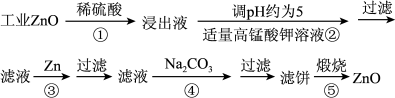
以黄铁矿(主要成分 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
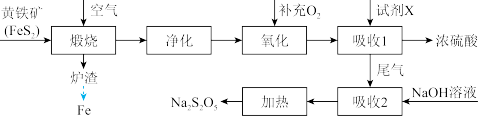
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)黄铁矿( )在空气中煅烧的化学方程式为
)在空气中煅烧的化学方程式为___________ 。
(3)工业上,吸收 时宜选用的试剂X为98.3%的浓硫酸,目的是
时宜选用的试剂X为98.3%的浓硫酸,目的是___________ 。
(4)因为 (焦亚硫酸钠)具有还原性,导致商品
(焦亚硫酸钠)具有还原性,导致商品 方中不可避免地存在
方中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是___________ 。
(5)某化学实验小组取1.0g黄铁矿样品在空气中充分灼烧(假设杂质不参加反应),生成的 气体恰好被
气体恰好被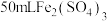 ,溶液完全吸收,在所得溶液中加入足量
,溶液完全吸收,在所得溶液中加入足量 溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
①原 溶液的物质的量浓度为
溶液的物质的量浓度为___________ ,黄铁矿中 的质量分数为
的质量分数为___________ 。
②工业上煅烧10t上述黄铁矿,产生的 经催化氧化制硫酸,理论上可制得98%的浓硫酸
经催化氧化制硫酸,理论上可制得98%的浓硫酸___________ t。
 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)黄铁矿(
 )在空气中煅烧的化学方程式为
)在空气中煅烧的化学方程式为(3)工业上,吸收
 时宜选用的试剂X为98.3%的浓硫酸,目的是
时宜选用的试剂X为98.3%的浓硫酸,目的是(4)因为
 (焦亚硫酸钠)具有还原性,导致商品
(焦亚硫酸钠)具有还原性,导致商品 方中不可避免地存在
方中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是(5)某化学实验小组取1.0g黄铁矿样品在空气中充分灼烧(假设杂质不参加反应),生成的
 气体恰好被
气体恰好被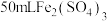 ,溶液完全吸收,在所得溶液中加入足量
,溶液完全吸收,在所得溶液中加入足量 溶液充分反应后,过滤、洗涤、干燥得9.32g固体。
溶液充分反应后,过滤、洗涤、干燥得9.32g固体。①原
 溶液的物质的量浓度为
溶液的物质的量浓度为 的质量分数为
的质量分数为②工业上煅烧10t上述黄铁矿,产生的
 经催化氧化制硫酸,理论上可制得98%的浓硫酸
经催化氧化制硫酸,理论上可制得98%的浓硫酸
更新时间:2022-03-26 23:00:44
|
相似题推荐
【推荐1】A、储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质—碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、 、
、 、
、 、
、 、
、 和
和 七种。
七种。
(1)请用上述物质填空(不用配平):_____
 。
。
(2)上述反应中氧化剂是(填化学式)______ ,被氧化的元素是(填元素符号)______ 。
(3) 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。
B、 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: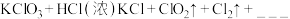
(4)请完成该化学方程式__________________
(5)浓盐酸在反应中显示出来的性质是______ (填写编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生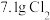 ,则生成
,则生成 的质量为
的质量为_____  。
。
(7) 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的_____ 倍(小数点后保留两位数字)。
 、
、 、
、 、
、 、
、 和
和 七种。
七种。(1)请用上述物质填空(不用配平):
 。
。(2)上述反应中氧化剂是(填化学式)
(3)
 在上述反应中表现出来的性质是(填选项序号)______。
在上述反应中表现出来的性质是(填选项序号)______。| A.氧化性 | B.氧化性和酸性 | C.酸性 | D.还原性和酸性 |
B、
 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为: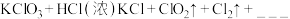
(4)请完成该化学方程式
(5)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(6)若产生
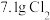 ,则生成
,则生成 的质量为
的质量为 。
。(7)
 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】称取软锰矿样品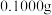 .对样品进行如下处理
.对样品进行如下处理
①用过氧化钠处理,得到 溶液;
溶液;
②煮沸溶液,除去剩余的过氧化物;
③酸化溶液, 歧化为
歧化为 和
和 ;
;
④滤去 ;
;
⑤用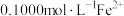 标准溶液滴定滤液中
标准溶液滴定滤液中 ,共用去
,共用去 。
。
计算样品中 的质量分数(保留1位小数;写出简要的计算过程)
的质量分数(保留1位小数;写出简要的计算过程)____________ 。
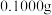 .对样品进行如下处理
.对样品进行如下处理①用过氧化钠处理,得到
 溶液;
溶液;②煮沸溶液,除去剩余的过氧化物;
③酸化溶液,
 歧化为
歧化为 和
和 ;
;④滤去
 ;
;⑤用
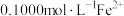 标准溶液滴定滤液中
标准溶液滴定滤液中 ,共用去
,共用去 。
。计算样品中
 的质量分数(保留1位小数;写出简要的计算过程)
的质量分数(保留1位小数;写出简要的计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】成都天府国际机场建设工程巨大,仅钢筋用量可修建11座法国埃菲尔铁塔。
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢___________ 。(填“高”或“低”)
(2)铁制品锈蚀的实质是:铁与空气中的___________ 发生了化学反应。
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是___________ 。(写化学方程式)
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?________
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢
(2)铁制品锈蚀的实质是:铁与空气中的
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含
 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)2molSO2和3molO2的分子数之比为___________ ,原子数之比___________
(2)19g某氯化物MCl2,含有0.4mol Cl-,则M的相对原子质量为___________ ;
(3)同温同压下,CH4气体和CO气体密度之比为___________ ;
(4)从100mL0.1mol/L Al2(SO4)3溶液中取出10mL,则这10mL溶液中Al3+的物质的量为___________ ,SO 的物质的量浓度是
的物质的量浓度是___________ ;
(5)向0.1mol/LBa(OH)2溶液中匀速逐滴加入0.2 mol/LH2SO4溶液直至过量,发生反应的离子方程式为:___________ ,溶液的导电情况如何变化:___________ 。
(1)2molSO2和3molO2的分子数之比为
(2)19g某氯化物MCl2,含有0.4mol Cl-,则M的相对原子质量为
(3)同温同压下,CH4气体和CO气体密度之比为
(4)从100mL0.1mol/L Al2(SO4)3溶液中取出10mL,则这10mL溶液中Al3+的物质的量为
 的物质的量浓度是
的物质的量浓度是(5)向0.1mol/LBa(OH)2溶液中匀速逐滴加入0.2 mol/LH2SO4溶液直至过量,发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液240mL:配制溶液时,一般可以分为以下几个步骤:①称量②计算③定容④溶解⑤转移⑥洗涤其正确的操作顺序为__ 。
(2)将40gNaOH配成2L溶液,其物质的量浓度为__ mol/L。
(3)FeCl3溶液中有少量的FeCl2杂质:除杂时发生的离子方程式__ 。
(4)钠投入水中发生反应的方程式___ 。如将2.3g钠投入水中,充分反应生成的NaOH的物质的量为___ mol,生成氢气的体积标准状况下为___ L,该反应的氧化剂是___ 。
(2)将40gNaOH配成2L溶液,其物质的量浓度为
(3)FeCl3溶液中有少量的FeCl2杂质:除杂时发生的离子方程式
(4)钠投入水中发生反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白。
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,该过程产生白色沉淀的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
(5)写出NaHSO4在水溶液中的电离方程式___________ 。12gNaHSO4中含有___________ 个O原子,将其溶于水配成500mL溶液,则溶液的物质的量浓度为___________ mol/L,从中取出l00mL可以消耗1mol/L的NaOH溶液___________ mL。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
| A.OH- | B. | C. | D.Cl- |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
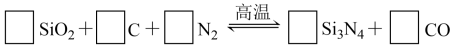
(1)配平上述反应的化学方程式(将化学计量数填在方框内);_____ SiO2+_____ C+_____ N2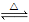
_____ Si3O4+_____ CO
(2)该反应的氧化剂是_________ ,其还原产物是_________ ;
(3)该反应产生标准状况下11.2升CO气体,则电子转移________ 摩尔。
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移______ (填大于、等于或小于)2摩尔,理由是__________________________ 。
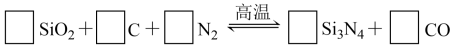
(1)配平上述反应的化学方程式(将化学计量数填在方框内);

(2)该反应的氧化剂是
(3)该反应产生标准状况下11.2升CO气体,则电子转移
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】近年来,我国研究储氢碳管获得重大进展,用电弧法合成碳纳米管,常伴有大量碳纳米颗粒生成,这种碳纳米颗粒可用氧化气化法除去,其反应的化学方程式为:
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂________ ,还原剂___________ ;
(2)硫酸在上述反应中表现出的性质是__________ (填选项编号);
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目__________ 。
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂
(2)硫酸在上述反应中表现出的性质是
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目
您最近一年使用:0次
【推荐3】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)被还原的元素是__ ,还原剂是__ ,还原产物是__ 。
(2)该反应中的氧化剂与还原剂个数之比是__ 。
(3)完成NaClO3氧化FeCl2的离子方程式:________ ClO +
+________ Fe2++________ H+=________ Cl-+________ Fe3++________ H2O(化学计量数是 1 的也请填上)
(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为___ 。
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)__ 。
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O(化学计量数是 1 的也请填上) 并用单线桥 法标出电子转移情况。
(1)被还原的元素是
(2)该反应中的氧化剂与还原剂个数之比是
(3)完成NaClO3氧化FeCl2的离子方程式:
 +
+(4)12个Na2SO3恰好与4个K2Cr2O7完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
(5)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:KMnO4+HCl(浓)═KCl+MnCl2+Cl2↑+H2O(未配平)
配平该化学方程式:___KMnO4+___HCl═____KCl+__MnCl2+__Cl2↑+__H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。下图是硫元素的“价类二维图”。
(1)硫元素在周期表中的位置为_______ ;H2S的电子式为_______ 。
(2)H2S与SO2混合时会产生淡黄色粉末,该反应的化学方程式为_______ 。
(3)实验室可用铜与浓硫酸反应制取SO2气体,该反应的化学方程式为_______ ,其中浓硫酸表现_______ 。性(填“氧化”、“还原”或“酸”)。
(4)工业上制硫酸最后阶段是吸收SO3和硫酸的生成,该阶段在吸收塔中进行,SO3蒸气从吸收塔下口通入,上口加入98.3%的浓硫酸吸收SO3,用浓硫酸吸收SO3而不用水吸收的原因是_______ 。
(5)请设计实验证明K2SO3粉末已被空气中的氧气氧化:_______ 。

(1)硫元素在周期表中的位置为
(2)H2S与SO2混合时会产生淡黄色粉末,该反应的化学方程式为
(3)实验室可用铜与浓硫酸反应制取SO2气体,该反应的化学方程式为
(4)工业上制硫酸最后阶段是吸收SO3和硫酸的生成,该阶段在吸收塔中进行,SO3蒸气从吸收塔下口通入,上口加入98.3%的浓硫酸吸收SO3,用浓硫酸吸收SO3而不用水吸收的原因是
(5)请设计实验证明K2SO3粉末已被空气中的氧气氧化:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
① 若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
② 若向①的四支试管中分别加入盐酸,B 盐的溶液有沉淀生成,D 盐的溶液有无色无味的气体逸出。根据①②实验事实请回答下列问题:
(1)A的化学式为_____________ ; B的化学式为_____________ ;
(2)写出盐酸与 D 反应的离子方程式:_________________ ;
(3)写出C溶液中阴离子的检验方法:_______________ 。
(4)利用氧化还原反应法配平:Cu + HNO3(稀)—Cu(NO3 )2+NO↑+H2O,配平后方程式为______________ ,反应中的还原剂是______ ,还原产物是______ 。
 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。① 若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
② 若向①的四支试管中分别加入盐酸,B 盐的溶液有沉淀生成,D 盐的溶液有无色无味的气体逸出。根据①②实验事实请回答下列问题:
(1)A的化学式为
(2)写出盐酸与 D 反应的离子方程式:
(3)写出C溶液中阴离子的检验方法:
(4)利用氧化还原反应法配平:Cu + HNO3(稀)—Cu(NO3 )2+NO↑+H2O,配平后方程式为
您最近一年使用:0次