利用Cu+2FeCl3=CuCl2+2FeCl2,可设计如图所示原电池装置,下列说法不正确的是
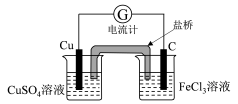

| A.该电池的负极是Cu |
| B.电池工作过程中,电子流向为:Cu→盐桥→C |
| C.盐桥中阳离子进入右池 |
| D.正极电极反应为:Fe3++e-=Fe2+ |
更新时间:2022-03-30 21:38:19
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】新型镁-锂双离子二次电池的工作原理如图。下列关于该电池的说法正确的是
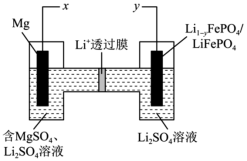
| A.放电时,Li+通过离子交换膜向左移动 |
| B.放电时,Li1-yFePO4/LiFePO4一极电极反应式为Li1-yFePO4+yLi+-ye-=LiFePO4 |
| C.充电时,x与电源的正极相连 |
| D.充电时,导线上每通过0.4mole-,左室中溶液的质量减少2g |
您最近一年使用:0次
【推荐2】氯碱工业的一种节能新工艺是将电解池与燃料电池相结合,相关物料的传输与转化关系如图所示(电极未标出)。下列说法错误的是
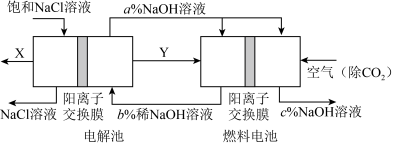
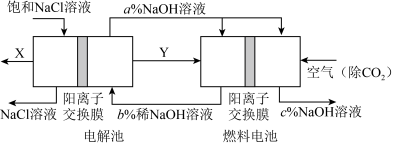
| A.电解池的阴极反应式为:2H2O+2e-═H2↑+2OH- |
| B.通入空气的电极为正极,电极反应为:O2+2H2O+4e-=4OH- |
| C.电解池中产生2molCl2时,理论上燃料电池中消耗1molO2 |
| D.a、b、c的大小关系为:c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】图中所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述正确的是( )


| A.产生气体的物质的量:(1)> (2) |
| B.电极上析出物质的质量:(1)> (2) |
| C.溶液pH的变化:(1)增大,(2)减小 |
| D.电极反应式:(1)中阳极的电极反应式为4OH--4e-=2H2O+O2↑,(2)中负极的电极反应式为2H++2e-=H2↑ |
您最近一年使用:0次
【推荐1】近日,电子科技大学孙威教授用弱酸性的醋酸锌[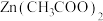 ,简写为
,简写为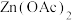 ]水溶液作为锌-空气电池的电解液,探索了碱式醋酸锌水合物[
]水溶液作为锌-空气电池的电解液,探索了碱式醋酸锌水合物[ ,简写为ZHA]可逆生成与分解的新型反应机制,工作原理示意图如图所示:
,简写为ZHA]可逆生成与分解的新型反应机制,工作原理示意图如图所示:
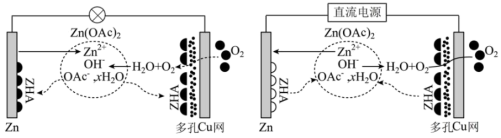
下列说法正确的是
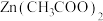 ,简写为
,简写为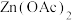 ]水溶液作为锌-空气电池的电解液,探索了碱式醋酸锌水合物[
]水溶液作为锌-空气电池的电解液,探索了碱式醋酸锌水合物[ ,简写为ZHA]可逆生成与分解的新型反应机制,工作原理示意图如图所示:
,简写为ZHA]可逆生成与分解的新型反应机制,工作原理示意图如图所示:
下列说法正确的是
| A.放电时,电子从Zn电极经电解液流向多孔Cu网电极 |
B.充电时,多孔Cu网电极的电极反应式为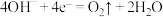 |
C.放电时的电池总反应为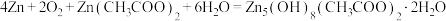 |
| D.与多孔Cu网电极相比,放电时,Zn电极电势低,充电时,Zn电极电势高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家利用垃圾渗透液研发出新型环保电池,实现发电、环保二位一体化结合的装置如图。
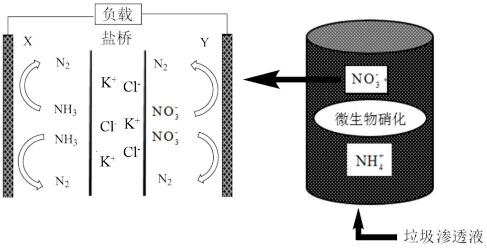
当该装置工作时,下列说法正确的是

当该装置工作时,下列说法正确的是
| A.盐桥中K+向X极移动,Cl-向Y极移动 |
| B.电路中流过3.75 mol电子时,产生N2的体积为22.4 L(标准状况) |
| C.电流由X极沿导线流向Y极 |
D.Y极反应式为2 +10e-+12H+=N2↑+6H2O +10e-+12H+=N2↑+6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是
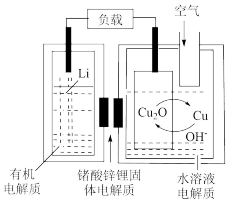

| A.该电池的负极为Li |
| B.通空气时,铜被腐蚀,表面产生Cu2O |
| C.放电时,正极的电极反应式为O2+2H2O+4e-=4OH- |
| D.若有1 mol Li+透过固体电解质时,标准状况下参与反应的O2体积为5.6 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示。质子交换膜只允许H+自由通过,下列说法错误的是
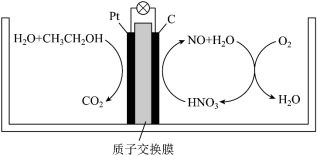

| A.电流由Pt电极流向C电极 |
| B.电池工作时正极区溶液的pH升高 |
C.常温常压下,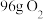 被还原同时有 被还原同时有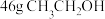 被氧化 被氧化 |
| D.负极反应为C2H5OH-12e-+3H2O=2CO2+12H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。
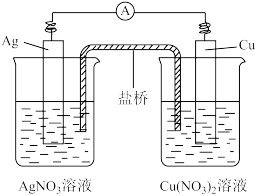
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
⑤盐桥中的K+移向Cu(NO3)2溶液
⑥电子的移动方向:Cu极-导线-Ag电极-AgNO3溶液-盐桥-Cu(NO3)2溶液
上述①~⑥中正确的有

①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
⑤盐桥中的K+移向Cu(NO3)2溶液
⑥电子的移动方向:Cu极-导线-Ag电极-AgNO3溶液-盐桥-Cu(NO3)2溶液
上述①~⑥中正确的有
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次